
���� X��Y��Z��WΪ�����ڵ�����Ԫ�أ��������������Ϊ+1��+4��+5��+7����X��Y��Z��W�ֱ�λ�ڵڢ�A�塢��A�塢��A�塢��A�壻�˵��������Y��Z��X��W��˳����������Y��Z��ԭ�Ӵ����ĵ�����Ϊ2��˵��Y��Z�����������Ӳ㣬��YΪCԪ�ء�ZΪNԪ�أ�W��Xԭ�Ӵ���������Ϊ8����WΪClԪ�ء�XΪNaԪ�أ��Դ˽����⣮
��� �⣺X��Y��Z��WΪ�����ڵ�����Ԫ�أ��������������Ϊ+1��+4��+5��+7����X��Y��Z��W�ֱ�λ�ڵڢ�A�塢��A�塢��A�塢��A�壻�˵��������Y��Z��X��W��˳����������Y��Z��ԭ�Ӵ����ĵ�����Ϊ2��˵��Y��Z�����������Ӳ㣬��YΪCԪ�ء�ZΪNԪ�أ�W��Xԭ�Ӵ���������Ϊ8����WΪClԪ�ء�XΪNaԪ�أ�
��1��������������֪��XΪ�ƣ�YΪ̼��ZΪ����WΪ�ȣ��ʴ�Ϊ���ƣ�̼�������ȣ�
��2���ǽ�����C��N�����⻯���ȶ��ԣ�CH4��NH3���ʴ�Ϊ��NH3��
��3��YΪ̼Ԫ�أ���Ԫ�����ڱ��е�λ�ã��ڶ����ڢ�A�壬�ʴ�Ϊ���ڶ����ڢ�A�壻
��4��X��Z������������Ӧ��ˮ����ֱ�ΪNaOH��HNO3�����߷�Ӧ����ʽΪ��NaOH+HNO3�TNaNO3+H2O���ʴ�Ϊ��NaOH+HNO3�TNaNO3+H2O��
��5��ZԪ�ص���̬�⻯��ΪNH3��������������Ӧ��ˮ����ΪHNO3�����߷�Ӧ�Ļ�ѧ����ʽ��NH3+HNO3�TNH4NO3���ʴ�Ϊ��NH3+HNO3�TNH4NO3��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã���ȷ�ƶ�Ԫ�ص�����Ϊ������Ĺؼ��������ڻ���֪ʶ�Ĺ��̣�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ������������Ϊ2��Ԫ��һ���������ڱ���A�� | |
| B�� | ͬ���ڵ�IA��Ԫ����ڢ�A��Ԫ���γɵ������ӻ����� | |
| C�� | ����ķе��ˮ�ķе�� | |
| D�� | ͬ����Ԫ���γɵ�������ľ������;���ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
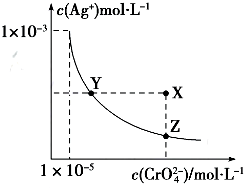
| A�� | t��ʱ��Ag2CrO4��KspΪ1��10-12 | |
| B�� | t��ʱ����Ag2CrO4��Һ�м���K2CrO4��Һ���ٴ�ƽ��ʱc2��Ag+����c��CrO42-����Ksp | |
| C�� | t��ʱ��Ksp��AgCl��=1.56��10-10 | |
| D�� | t��ʱ����0.01mol•L-1 AgNO3��Һ�ζ�20mL 0.01mol•L-1KCl��0.01mol K2CrO4�Ļ����Һ��CrO${\;}_{4}^{2-}$�ȳ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ʷ�����ѧ��Ӧ�������������仯 | |
| B�� | ���������仯�����ʱ仯���ǻ�ѧ�仯 | |
| C�� | ��һ��ȷ���Ļ�ѧ��Ӧ��ϵ�У���Ӧ������������������������������ͬ | |
| D�� | ��һ��ȷ���Ļ�ѧ��Ӧ��ϵ�У���Ӧ������������Ǹ���������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ת��0.1mol����ʱ��a�缫����1.12LH2 | |
| B�� | b�缫�Ϸ����ĵ缫��Ӧ�ǣ�2H2O+2e-=H2��+2OH- | |
| C�� | c�缫�Ͻ��л�ԭ��Ӧ��B����е�H+����ͨ����Ĥ����A�� | |
| D�� | d�缫�Ϸ����ĵ缫��Ӧ�ǣ�O2+4H++4e-=2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����Ա�����ú���� | B�� | ����Ӳ������ӣ��۷е����� | ||
| C�� | ��������ɫ����������������չ�� | D�� | ����Ӳ������ӣ��ܶ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | c��H+��=c��OH-��-c��CH3COOH�� | B�� | c��H+��+2c��Ba2+��=c��CH3COO-��+c��OH-�� | ||
| C�� | c��Ba2+����c��CH3COO-����c��OH-����c��H+�� | D�� | 2c��Ba2+��=c��CH3COO-��+c��CH3COOH�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com