
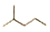
 ,其分子式为C6H14,名称是2-甲基戊烷,它可由2种炔通过加成反应得到.
,其分子式为C6H14,名称是2-甲基戊烷,它可由2种炔通过加成反应得到.| 实验步骤 | 解 释 或 实 验 结 论 |
| (1)称取A 18.0g,升温使其汽化,测其密度是相同条件下H2的45倍. | ①A的相对分子质量为90. |
(2)A的核磁共振氢谱如图: | ②A中含有4种氢原子. |
分析 (1)根据该有机物的键线式写出分子式;根据系统命名法完成该有机物的命名;-C≡C-与氢气加成生成-CH2-CH2-,则该烃可由乙炔,丁炔,两种烃炔与氢气加成得到;
(2)根据蒸馏操作装置写出使用的玻璃仪器名称;
(3)物质的相对分子质量之比等于相对密度;核磁共振氢谱有几个峰,则有几种H原子;
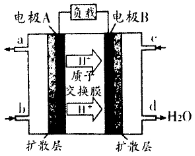
(4)由氢离子的定向移动可知A为原电池的负极,B为原电池的正极,则a通入甲醇,c通入氧气,外电路中电子从为负极到正极;负极失电子发生氧化反应.
解答 解:(1) ,分子中含有6个碳原子,属于饱和烃,分子式为C6H14;该有机物主链上有5个C,2号C一个甲基,命名为:2-甲基戊烷;-C≡C-与氢气加成生成-CH2-CH2-,则该烃可由乙炔,丁炔,2种烃炔与氢气加成得到;
,分子中含有6个碳原子,属于饱和烃,分子式为C6H14;该有机物主链上有5个C,2号C一个甲基,命名为:2-甲基戊烷;-C≡C-与氢气加成生成-CH2-CH2-,则该烃可由乙炔,丁炔,2种烃炔与氢气加成得到;
故答案为:C6H14; 2-甲基戊烷;2;
(2)含有杂质的工业乙醇的蒸馏装置中,需要使用的玻璃仪器为:酒精灯、蒸馏烧瓶、温度计、冷凝管、尾接管、锥形瓶,还缺少温度计和冷凝管,
故答案为:蒸馏烧瓶;温度计;
(3)称取A物质 18.0g,升温使其汽化,测其密度是相同条件下H2的45倍,则相对分子质量为45×2=90,
A的核磁共振氢谱有4个峰,则有4种H原子,
故答案为:90;4;
(4)由氢离子的定向移动可知A为原电池的负极,B为原电池的正极,则a通入甲醇,c通入氧气,外电路中电子从为负极到正极,即从A到B,电池负极的电极反应方程式为CH3OH-6e-+H2O=CO2+6H+,
故答案为:A;B;CH3OH-6e-+H2O=CO2+6H+.
点评 本题综合考查有机物的结构和性质,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握有机物的键线式与结构简式,把握有机物的分离、提纯方法,难度不大.


科目:高中化学 来源: 题型:实验题
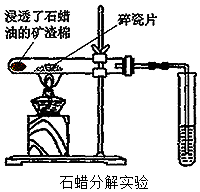 (1)完全燃烧0.1mol某烃,燃烧产物依次通过浓硫酸、浓碱液,实验结束后,称得浓硫酸增重9g,浓碱液增重17.6g.该烃的化学式C4H10,并写出其所有可能的结构简式:CH3CH2CH2CH3、CH3CH(CH3)CH3.
(1)完全燃烧0.1mol某烃,燃烧产物依次通过浓硫酸、浓碱液,实验结束后,称得浓硫酸增重9g,浓碱液增重17.6g.该烃的化学式C4H10,并写出其所有可能的结构简式:CH3CH2CH2CH3、CH3CH(CH3)CH3.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向碳酸氢钙溶液中加入少量烧碱溶液:Ca2++2HCO3-+20H-═CaCO3↓+CO32-+H2O | |
| B. | 碘水中通入足量的 S02:I2+SO2+2H2O═2I-+S042-+4H+ | |
| C. | 向氯化铝溶液中滴加过量氨水:Al3++4NH3•H2O═A1O2-+4NH4++2H2O | |
| D. | 在强碱溶液中次氯酸钠与Fe(0H)3反应生成Na2FeO4:3ClO+2Fe(OH)3═2FeO32-+3Cl-+H2O+4H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 合成纤维、光导纤维都属于有机高分子材料 | |
| B. | 氟利昂作制冷剂会加剧雾霾天气的形成 | |
| C. | 天津港爆炸案对剧毒的氰化钠(NaCN)喷洒双氧水消毒,是利用了双氧水的氧化性 | |
| D. | 利用加热的方法杀死人体内感染的埃博拉病毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 需要加热才能发生的反应,一定是吸热反应 | |
| B. | 1mol酸与碱恰好中和时所放出的热量叫中和热 | |
| C. | 化学反应中的能量变化都表现为热量的变化 | |
| D. | 化学反应中的能量变化,主要是由化学键的变化引起的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
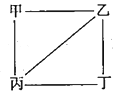 X、Y、Z、W为原子序数递增的4种短周周期元素,其中Y、Z为金属元素.X、Y、Z、W的最高价氧化物对应的水化物甲、乙、丙、丁之间存在如下图所示反应关系(图中“一”相连的两种物质能发生反应).下列判断正确的是( )
X、Y、Z、W为原子序数递增的4种短周周期元素,其中Y、Z为金属元素.X、Y、Z、W的最高价氧化物对应的水化物甲、乙、丙、丁之间存在如下图所示反应关系(图中“一”相连的两种物质能发生反应).下列判断正确的是( )| A. | X是元素周期表中非金属性最强的元素 | |
| B. | Z位于元素周期表第3周期IA族 | |
| C. | 4种原子中,Y原子半径最小 | |
| D. | W的阴离子可能促进水的电离 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com