
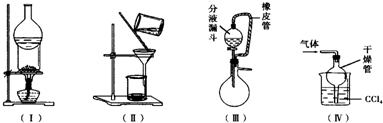
 下列实验装置用途正确的是( )
下列实验装置用途正确的是( )| A. | 装置(Ⅰ)可用于I2与NH4Cl混合物的分离 | |
| B. | 装置(Ⅱ)用于分离Fe(OH)3胶体和FeCl3溶液 | |
| C. | 装置(Ⅲ)橡皮管起到平衡气压,使液体顺利流下的作用 | |
| D. | 装置(Ⅳ)用于吸收HCl或NH3 |
分析 A.装置(I)适用于加热时易升华或易分解的物质,且易分解的物质冷却后能生成固体;
B.装置(II)适用于分离不溶性固体和液体;
C.当分液漏斗上部压强大于烧瓶内压强时,分液漏斗内液体才能顺利流下;
D.有缓冲装置的能防止倒吸,且尾气处理中,尾气能溶于该溶液.
解答 解:A.加热时碘易升华、氯化铵易分解,且氯化铵分解生成的气体遇冷会生成氯化铵固体,所以该装置不能用于分离碘和氯化铵,故A错误;
B.装置(II)适用于分离不溶性固体和液体,Fe(OH)3胶体和FeCl3溶液都能透过滤纸,所以不能用过滤方法分离,应该采用渗析方法分离,故B错误;
C.当分液漏斗上部压强大于烧瓶内压强时,分液漏斗内液体才能顺利流下,所以橡皮管起到平衡气压,使液体顺利流下的作用,故C正确;
D.该装置有缓冲作用,但四氯化碳不能吸收HCl或氨气,应该用水,故D错误;
故选C.
点评 本题考查化学实验方案评价,为高频考点,涉及物质的分离和提纯、尾气处理等实验基本操作,明确实验原理是解本题关键,知道物质分离基本方法,注意C中橡皮管作用,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
 A、B、C、D、E、F是元素周期表中前四周期的元素,原子序数依次增大,A、B是相邻的同一短周期元素,其中A元素所形成的化合物种类最多.C、D、E、F是位于同一周期的金属元素,基态C、F原子的价电子层中未成对电子均为1个,且C、F原子的电子数目相差10.基态D、E原子的价电子层中未成对电子数分别为4、2.且原子序数相差2,其中D元素是生产、生活中常见的金属.
A、B、C、D、E、F是元素周期表中前四周期的元素,原子序数依次增大,A、B是相邻的同一短周期元素,其中A元素所形成的化合物种类最多.C、D、E、F是位于同一周期的金属元素,基态C、F原子的价电子层中未成对电子均为1个,且C、F原子的电子数目相差10.基态D、E原子的价电子层中未成对电子数分别为4、2.且原子序数相差2,其中D元素是生产、生活中常见的金属.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl | B. | KOH | C. | Al2O3 | D. | MgSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
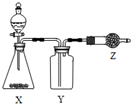 如图是用于制取、收集并吸收多余气体的装置,如表方案正确的是( )
如图是用于制取、收集并吸收多余气体的装置,如表方案正确的是( )| 选项 | X | Y | Z |
| A | 食盐、浓硫酸 | HCl | 碱石灰 |
| B | CaO、浓氨水 | NH3 | 无水CaCl2 |
| C | Cu、浓硝酸 | NO2 | 碱石灰 |
| D | 电石、食盐水 | C2H2 | 含溴水的棉花 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com