
【题目】我国科学家在太阳能可规模化分解水制氢方面取得新进展——率先提出并验证了一种全新的基于粉末纳米颗粒光催化剂太阳能分解水制氢的“氢农场”策略,其太阳能光催化全分解水制氢的效率创国际最高记录(示意图如图所示,M1、M2 为含铁元素的离子)。下列说法正确的是

A.制 O2 装置中,太阳能转化为电能
B.制 H2 装置中,交换膜为阴离子交换膜
C.系统制得1mol H2的同时可制得 1mol O2
D.制H2时阳极可发生反应:[Fe(CN)6]4––e- = [Fe(CN)6]3–
科目:高中化学 来源: 题型:
【题目】化合物X的分子式为C5H11Cl,用NaOH的醇溶液处理X,可得分子式为C5H10的两种产物Y、Z,Y、Z经催化加氢后都可得到2甲基丁烷。若将化合物X用NaOH的水溶液处理,则所得有机产物的结构简式可能是( )
A.CH3CH2CH2CH2CH2OH B.(CH3)2COHCH2CH3
C.(CH3)2CHCH2CH2OH D.(CH3)3CCH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取一小块金属钠,用滤纸吸干表面的煤油,用小刀切开后,可看到断面呈____色,具有_____光泽,但断面很快变___________,主要是由于生成一薄层_______。若把钠放在石棉网上加热,可观察到的现象是_______________ ,反应的化学方程式为_______其中还原剂为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,两圆圈相交的阴影部分表示圆圈内物质相互发生的反应。钠及其氧化物的物质的量 均为0.1 mol,水的质量为100 g。下列说法正确的是

A.甲、乙、丙都属于氧化还原反应
B.甲反应的离子方程式为Na+2H2O![]() Na++2OH-+H2↑
Na++2OH-+H2↑
C.丙充分反应,能产生0.05 mol O2,转移电子0.1 mol
D.甲、乙、丙充分反应后所得溶液的质量分数分别为w1、w2、w3,则2w1=w2=w3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学家孙予罕等发现,以泡沫镍[3 NiO/Ni(3 表示 NiO 在泡沫镍中的质量百分数)] 作为基材上的催化剂可实现将烷烃直接电催化转化为醇类(转化示意图如图所示)。下列说法正确的是
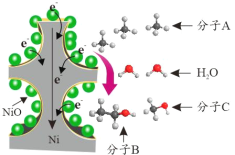
A.22.4 L A 中质子数为 10 mol
B.1mol C 中共价键数目为 4 mol
C.生成 1 mol Ni 可还原出 1 mol B
D.11.8 g 泡沫镍含 Ni 单质 0.194 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴(Co)是生产耐热合金、硬质合金、防腐合金、磁性合金和各种钴盐的重要原料,其金属性弱于 Fe 强于 Cu。某低位硫钴铜矿的成分为:CoS、CuFeS2、CaS、SiO2, 一种利用生物浸出并回收其中钴和铜的工艺流程如图:

回答下列问题:
(1)Cu2+的生物浸出原理如下:

温度超过 50℃浸出率急剧下降,其原因是_____;其他金属离子的浸出原理与上图类似, 写出由 CoS 浸出 Co2+的离子方程式_____。
(2)浸出渣的主要成分为_____。
(3)萃取分离铜的原理如下:Cu2++2(HR)org![]() (CuR2)org+2H+。根据流程,反萃取加入的试剂应该为_____(写化学式)。
(CuR2)org+2H+。根据流程,反萃取加入的试剂应该为_____(写化学式)。
(4)除铁步骤中加入 H2O2,调节溶液的 pH 至 4,将 Fe2+转化为 FeOOH 过滤除去,写出该转化的离子方程式为_____。检验 Fe2+是否完全被转化的试剂为_____。
(5)通过电解法制得的粗钴含有少量铜和铁,需要电解精炼,进行精炼时,精钴应处于_____极(填“阴”或“阳”),阳极泥的主要成分为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把18.4g由NaOH和NaHCO3组成的固体混合物在密闭容器中加热到约250摄氏度, 经充分反应后排出气体,冷却后称得固体质量为16.6g,试确定原混合物中NaOH与NaHCO3的物质的量的关系为( )
A.NaOH<NaHCO3B.NaOH>NaHCO3
C.NaOH=NaHCO3D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图所示的三个容积相同的容器①②③中进行如下反应:3A(g)+B(g) ![]() 2C(g) ΔH<0,若起始温度相同,分别向三个容器中通入3 mol A和1 mol B,则达到平衡时各容器中C物质的体积分数由大到小的顺序为( )
2C(g) ΔH<0,若起始温度相同,分别向三个容器中通入3 mol A和1 mol B,则达到平衡时各容器中C物质的体积分数由大到小的顺序为( )

A. ③②①B. ③①②C. ①②③D. ②①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用AgNO3溶液分别滴定浓度均为0.01mol/L的KCl、K2C2O4溶液,所得的沉淀溶解平衡图象如下图所示(不考虑C2O42-的水解)。下列叙述正确的是
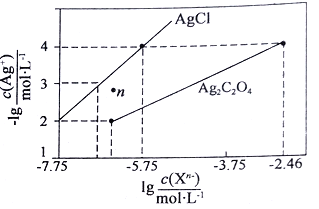
A.Ksp(Ag2C2O4)的数量级等于10-7
B.n点表示AgCl的不饱和溶液
C.向c(Cl-)=c(C2O42-)的混合液中滴入AgNO3溶液时,先生成Ag2C2O4 沉淀
D.Ag2C2O4+2C1-=2AgCl+C2O42-的平衡常数为109.04
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com