
截至到2013年12月末,中国光伏发电新增装机容量达到10.66 GW,光伏发电累计装机容量达到17.16 GW,图为利用光伏并网发电装置电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。
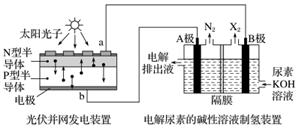
下列叙述中正确的是( )
A.N型半导体为正极,P型半导体为负极
B.制氢装置溶液中电子流向:从B极流向A极
C.X2为氢气
D.工作时,A极的电极反应式为CO(NH2)2+8OH--6e-===CO +N2↑+6H2O
+N2↑+6H2O
 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案科目:高中化学 来源: 题型:
对比以下几个反应式:
Cl+Cl―→Cl2,ΔH=-247 kJ·mol-1;
O+O―→O2,ΔH=-493 kJ·mol-1;
N+N―→N2,ΔH=-946 kJ·mol-1。
可以得出的结论是( )
A.在常温下氮气比氧气和氯气稳定
B.氮、氧和氯的单质常温下为气体
C.氮、氧和氯都是双原子分子
D.氮气、氧气和氯气的密度不同
查看答案和解析>>
科目:高中化学 来源: 题型:
根据2CrO +2H+??Cr2O
+2H+??Cr2O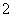 7+H2O设计图示装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图中右侧电极连接电源的______极,其电极反应式为_________________________。
7+H2O设计图示装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图中右侧电极连接电源的______极,其电极反应式为_________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
H3PO2也可用电渗析法制备。“四室电渗析法”工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):
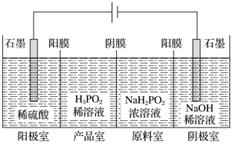
①写出阳极的电极反应式______________________________________________。
②分析产品室可得到H3PO2的原因__________________________________________
________________________________________________________________________。
③早期采用“三室电渗析法”制备H3PO2:将“四室电渗析法”中阳极室的稀硫酸用H3PO2稀溶液代替。并撤去阳极室与产品室之间的阳膜,从而合并了阳极室与产品室。其缺点是产品中混有____________杂质。该杂质产生的原因是________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
现将氯化铝溶液蒸干灼烧并熔融后用铂电极进行电解,下列有关电极产物的判断正确的是( )
A.阴极产物是氢气
B.阳极产物是氧气
C.阴极产物是铝和氧气
D.阳极产物只有氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
铜与稀硫酸不反应,某校实验小组的同学在老师的指导下设计了下列装置,实现了铜与稀硫酸的反应。请回答下列问题:
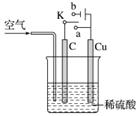
(1)甲同学认为在通入空气的同时,将开关K与______(填“a”或“b”)连接,即可实现。则此时石墨电极的反应式为__________________,电池的总反应式为________________________。电池工作时,H+向________(填“C”或“Cu”)极移动。
(2)乙同学认为,不通入空气,将K与______(填“a”或“b”)连接,也可以实现。则Cu极的电极反应式为________________________,总反应的离子方程式为________________________。若标准状况下产生2.24 L气体,则电路中转移的电子为______mol。
(3)丙同学认为还可以用如图所示装置模拟工业上电镀铜。他认为只要将C换成Fe(Cu足量),并将乙同学的实验持续足够长时间,即可实现在Fe上镀Cu。你认为他的想法______(填“正确”或“不正确”),理由是______________。这种方法得到的铜镀层______(填“牢固”或“不牢固”),理由是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知Al2O3(s)+AlCl3(g)+3C(s)===3AlCl(g)+3CO(g) ΔH=a kJ·mol-1
判断下列变化过程是否正确,正确的划“√”,错误的划“×”
(1)3AlCl(g)+3CO(g)===Al2O3(s)+AlCl3(g)+3C(s)
ΔH=a kJ·mol-1( )
(2)AlCl(g)+CO(g)===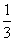 Al2O3(s)+
Al2O3(s)+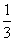 AlCl3(g)+3C(s)
AlCl3(g)+3C(s)
ΔH=-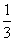 a kJ·mol-1( )
a kJ·mol-1( )
(3)2Al2O3(s)+2AlCl3(g)+6C(s)===6AlCl(g)+6CO(g)
ΔH=-2a kJ·mol-1( )
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com