
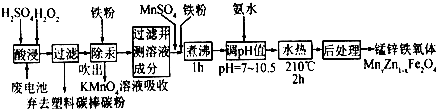
���� �ϵ������õ���Һ��Һ����Ҫ������������Mn2+��Hg2+��Zn2+���������۳�Hg��������������KMnO4��Һ���գ����������Һ�к�������п�����������������̵ȣ�����MnSO4�����ۣ�������Һ���ӵijɷ֣���г�ȥ˫��ˮ����ˮ�ȣ����к�����Ҳ�ܵõ���п�����壬
��1�����ʱ��˫��ˮ�����������������������̻�ԭ���������̣���Ӧ����ˮ���ɣ�
��2���������۰�Hg��ԭ������
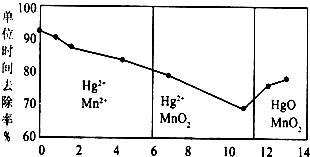
��3������ͼ��֪��pH��6ʱHg�����Ը�����ط�Ӧ����Hg2+��Mn2+��
����ͼ��֪����pHֵ�����߹���ȥ�����Ƚ��ͺ����ӣ�
��������������Mn2+���ɣ�������Mn2+���д����ã�
��4��MnΪ+2�ۡ�ZnΪ+2�ۣ����û��ϼ۴�����Ϊ0������FeԪ�ػ��ϼۣ��ٽ��Mg��Zn��Feԭ����Ŀ֮�ȸ�дΪ��������ʽ��
��5�����������Һ�к�������п�����������������̡�����ȣ�������MnSO4�����ۣ����к���������Ҳ�ܵõ���п�����壬��ʵ���м��������һ������MnSO4�����ۣ�Ӧ�ǵ�����Һ���ӵijɷ֣�����ˮ�Ⱥ�����п����������ɣ�
��� �⣺��1�����ʱ��˫��ˮ�����������������������̻�ԭ���������̣���Ӧ����ˮ���ɣ���Ӧ����ʽΪ��MnO2+H2O2+H2SO4=MnSO4+O2��+2H2O��
�ʴ�Ϊ��MnO2+H2O2+H2SO4=MnSO4+O2��+2H2O��
��2�����۾��л�ԭ�ԣ��ܰѹ����ӻ�ԭΪ�����ʣ��������۵������ǻ�ԭ�����ʴ�Ϊ����ԭ����
��3������ͼ��֪��pH��6ʱHg�����Ը�����ط�Ӧ����Hg2+��Mn2+����Ӧ���ӷ���ʽΪ��5Hg+2MnO4-+16H+=5Hg2++2Mn2++8H2O��
�ʴ�Ϊ��5Hg+2MnO4-+16H+=5Hg2++2Mn2++8H2O��
����ͼ���֪����������������PH�������Ƚ��ͺ����ӣ�
�ʴ�Ϊ����pH�����߹����������Ƚ��ͺ����ӣ�
�۲�����������������������ǿ���أ�������������Mn2+���ɣ�������Mn2+���д����ã�ǿ���Ի����¹��ĵ�λʱ��ȥ���ʸߣ�
�ʴ�Ϊ��Mn2+ ���д����ã���λʱ����ȥ���ʸߣ�
��4��MnΪ+2�ۡ�ZnΪ+2�ۣ���x=0.2ʱ�����û��ϼ۴�����Ϊ0����֪FeԪ�ػ��ϼ�Ϊ+3����дΪ��������ʽΪ��MnO•4ZnO•5Fe2O3��
�ʴ�Ϊ��MnO•4ZnO•5Fe2O3��
��5�����������Һ�к�������п�����������������̡�����ȣ�������MnSO4�����ۣ����к���������Ҳ�ܵõ���п�����壬��ʵ���м��������һ������MnSO4�����ۣ�Ӧ�ǵ�����Һ���ӵijɷ֣�����ˮ�Ⱥ�����п����������ɣ�
�ʴ�Ϊ��������Һ���ӵijɷ֣�����ˮ�Ⱥ�����п����������ɣ�
���� ���⿼�黯ѧ�������̡����ʵķ����ᴿ���Բ����ķ������ۡ���ͼ��ȡ��Ϣ�����ȣ����ؿ���ѧ����֪ʶ��Ǩ�����ã��Ѷ��еȣ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �ڢ�A��ĵ����ס��飨As����Ԫ���ڻ������г����ֳ���������̬�����ڢ�A��Ԫ�صĻ��������о�����������������Ҫ��;��
�ڢ�A��ĵ����ס��飨As����Ԫ���ڻ������г����ֳ���������̬�����ڢ�A��Ԫ�صĻ��������о�����������������Ҫ��;�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HCl | B�� | FeCl2 | C�� | KOH | D�� | Na2CO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | FeCl3��Һ | B�� | Ca��OH��2������Һ | C�� | CuSO4��Һ | D�� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 mol Na2O2�к��е���������Ϊ2NA | |
| B�� | ��״���£���H2O2�Ƶ�2.24LO2ת�Ƶĵ�����ĿΪ0.4NA | |
| C�� | ���³�ѹ�£�8g O3����4 NA������ | |
| D�� | �����£�1L pH=2��H2SO4��Һ�к��е�H+��ĿΪ0.02NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
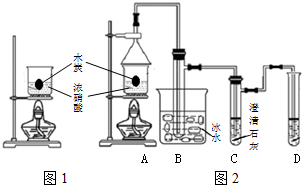 Ũ������һ�ֳ������ᣬ���Ȼ�����ֽ�����NO2��ijʵ��С����̽��̼��Ũ����ķ�Ӧ�����ʵ��װ����ͼ���ش��������⣺
Ũ������һ�ֳ������ᣬ���Ȼ�����ֽ�����NO2��ijʵ��С����̽��̼��Ũ����ķ�Ӧ�����ʵ��װ����ͼ���ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
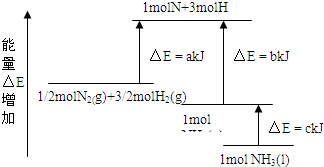
| A�� | N2��g��+3H2��g��?2NH3��g������H=2��b-a�� kJ/mol | |
| B�� | N2��g��+3H2��g��?2NH3��l������H=2��a-b-c�� kJ/mol | |
| C�� | $\frac{1}{2}$N2��g��+$\frac{3}{2}$H2��g��?NH3��l������H=��b+c-a�� kJ/mol | |
| D�� | $\frac{1}{2}$N2��g��+$\frac{3}{2}$H2��g��?NH3��g������H=��a+b�� kJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ö����ЧӦ����������Һ�ͽ��� | |
| B�� | ���ȱ���FeCl3��Һ����ȡFe��OH��3���� | |
| C�� | ������ɫ��Ӧ���Լ���NaCl��KNO3��Na2SO4 | |
| D�� | ��Ca��OH��2��Һ��������Na2CO3��NaHCO3��Һ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com