
| A�� | �٢� | B�� | �ۢ� | C�� | �٢ۢ� | D�� | �٢ۢ� |
���� �ٵ�������������˫ԭ�ӷ��ӣ������11.2L�����������ʵ���Ϊ0.5mol������1molԭ�ӣ�
�����Ϊ��ԭ�ӷ��ӣ�
����Һ���δ֪��
���Ȼ�������ˮ��ȫ����������Ӻ������ӣ�
�ݸ���O2��O3������ԭ�ӹ��������㣻
��� �⣺�ٱ�״���£�11.2L��������ʵ���Ϊ0.5mol��0.5mol�����������Ļ�������к���1molԭ�ӣ�������ԭ����ΪNA������ȷ��
��ͬ��ͬѹ�£������Ħ�������ͬ���������ͬ����������������ʵ�����ͬ�������ķ�������ȣ���ԭ����֮��Ϊ��2��1���ʴ���
����Һ���δ֪����������Һ�������Ӹ������ʴ���
���Ȼ�������ˮ��ȫ����������Ӻ������ӣ����������ʷ��ӣ��ʴ���
��O2��O3������ԭ�ӹ��ɣ�32gO2��O3���е���ԭ�ӵ����ʵ���n=$\frac{m}{M}$=$\frac{32g}{16g/mol}$=2mol���ʺ���ԭ����Ϊ2NA������ȷ��
��ѡ��A��
���� ���⿼���˰���٤���������йؼ��㣬�������չ�ʽ��ʹ�ú����ʵĽṹ�ǽ���ؼ����ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
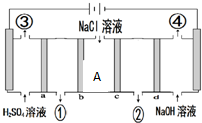
| A�� | a��cΪ�����ӽ���Ĥ��b��dΪ�����ӽ���Ĥ | |
| B�� | ������������������Ϊ1��1 | |
| C�� | �ٴ����ɵ�����Ϊ�������� | |
| D�� | ��ת��2mol e-ʱ��A������������Ϊ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 28g��ϩ�������õ��Ӷ���ĿΪ4NA | |
| B�� | 1 mol����-CH3�������ĵ�������Ϊ9NA | |
| C�� | 0.5 mol1��3-����ϩ�����к���C=C˫����ΪNA | |
| D�� | ��״���£�11.2 L��������������Ϊ0.5 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
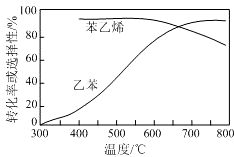 �ұ��������Ʊ���ϩ��Ӧ��
�ұ��������Ʊ���ϩ��Ӧ��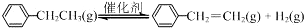
| ��ѧ�� | C-H | C-C | C=C | H-H |
| ����/kJ•mol?1 | 412 | 348 | 612 | 436 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ֻ��̼���������ˮ | |
| B�� | ֻ��CO2��ˮ | |
| C�� | ������̼�������ˮ������Ԫ�صĻ����� | |
| D�� | ��CO��CO2��ˮ������Ԫ�صĻ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
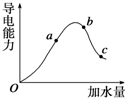 ��25��ʱ���������ˮϡ��������Һ�ĵ��������仯������ͼ��ʾ����ش�
��25��ʱ���������ˮϡ��������Һ�ĵ��������仯������ͼ��ʾ����ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | �ζ����������Ǵ��ڣ�Ka��Kh | |
| B�� | �����ʾ��Һ�д��ڣ�c��Na+��=c��A-�� | |
| C�� | �����ʾ��Һ�д��ڣ�c��Na+��=c��A-��+c��HA�� | |
| D�� | ������ʾ��Һ�м�ˮ��$\frac{c��{A}^{-}��}{c��O{H}^{-}��•c��HA��}$��ֵ��С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�������и�������Ӧ�Կ��Զ���ѧ�Ծ��������棩 ���ͣ������
[��ѧ��ѡ��2����ѧ�뼼��]
��ҵ��ͭ�ķ������ɻ�ͭ����Ҫ�ɷ���CuFeS2,���ʲ���ͭԪ�أ����ƾ�ͭ�Ĺ�������ʾ��ͼ��ͼ��
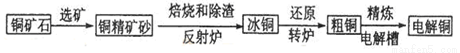
��1������ͭ����ͭ����������Ϊ0.4������1�ִ�ͭ��������Ҫ���ֻ�ͭ��____________�֡�
��2�����ڷ���¯�У���ͭ����ɰ��ʯӢɰ��ϼ��ȵ�1000�����ң���ͭ���������Ӧ����Cu��Fe�ĵͼ����_____________________���Ҳ���Fe������ת��ΪFe�ĵͼ������
��3�����ӻ��������ͳ������ԭ�ϽǶȿ���δ��������ò�����������___________��
��4������ת¯�У���ͭ�е�Cu2S�ȱ�������Cu2O��,���ɵ�Cu2O����Cu2S��Ӧ��������Ӧ���Ȼ�ѧ����ʽΪ����2Cu2S��s��+3O2��g���T2Cu2O��s����+2SO2��g����H=-768.2kJ.mol-1
��2Cu2O��s��+Cu2S��s���T6Cu��s��+SO2��g����H=+116.0kJ.mol-1
��ӦCu2Sת��Ϊͭ���Ȼ�ѧ����ʽ��_________________________��
��3molCu2S��һ�����Ŀ����������������������Ϊ4:1�����ܱ������г�ַ�Ӧ�����������Ӧ����ȫ��Cu2S��ȫ���뷴Ӧ�����õ�����ͭ3mol������������SO2���������Ϊ_____________��
��5������⾫��ͭ���������ҺΪ______________�����һ��ʱ��������Һ��Ũ��_____________������١��������䡱��������
��6�������ڷ�ӦCu+H2O2+H2SO4=CuSO4+2H2O�����Ʊ�CuSO4�������÷�Ӧ���Ϊԭ��أ��������缫��ӦʽΪ__________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com