
| A. | NH4+ | B. | Mg2+ | C. | Fe2+ | D. | Fe3+ |
科目:高中化学 来源: 题型:解答题
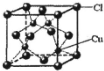 ,其中Cl-的配位数为4,已知晶胞的棱长为dcm,用NA表示阿伏加德罗常数值,则晶胞的密度表达式为$\frac{396}{{d}^{3}•{N}_{A}}$g/cm3.
,其中Cl-的配位数为4,已知晶胞的棱长为dcm,用NA表示阿伏加德罗常数值,则晶胞的密度表达式为$\frac{396}{{d}^{3}•{N}_{A}}$g/cm3.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
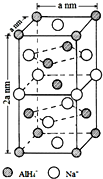
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na通常保存在煤油中,而同族的Li只能保存在液体石蜡中 | |
| B. | 金刚石与石墨互为同素异形体,已知 燃烧热金刚石更高,则石墨比金刚石更稳定 | |
| C. | X的化学式为Na2CO3,若Mg 与CO2则生成MgO和C | |
| D. | 当有0.4molNa参与反应时,被氧化的CO2为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ①③④ | C. | ①②③④ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在铁制品上镀铜时,镀件为阳极,铜盐为电镀液 | |
| B. | 铁管上镶嵌锌块,铁管不易被腐蚀 | |
| C. | 生铁中含有碳,抗腐蚀能力比纯铁弱 | |
| D. | 将海水中的钢铁闸门与电源的负极相连,可防止闸门被腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
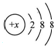 其中:
其中:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 在一定温度下,1L的密闭容器内某一反应M、N的物质的量随反应时间变化的曲线如图所示,下列表述中正确的是( )
在一定温度下,1L的密闭容器内某一反应M、N的物质的量随反应时间变化的曲线如图所示,下列表述中正确的是( )| A. | t1时,N的浓度是M的浓度的2倍 | |
| B. | t2时,正逆反应速率相等,反应达到平衡 | |
| C. | t3时,正反应速率大于逆反应速率 | |
| D. | 反应的化学方程式为:M?2N |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | b是电池的负极 | |
| B. | HS-在硫氧化菌作用下转化为SO42-的反应是:HS-+4H2O-8e-═SO42-+9H+ | |
| C. | 该电池在高温下进行效率更高 | |
| D. | 若该电池有0.4 mol 电子转移,则有0.45 mol H+通过质子交换膜 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com