
【题目】体积均为aL的盐酸和碳酸钠溶液,将碳酸钠溶液逐渐加入盐酸中与将盐酸逐渐加入碳酸钠溶液中产生的气体体积比为x:y(同温同压,且x不等于y),则原碳酸钠与盐酸溶液中溶质的物质的物质的量浓度之比为( )
A. x :y B. (x-2y) :x C. 2x :(2x-y) D. (2x-y) :2x
【答案】D
【解析】若盐酸过量,将Na2CO3溶液逐渐加入盐酸中与将盐酸逐渐加入Na2CO3溶液中产生的CO2在同温同压下的体积应相等,由于x不等于y,则盐酸不足,Na2CO3溶液过量。设原Na2CO3溶液中Na2CO3物质的量为m,原盐酸中HCl物质的量为n,将Na2CO3溶液逐渐加入盐酸中发生的反应为Na2CO3+2HCl=2NaCl+H2O+CO2↑,生成的CO2以HCl计算,生成CO2物质的量为![]() ;将盐酸逐渐加入Na2CO3溶液中依次发生的反应为Na2CO3+HCl=NaHCO3+NaCl、NaHCO3+HCl= NaCl+H2O+CO2↑,第一步消耗HCl物质的量为m,则第二步消耗HCl物质的量为(n-m),生成CO2物质的量为(n-m);根据阿伏加德罗定律,
;将盐酸逐渐加入Na2CO3溶液中依次发生的反应为Na2CO3+HCl=NaHCO3+NaCl、NaHCO3+HCl= NaCl+H2O+CO2↑,第一步消耗HCl物质的量为m,则第二步消耗HCl物质的量为(n-m),生成CO2物质的量为(n-m);根据阿伏加德罗定律, ![]() :(n-m)=x:y,m:n=(2x-y):2x;盐酸和碳酸钠溶液的体积都为aL,则原碳酸钠溶液与盐酸溶液物质的量浓度之比为(2x-y):2x,答案选D。
:(n-m)=x:y,m:n=(2x-y):2x;盐酸和碳酸钠溶液的体积都为aL,则原碳酸钠溶液与盐酸溶液物质的量浓度之比为(2x-y):2x,答案选D。


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验,能达到实验目的是( ) 
A.用图1 所示装置除去Cl2中含有的少量HCl
B.用图2 所示装置蒸干NH4HCO3饱和溶液制备NH4HCO3晶体
C.用图3 所示装置制取少量纯净的CO2气体
D.用图4 所示装置分离CCl4萃取碘水后已分层的有机层和水层
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示.下列有关微生物电池的说法错误的是( ) 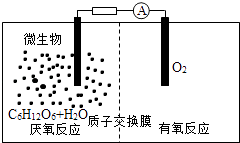
A.正极反应中有CO2生成
B.微生物促进了反应中电子的转移
C.质子通过交换膜从负极区移向正极区
D.电池总反应为C6H12O6+6O2═6CO2+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物Ⅲ是合成中药黄芩中的主要活性成分的中间体,合成方法如下: 
下列有关叙述正确的是( )
A.I的分子式为C9H10O4
B.II中所有原子有可能均共面
C.可用FeCl3溶液鉴别有机物I和III
D.1 mol产物III与足量溴水反应,消耗Br2的物质的量为1.5 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:反应aA(g)+bB(g)cC(g)某温度下,在2L的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示. 
(1)从反应开始到12s时,用A表示的 反应速率为;
(2)经测定前4s内v(C)=0.05molL﹣1s﹣1 , 则该反应的化学方程式为;
(3)请在图中将生成物C的物质的量浓度随时间的变化曲线绘制出来;
(4)若上述反应分别在甲、乙、丙 三个相同的密闭容器中进行,经同一段时间后,测得三个容器中的反应速率分别为: 甲:v(A)=0.3molL﹣1s﹣1;
乙:v(B)=0.12molL﹣1s﹣1;
丙:v(C)=9.6molL﹣1min﹣1;
则甲、乙、丙三个容器中反应速率由快到慢的顺序为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)22克CO2的物质的量为_________mol,其中含有O原子的个数为_____________,含质子的物质的量为____mol,该气体在标准状况下的体积为_________L。
(2)写出下列反应的离子方程式。Fe2O3与稀盐酸反应_________________________________
(3)写出下列离子方程式对应的任意一个化学方程式。2H++CO32-![]() CO2↑+H2O __________________________________;
CO2↑+H2O __________________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料。实验室模拟工业上以铝土矿为原料制取Al2(SO4)3和铵明矾晶体[NH4Al(SO4)2·12H2O]的工艺流程如图所示:

请回答下列问题:
(1)固体a的化学式为________。
(2)写出Ⅱ中加过量的烧碱涉及到的反应离子方程式______________、_____________;Ⅲ中通入足量CO2气体发生反应的离子方程式为_________________。
(3)由Ⅲ中得到滤液c的实验操作为__________,从铵明矾溶液中获得铵明矾晶体的实验操作依次为(填操作名称)________、冷却结晶、过滤洗涤。
(4)滤液c显________性,日常生活中常用其溶质来________________(任写一点);
(5)若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的物质的量之比为1∶1,则投料时铝土矿中的Al2O3和H2SO4的物质的量之比为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com