
【题目】(1)现有下列十种物质:①蔗糖②熔融NaCl③石墨④铜丝⑤NaOH固体⑥SO2⑦NaHSO4固体⑧K2O固体⑨液态H2SO4⑩饱和FeCl3溶液 上述物质中可导电的是________(填序号,下同);上述物质中不能导电,但属于电解质的是_______________________。
(2)NaHSO4是一种酸式盐,请填写下列空白:
①NaHSO4晶体熔化时的电离方程式为______________________________。
②3 mol·L-1 NaHSO4与2 mol·L-1 Ba(OH)2溶液等体积混合,该反应总的离子方程为___________。
(3)实验室制备少量Fe(OH)3胶体所用的物质有__________(填序号),反应的离子方程式为________________________________________________。
(4)某强酸性反应体系中,反应物和生成物共六种物质:O2、MnO4-、H2O、Mn2+、H2O2、H+,已知该反应中H2O2只发生了如下过程:H2O2→O2。写出该反应的离子方程式:_________________________。
【答案】 ②③④⑩ ⑤⑦⑧⑨ NaHSO4(熔融) =Na++ HSO4- 3H++2SO42-+2Ba2++3OH-=2BaSO4↓+3H2O ⑩ Fe3+ +3H2O ![]() Fe(OH)3(胶体) +3H+ 5H2O2+2MnO4-+6H+=5O2↑+2Mn2++8 H2O
Fe(OH)3(胶体) +3H+ 5H2O2+2MnO4-+6H+=5O2↑+2Mn2++8 H2O
【解析】(1)①蔗糖非电解质,不导电;②熔融的NaCl是电解质,能导电;③石墨能导电;④铜丝能导电;⑤NaOH固体不导电,但是电解质;⑥SO2是非电解质,不导电;⑦NaHSO4固体不导电,但是电解质;⑧K2O固体不导电,但是电解质;⑨液态H2SO4不导电,但是电解质;⑩饱和FeCl3溶液能导电,但既不是电解质也不是非电解质;因此能导电的是②③④⑩,属于电解质的是⑤⑦⑧⑨;
(2)①NaHSO4晶体熔化时的电离方程式为:NaHSO4(熔融)=Na++HSO4-;②3 molL-1 NaHSO4与2 molL-1 Ba(OH)2溶液等体积混合时,Ba2+完全转化为沉淀,H+反应完全,该反应总的离子方程式为3H++2SO42-+2Ba2++3OH-=2BaSO4↓+3H2O;
(3)制备氢氧化铁胶体的方法是向沸水中低价饱和的FeCl3溶液,所以选⑩,离子方程式为:Fe3++3H2O![]() Fe(OH)3(胶体)+3H+;
Fe(OH)3(胶体)+3H+;
(4)根据以上分析,依据电子得失总数相等配平离子方程式为:5H2O2+2MnO4-+6H+=5O2↑+2Mn2++8 H2O


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】完全燃烧一定量的乙烯与某烷烃的混合气体后,测得其生成物中气体的质量是反应前混合烃质量的2.86倍,试通过计算确定该气态烷烃的分子式及它在该混合气体中所占的物质的量分数(气体体积和质量均在常温下测定)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某市对大气进行监测,发现该市首要污染物可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此PM2.5、SO2、NO2等你进行研究具有重要意义.请回答下列问题:
(1)对PM2.5样本用适量蒸馏水处理制成待测试样.测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
离子 | K+ | Na+ | NH4+ | SO42﹣ | NO3﹣ | Cl﹣ |
浓度/molL﹣1 | 4×10﹣6 | 6×10﹣4 | 2×10﹣5 | 4×10﹣5 | 3×10﹣5 | 2×10﹣5 |
根据表中数据判断PM2.5的酸碱性为 , 试样的PH值= .
(2)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料.
已知:H2(g)+ ![]() O2(g)=H2O(g)△H=﹣241.8kJ/mol﹣1
O2(g)=H2O(g)△H=﹣241.8kJ/mol﹣1
C(s)+ ![]() O2(g)=CO(g)△H=﹣110.5kJ/mol﹣1
O2(g)=CO(g)△H=﹣110.5kJ/mol﹣1
写出焦炭与水蒸气反应的热化学方程式:
②洗涤含SO2的烟气.以下物质可作为洗涤剂的是 .
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(3)汽车尾气中NOx和CO的生成及转化
①已知气缸中生成NO的反应为:N2(g)+O2(g)2NO(g)△H>0.
若1mol空气含0.8mol N2和0.2mol O2 , 1300℃时在密闭容器内反应达到平衡.测得NO的物质的量为8×10﹣4mol,计算该温度下的平衡常数K= . 汽车启动后,气缸温度越高,单位时间内NO排放量越大,原因是
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g),已知该反应的△H>0,简述该设想能否实现的依据:;
③目前,在汽车尾气系统中装置催化转化器可减少CO和NO的污染,其化学反应方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,水溶液中H+和OH﹣的浓度变化曲线如图,下列说法正确的是( ) 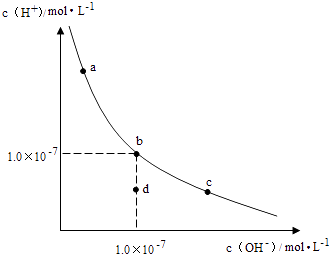
A.升高温度,可能引起由c向b的变化
B.该温度下,水的离子积常数为1.0×10﹣13
C.该温度下,加入FeCl3可能引起由b向a的变化
D.该温度下,稀释溶液可能引起由c向d的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式: ①Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H1=﹣26.7kJmol﹣1
②3Fe2O3(s)+CO(g)═2Fe3O4(s)+CO2(g)△H2=﹣50.75kJmol﹣1
③Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H3=﹣36.5kJmol﹣1
则反应FeO(s)+CO(g)═Fe(s)+CO2(g)的焓变为( )
A.+7.28 kJmol﹣1
B.﹣7.28 kJmol﹣1
C.+43.68 kJmol﹣1
D.﹣43.68 kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白磷有剧毒,白磷中毒可用硫酸铜溶液解毒,白磷与硫酸铜可以发生如下两个反应:
(1)2P+5CuSO4+8H2O![]() 5Cu+2H3PO4+5H2SO4
5Cu+2H3PO4+5H2SO4
(2)11P+15CuSO4+24H2O![]() 5Cu3P+6H3PO4+15H2SO4
5Cu3P+6H3PO4+15H2SO4
下列有关说法中错误的是
A. 在上述两个反应中,水既不是氧化剂也不是还原剂
B. 在上述两个反应中,氧化产物都是H3PO4
C. 在反应(2)中,当有5molCuSO4发生反应时,共转移10mol电子
D. 在上述两个反应中,氧化剂都只有硫酸铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,某同学向100mL H2S饱和溶液中通入SO2 , 所得溶液pH变化如图所示.下列分析中正确的是( ) 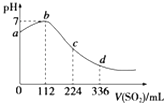
A.b点对应的溶液导电性最强
B.亚硫酸是比氢硫酸更弱的酸
C.ab段反应是SO2+2H2S═3S↓+2H2O
D.原H2S溶液的物质的量浓度为0.05molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锡及其化合物在生产、生活中有着重要的用途.已知:Sn的熔点为231℃;Sn2+易水解、易被氧化;SnCl4极易水解、熔点为﹣33℃、沸点为114℃.请按要求回答下列相关问题:
(1)元素锡比同主族碳的周期数大3,锡的原子序数为 .
(2)用于微电子器件生产的锡粉纯度测定:①取1.19g试样溶于稀硫酸中(杂质不参与反应),使Sn完全转化为Sn2+;②加入过量的Fe2(SO4)3;③用0.1000mol/L K2Cr2O7溶液滴定(产物中Cr呈+3价),消耗20.00mL.步骤②中加入Fe2(SO4)3的作用是;此锡粉样品中锡的质量分数: .
(3)用于镀锡工业的硫酸亚锡(SnSO4)的制备路线如下: 
①步骤Ⅰ加入Sn粉的作用:及调节溶液pH.
②步骤Ⅱ用到的玻璃仪器有烧杯、、 .
③步骤Ⅲ生成SnO的离子方程式: .
④步骤Ⅳ中检验SnO是否洗涤干净的操作是 , 证明已洗净.
⑤步骤Ⅴ操作依次为、、过滤、洗涤、低温干燥.
(4)SnCl4蒸气遇氨及水汽呈浓烟状,因而可制作烟幕弹,其反应的化学方程式为 .
实验室欲用下图装置制备少量SnCl4(夹持装置略),该装置存在明显缺陷,改进方法是 . 
利用改进后的装置进行实验,当开始装置C中收集到有SnCl4时即可熄灭B处酒精灯,反应仍可持续进行的理由是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com