
| A. | H2燃烧生成1 mol H2O(g)时,放出241.8 kJ的热量 | |
| B. | O2前面的$\frac{1}{2}$表示参加反应的O2的分子数目 | |
| C. | 燃烧热是以在101 kPa时,1 mol可燃物完全燃烧生成稳定的氧化物时所放出的热量定义的,则 H2的燃烧热为285.8 kJ•mol-1 | |
| D. | 1 mol H2和$\frac{1}{2}$ mol O2所具有的总能量大于1mol H2O(g)所具有的总能量 |
分析 热化学方程式是表示化学反应中的物质变化和焓变(能量变化)的方程式.△H为“-”为放热反应,△H为“+”为吸热反应.热化学方程式中化学计量数只表示该物质的物质的量,不表示物质分子个数或原子个数,它可以是整数,也可以是分数.
解答 解:A.热化学方程式中△H为“-”为放热反应,根据H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ/mol;可知:1molH2燃烧生成1molH2O(g)时,放出241.8kJ的热量.故A正确;
B.热化学方程式中化学计量数只表示该物质的物质的量,故O2前面的$\frac{1}{2}$表示参加反应的O2的物质的量,不表示参加反应的O2的分子数目,故B错误;
C.在25℃和101kPa时,1 mol可燃物完全燃烧生成稳定的化合物时所放出的热量,叫做该物质的燃烧热.根据H2(g)+$\frac{1}{2}$O2(g)═H2O(1)△H=-285.8kJ/mol.可知:1molH2燃烧生成稳定的1molH2O(1)放出285.8kJ的热量,则H2的燃烧热为285.8 kJ•mol-1,故C正确;
D.根据H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ/mol;反应放热,所以1 mol H2和$\frac{1}{2}$ mol O2所具有的总能量大于1mol H2O(g)所具有的总能量,故D正确.
故选B.
点评 掌握热化学方程式的意义,掌握燃烧热的定义,注意单位的使用,是解答本题的关键.


科目:高中化学 来源: 题型:选择题
| A. | Na2O2可用作呼吸面具中氧气的来源 | |
| B. | Na2O 和Na2O2投入水中都能生成NaOH | |
| C. | Na2O2和Na2O 均可以露置在空气中保存 | |
| D. | NaCl的性质稳定,可用作调味品 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2△H和2K | B. | -2△H和K2 | C. | 2△H和-2K | D. | -2△H和K-2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
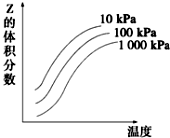 图是温度和压强对X+Y?2Z反应影响的示意图.图中横坐标表示温度,纵坐标表示平衡时混合气体中Z的体积分数.下列叙述正确的是( )
图是温度和压强对X+Y?2Z反应影响的示意图.图中横坐标表示温度,纵坐标表示平衡时混合气体中Z的体积分数.下列叙述正确的是( )| A. | 上述可逆反应的正反应为放热反应 | B. | X、Y、Z均为气态 | ||
| C. | 增大压强平衡向正反应方向移动 | D. | 上述反应的逆反应的△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碘的CCl4溶液呈紫红色 | |
| B. | 碘在CCl4中的溶解度比在水中的溶解度大 | |
| C. | 萃取时,要充分振荡混合液体并适当旋转活塞排气减压 | |
| D. | 分液时,水从分液漏斗下口流出,碘的CCl4溶液从漏斗上口倒出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 重氢原子:${\;}_{1}^{2}$D | |
| B. | S2-的结构示意图: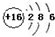 | |
| C. | 质子数为53,中子数为78的碘原子:${\;}_{53}^{131}$I | |
| D. | N2的电子式: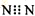 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯和液溴在FeBr3催化作用下生成溴苯 | |
| B. | 丙烯和氯气在一定条件下反应生成ClCH2CH=CH2的反应 | |
| C. | 乙烯使酸性高锰酸钾溶液褪色 | |
| D. | 乙烯与HCl气体反应生成一氯乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤、石油是不可再生能源,天然气是可再生能源 | |
| B. | 在化学反应中,反应物转化为生成物的同时,必然发生能量的变化 | |
| C. | 热值指在一定条件下,1mol的物质完全燃烧所放出的热量 | |
| D. | 若化学过程中断开化学键放出的能量大于形成化学键所吸收的能量,则反应放热 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
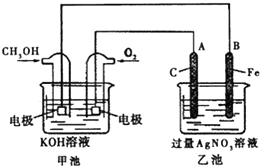 人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中的信息,填写空格.
人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中的信息,填写空格.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com