
【题目】下列描述中正确的是
A. CS2为V形的极性分子
B. ClO3—的空间构型为平面三角形
C. SF6中有6对相同的成键电子对
D. SiF4和SO32—的中心原子均为sp2杂化
科目:高中化学 来源: 题型:
【题目】常温下将NaOH溶液添加到己二酸(H2X)溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述错误的是

A. Ka2(H2X)的数量级为10-6
B. 曲线N表示pH与 的变化关系
的变化关系
C. NaHX溶液中c(H+)>c(OH-)
D. 当混合溶液呈中性时,c(Na+)>c(HX-)>c(X2-)>c(H+)=c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳元素形成的有机化合物在动植物体内及人类生存环境中有着相当广泛的存在,起着非常重要的作用。请结合下列有关含碳化合物的研究,完成下列填空。
(1)为了高效利用能源并且减少CO2的排放,可用下列方法把CO2转化成甲醇燃料:
①CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H=akJmol1
②2H2(g)+O2(g)=2H2O(g) △H=bkJmol1
③CH3OH(g)=CH3OH(l) △H=ckJmol1
④H2O(g)=H2O(l) △H=dkJmol1
则表示CH3OH(l)燃烧热的热化学方程式为___。
(2)用甲醇燃料电池电解处理酸性含铬废水(主要含有Cr2O72),用如图装置模拟该过程:
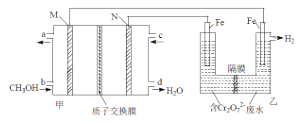
①请完成电解池中Cr2O72转化为Cr3+的离子方程式___。
②当甲池中消耗甲醇1.6g时,乙池中两电极的质量差为___g。
(3)葡萄糖和果糖为同分异构体,在一定条件下,C6H12O6(葡萄糖)![]() C6H12O6(果糖) △H﹤0。该反应的速率方程式可表示为v(正)=k(正)c(葡)、v(逆)=k(逆)c(果),k(正)和k(逆)在一定温度下为常数,分别称作正、逆反应速率常数。T1温度下,k(正)=0.06s1,k(逆)=0.002s1。
C6H12O6(果糖) △H﹤0。该反应的速率方程式可表示为v(正)=k(正)c(葡)、v(逆)=k(逆)c(果),k(正)和k(逆)在一定温度下为常数,分别称作正、逆反应速率常数。T1温度下,k(正)=0.06s1,k(逆)=0.002s1。
①T1温度下,该反应的平衡常数K1=___。
②该反应的活化能Ea(正)___Ea(逆)(填“大于”、“小于”或“等于”)。
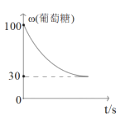
③该T2温度下,从开始反应到平衡的过程中,葡糖糖的质量分数变化如图所示。可以确定温度T2___T1(填“大于”、“小于”或“等于”)。
(4)H2A为二元弱酸。室温下配制一系列c(H2A)+c(HA)+c(A2)=0.100molL1的H2A与NaOH的混合溶液。测得H2A、HA、A2的物质的量分数c(x)%(c(x)%=![]() ×100%)随pH变化如图所示。
×100%)随pH变化如图所示。
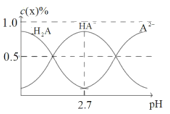
①当c(Na+)=0.100molL1时,溶液中离子浓度的大小顺序为___。
②室温下,若将0.100molL1的H2A与amolL1的NaOH溶液等体积混合,使溶液的pH=7。则H2A的Ka2=___molL1(用a表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列几组物质:
① | ② | ③ | ④ |
12C、14C | CH3CH3、CH3CH2CH3 | CH3CH2CH3、 |
|
(1)互为同系物的是________(填序号,下同)。
(2)互为同分异构体的是______。
(3)互为同位素的是_______。
(4)属于同一种物质的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼氢化钠(NaBH4)在有机合成中被称为“万能还原剂”,它的特点是性能稳定,还原时有选择性。采用NaBO2、SiO2、Na、H2为原料制备NaBH4的流程如图所示。
已知:NaBH4常温下能与水反应,可溶于异丙胺(沸点:33 ℃)。
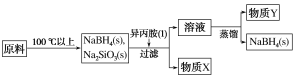
(1)NaBH4中含有的化学键类型为____________________。
(2)制取NaBH4的化学方程式为_________________________________________________;
在该反应加料之前,需要将反应容器加热至100 ℃以上并通入氩气,通入氩气的目的是__ 。
(3)在强碱性条件下,常用NaBH4处理含Au3+的废液生成单质Au,已知,反应后硼元素以BO2形式存在,反应前后硼元素化合价不变,且无气体生成,则发生反应的离子方程式为_______ 。
(4)物质X的化学式为__________;以上流程中可以循环使用的物质是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用还原沉淀法处理含铬废水(Cr2O72—和CrO42—),其流程为:
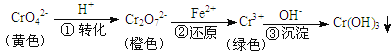
已知:步骤③生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s)![]() Cr3+(aq)+3OH—(aq) Ksp=c(Cr3+)·c3(OH—)=10-32
Cr3+(aq)+3OH—(aq) Ksp=c(Cr3+)·c3(OH—)=10-32
下列有关说法不正确的是
A.步骤①中当v正(CrO42—)=2v逆(Cr2O72—)时,说明反应:2CrO42—+2H+![]() Cr2O72—+H2O达到平衡状态
Cr2O72—+H2O达到平衡状态
B.若向K2Cr2O7溶液中加NaOH浓溶液,溶液可由橙色变黄色
C.步骤②中,若要还原1 mol Cr2O72—离子,需要12 mol (NH4)2Fe(SO4)2
D.步骤③中,当将溶液的pH调节至5时,可认为废水中的铬元素已基本除尽(当溶液中c(Cr3+)≤10-5mol/L时,可视作该离子沉淀完全)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PHB树脂可用于制作外科手术缝合线,有机物K是一种抗惊厥药物,它们的合成路线如图:
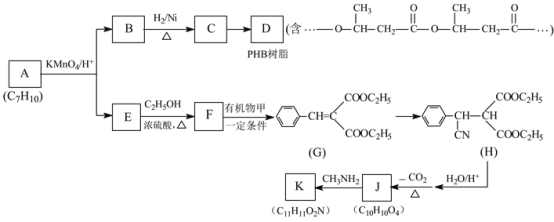
已知:
①RCN![]() RCOOH
RCOOH
②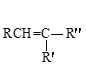
![]() RCOOH+
RCOOH+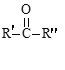
③RCHO+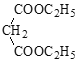
![]()
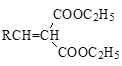 + H2O
+ H2O
R、R′、R″代表烃基
(1)有机物甲的结构简式为____________。
(2)写出一定条件下C→D的化学方程式:____________。
(3)写出E→F的化学方程式:__________________。
(4)A的结构简式为______________。
(5)已知1 mol J最多与2 mol NaHCO3反应;K分子结构中含有一个五元环与一个六元环。写出一定条件下J→K的化学方程式:____________。
(6)S是A的一种同分异构体,分子中没有环状结构,S的核磁共振氢谱有三个峰,峰面积之比为6:3:1,则S的结构简式为___________(写出一种即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物其结构简式如图,关于该有机物,下列叙述不正确的是( )
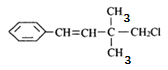
A.该有机物有三种官能团
B.1mol该有机物能与H2发生反应,消耗H2物质的量为4mol
C.一定条件下,能发生加聚反应
D.该有机物苯环上的一个H被取代,有3种同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是:
A. 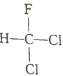 和
和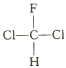 互为同分异构体
互为同分异构体
B. 15g甲基(﹣CH3)含有的电子数是9NA
C. 7.8g苯中含有的碳碳双键数为0.3NA
D. 标准状况下,2.24 L CCl4中的原子总数为0.5NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com