
分析 碳酸钙、碳酸镁是弱酸盐,能和酸反应不能和碱反应;氢氧化铝是两性氢氧化物,能和强酸、强碱反应;氢氧化镁属于碱,不能和碱反应,据此分析解答.
解答 解:碳酸钙、碳酸镁是弱酸盐,能和酸反应不能和碱反应;氢氧化镁属于碱,不能和碱反应,氢氧化铝是两性氢氧化物,能和强酸、强碱反应生成盐和水,
氢氧化铝和盐酸、氢氧化钠反应方程式分别为Al(OH)3+3HCl═AlCl3+3H2O、Al(OH)3+NaOH═NaAlO2+2H2O,
故答案为:Al(OH)3+3HCl═AlCl3+3H2O;Al(OH)3+NaOH═NaAlO2+2H2O.
点评 本题以药物成分为载体考查两性氢氧化物,明确元素化合物性质是解本题关键,氢氧化铝是高中阶段典型的类型氢氧化物,能溶于强碱但不溶于氨水等弱碱,题目难度不大.


科目:高中化学 来源: 题型:解答题
| 阳离子 | K+、Na+、Al3+、Cu2+ |
| 阴离子 | OH-、HCO3-、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用澄清石灰水来区分二氧化碳和二氧化硫 | |
| B. | 用米汤检验食用加碘盐(含KIO3)中含有碘元素 | |
| C. | 能使灼热的CuO由黑变红的气体一定是H2 | |
| D. | 可用石蕊试液来鉴别盐酸和NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
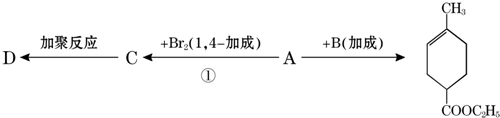
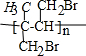 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(NO3)2+H2SO4═BaSO4↓+2HNO3 | B. | BaCl2+Na2SO4═BaSO4↓+2NaCl | ||
| C. | Ba(OH)2+K2SO4═BaSO4↓+2KOH | D. | Ba(OH)2+H2SO4═BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
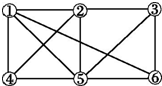
| A. | a 或b | B. | c | C. | d 或e | D. | f |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ,写出B的化学式:Fe3O4,写出C的化学式:Al2O3,主要成分是J的矿石的名称:赤铁矿.
,写出B的化学式:Fe3O4,写出C的化学式:Al2O3,主要成分是J的矿石的名称:赤铁矿.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
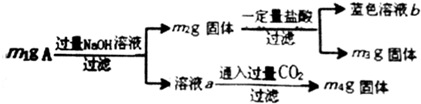
| A. | 由m1、m2、m4可计算出混合物中Al、Al2O3的物质的量 | |
| B. | 生成蓝色溶液的离子方程式为Cu+2Fe3+=Cu2++2Fe2+ | |
| C. | 蓝色溶液中一定有Cu2+、Fe2+、Fe3+ | |
| D. | 当m2-m3=2.96g时,Fe3O4的质量至少为2.32g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com