
ŹµŃéŹŅÖŠ,ŅŌĻĀĪļÖŹµÄÖü“ę”¢“¦Ąķ·½·Ø£¬²»ÕżČ·µÄŹĒ£Ø £©
A£®ÉŁĮæÄʱ£“ęŌŚĆŗÓĶÖŠ
B£®ĒāŃõ»ÆÄĘČÜŅŗÖü“ęŌŚ“ųĻš½ŗČūµÄ²£Į§ŹŌ¼ĮĘæÖŠ
C£®ÅØĻõĖįÓĆ“ųĻš½ŗČūµÄĻøæŚ”¢×ŲÉ«ŹŌ¼ĮĘæŹ¢·Å£¬²¢Öü“ęŌŚŅõĮ¹“¦
D£®ŅŗäåŅ×»Ó·¢£¬ŌŚ“ę·ÅŅŗäåµÄŹŌ¼ĮĘæÖŠÓ¦¼ÓĖ®·ā

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğŗžÄĻŹ”ø߶žÉĻѧʌʌ֊£ØĄķ£©»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŹµŃéĢā
ĄūÓĆĻĀĶ¼×°ÖĆ²ā¶ØÖŠŗĶČȵďµŃé²½ÖčČēĻĀ£ŗ

¢ŁÓĆĮæĶ²ĮæČ”50 mL 0.25 mol/LĮņĖįµ¹ČėŠ”ÉÕ±ÖŠ£¬²ā³öĮņĖįĪĀ¶Č£»
¢ŚÓĆĮķŅ»ĮæĶ²ĮæČ”50 mL 0.55 mol/L NaOHČÜŅŗ£¬²¢ÓĆĮķŅ»ĪĀ¶Č¼Ę²ā³öĘäĪĀ¶Č£»
¢Ū½«NaOHČÜŅŗµ¹ČėŠ”ÉÕ±ÖŠ£¬Éč·ØŹ¹Ö®»ģŗĻ¾łŌČ£¬²ā³ö»ģŗĻŅŗ×īøßĪĀ¶Č”£»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Š“³öĻ”ĮņĖįŗĶĻ”ĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦±ķŹ¾ÖŠŗĶČȵÄČČ»Æѧ·½³ĢŹ½(ÖŠŗĶČČŹżÖµĪŖ57.3 kJ/mol)£ŗ_________ __________________”£
£Ø2£©µ¹ČėNaOHČÜŅŗµÄÕżČ·²Ł×÷ŹĒ£ŗ____________”£ (“ÓĻĀĮŠŃ”ĻīÖŠŃ”³ö)”£
A£®ŃŲ²£Į§°ō»ŗĀżµ¹Čė B£®·ÖČż“ĪÉŁĮæµ¹Čė C£®Ņ»“ĪŃøĖŁµ¹Čė
£Ø3£©ŹµŃ鏿¾ŻČēĻĀ±ķ£ŗ
¢ŁĒėĢīŠ“ĻĀ±ķÖŠµÄæÕ°×£ŗ
ĪĀ¶Č ŹµŃé“ĪŹż | ĘšŹ¼ĪĀ¶Čt1”ę | ÖÕÖ¹ĪĀ¶Čt2/”ę | ĪĀ¶Č²īĘ½¾łÖµ (t2£t1) /”ę | ||
H2SO4 | NaOH | Ę½¾łÖµ | |||
1 | 26.2 | 26.0 | 26.1 | 29.5 | |
2 | 27.0 | 27.4 | 27.2 | 32.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.2 | |
4 | 26.4 | 26.2 | 26.3 | 29.8 | |
¢Ś½üĖĘČĻĪŖ0.55 mol/L NaOHČÜŅŗŗĶ0.25 mol/LĮņĖįČÜŅŗµÄĆܶȶ¼ŹĒ1 g/cm3£¬ÖŠŗĶŗóÉś³ÉČÜŅŗµÄ±ČČČČŻc£½4.18 J/(g”¤”ę)”£ŌņÖŠŗĶČȦ¤H £½__________ ( Č”Š”ŹżµćŗóŅ»Ī»)”£
¢ŪÉĻŹöŹµŃ鏿ֵ½į¹ūÓė57.3 kJ/molÓŠĘ«²ī£¬²śÉśĘ«²īµÄŌŅņæÉÄÜŹĒ(Ģī×ÖÄø)___________”£
a£®ŹµŃé×°ÖƱ£ĪĀ”¢øōČČŠ§¹ū²ī
b£®ÓĆĪĀ¶Č¼Ę²ā¶ØNaOHČÜŅŗĘšŹ¼ĪĀ¶ČŗóÖ±½Ó²ā¶ØH2SO4ČÜŅŗµÄĪĀ¶Č
c£®·Ö¶ą“Ī°ŃNaOHČÜŅŗµ¹ČėŹ¢ÓŠĮņĖįµÄŠ”ÉÕ±ÖŠ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ½Ī÷Ź”øßŅ»ÉĻѧʌ10ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ŌŚ±ź×¼×“æöĻĀ4.48L CH4ŗĶCO2»ģŗĻĘųĢåµÄÖŹĮæĪŖ6.0g£¬Ōņ»ģŗĻĘųĢåĘ½¾łÄ¦¶ūÖŹĮæĪŖ g/mol£¬Ļą¶ŌÓŚĒāĘųµÄĆܶČĪŖ £»CH4ŗĶCO2µÄÖŹĮæ±ČĪŖ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģɽ¶«Ź”øßČżÉĻѧʌʌ֊²āŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
³£ĪĀĻĀÓŠÅØ¶Č¾łĪŖ0.5 mol/LµÄĖÄÖÖČÜŅŗ£ŗ
¢ŁNa2CO3ČÜŅŗ ¢ŚNaHCO3ČÜŅŗ ¢ŪHClČÜŅŗ ¢Ü°±Ė®
£Ø1£©ÉĻŹöČÜŅŗÖŠ£¬æÉ·¢ÉśĖ®½āµÄŹĒ_______ _(ĢīŠņŗÅ£¬ĻĀĶ¬)”£
£Ø2£©ÉĻŹöČÜŅŗÖŠ£¬¼ČÄÜÓėĒāŃõ»ÆÄĘ·“Ó¦£¬ÓÖÄÜŗĶĮņĖį·“Ó¦µÄČÜŅŗÖŠĄė×ÓÅضČÓɓ󵽊”µÄĖ³ŠņĪŖ_________________________”£
£Ø3£© Ļņ¢ÜÖŠ¼ÓČėÉŁĮæĀČ»Æļ§¹ĢĢ壬“ĖŹ±c(NH4+)/c(OH£)µÄÖµ________(Ģī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±)”£
£Ø4£© Čō½«¢ŪŗĶ¢ÜµÄČÜŅŗ»ģŗĻŗóČÜŅŗĒ”ŗĆ³ŹÖŠŠŌ£¬Ōņ»ģŗĻĒ°¢ŪµÄĢå»ż________¢ÜµÄĢå»ż(Ģī”°“óÓŚ”±”¢”°Š”ÓŚ”±»ņ”°µČÓŚ”±)£¬“ĖŹ±ČÜŅŗÖŠĄė×ÓÅضČÓɓ󵽊”µÄĖ³ŠņŹĒ________________”£
£Ø5£© Č”10 mLČÜŅŗ¢Ū£¬Č»ŗó¼ÓĖ®Ļ”ŹĶµ½500 mL£¬Ōņ“ĖŹ±ČÜŅŗÖŠÓÉĖ®µēĄė³öµÄc(H£«)£½________ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģŗŚĮś½“óĒģŹµŃé֊ѧøßČżÉĻŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ä唢µā¼°Ęä»ÆŗĻĪļŌŚ¹¤Å©ŅµÉś²śŗĶČÕ³£Éś»īÖŠÓŠÖŲŅŖÓĆĶ¾”£
¢ń£®ĒāäåĖįŌŚŅ½Ņ©ŗĶŹÆ»Æ¹¤ŅµÉĻÓŠ¹ć·ŗÓĆĶ¾£¬ĻĀĶ¼ŹĒÄ£Äā¹¤ŅµÖʱøĒāäåĖįµÄĮ÷³Ģ£ŗ
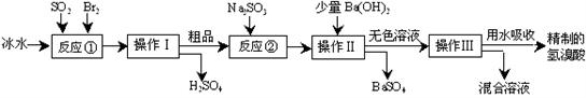
øł¾ŻÉĻŹöĮ÷³Ģ»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©·“Ó¦¢ŁÖŠ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ £»Ź¹ÓƱłĖ®µÄÄæµÄŹĒ
£Ø2£©²Ł×÷¢ńµÄĆū³ĘŹĒ £»²Ł×÷¢ņµÄĆū³ĘŹĒ £»
£Ø3£©·“Ó¦¢ŚÖŠ¼ÓČėNa2SO3µÄÄæµÄŹĒ £»µ«ŅŖ·ĄÖ¹¹żĮ棬ŌŅņŹĒ £ØÓĆĄė×Ó·½³ĢŹ½±ķŹ¾£©
¢ņ£®Ā±ĖŲ»„»ÆĪļŹĒÖø²»Ķ¬Ā±ĖŲŌ×ÓÖ®¼äŅŌ¹²¼Ū¼ü½įŗĻŠĪ³ÉµÄ»ÆŗĻĪļ”£XX”äŠĶĀ±ĖŲ»„»ÆĪļÓėĀ±ĖŲµ„ÖŹ½į¹¹ĻąĖĘ”¢ŠŌÖŹĻą½ü, ÄÜÓė“󶹏ż½šŹō·“Ӧɜ³É½šŹōĀ±»ÆĪļ£¬ÄÜÓėŠķ¶ą·Ē½šŹōµ„ÖŹ·“Ӧɜ³ÉĻąÓ¦Ā±»ÆĪļ£¬ÄÜÓėĖ®·“Ó¦µČ”£ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø4£©äå»Æµā£ØIBr£©ÓėĖ®·“Ó¦µÄ·½³ĢŹ½ĪŖIBr +H2O£½HBr+HIOĻĀĮŠ¹ŲÓŚIBrµÄŠšŹöÖŠ²»ÕżČ·µÄŹĒ
A£®IBrÖŠäåŗĶµāµÄ»ÆŗĻ¼Ū¾łĪŖ0¼Ū B£®ŌŚŠķ¶ą·“Ó¦ÖŠIBrŹĒĒæŃõ»Æ¼Į
C£®ŌŚIBrÓėĖ®µÄ·“Ó¦ÖŠ£¬Ėü¼ČŹĒŃõ»Æ¼ĮÓÖŹĒ»¹Ō¼Į D£®ÓėNaOHČÜŅŗ·“Ӧɜ³ÉNaIO”¢NaBrŗĶH2O
£Ø5£© ŌŚ“ÖµāÖŠŗ¬ÓŠIBrŗĶICl£¬ŹÜČČŹ±£¬I2”¢ICl”¢IBr¾łæÉÉż»Ŗ”£ŌŚ“ÖµāÖŠ¼ÓČėŅ»ÖÖĪļÖŹŗó£¬ŌŁ½ųŠŠÉż»Ŗ£¬æÉÖĘµĆ¾«µā£¬Ó¦¼ÓČėµÄĪļÖŹŹĒ
A£®H2O B£®KI C£®Zn D£®KCl
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ¼ŖĮÖŹµŃé֊ѧø߶žÉĻŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
øßĀČĖį”¢ĮņĖį”¢ĻõĖįŗĶŃĪĖį¶¼ŹĒĒæĖį£¬ĘäĖįŠŌŌŚĖ®ČÜŅŗÖŠĻą²ī²»“ó”£ŅŌĻĀŹĒijĪĀ¶ČĻĀÕāĖÄÖÖĖįŌŚ±ł“×ĖįÖŠµÄµēĄė³£Źż£ŗ
Ėį | HClO4 | H2SO4 | HCl | HNO3 |
KA | 1.6”Į10£5 | 6.3”Į10£9 | 1.6”Į10£9 | 4.2”Į10£10 |
øł¾ŻÉĻŹö±ķøńÖŠµÄŹż¾Ż£¬ÅŠ¶ĻŅŌĻĀĖµ·ØÖŠ²»ÕżČ·µÄŹĒ£Ø £©
A£®ŌŚ±ł“×ĖįÖŠÕāĖÄÖÖĖį¶¼Ć»ÓŠĶźČ«µēĄė
B£®ŌŚ±ł“×ĖįÖŠøßĀČĖįŹĒÕāĖÄÖÖĖįÖŠĖįŠŌ×īĒæµÄĖį
C£®ŌŚ±ł“×ĖįÖŠĮņĖįµÄµēĄė·½³ĢŹ½æɱķŹ¾ĪŖH2SO4===2H£«£«SO42£
D£®Ė®¶ŌÓŚÕāĖÄÖÖĖįµÄĒæČõƻӊĒų·ÖÄÜĮ¦£¬µ«±ł“×ĖįæÉŅŌĒų·ÖÕāĖÄÖÖĖįµÄĒæČõ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ¹ć¶«ÉĒĶ·½šÉ½ÖŠŃ§øßŅ»10ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠŹµŃ黳±¾²Ł×÷¼°×¢ŅāŹĀĻīÖŠ£¬Ö÷ŅŖ³öÓŚ°²Č«æ¼ĀĒµÄŹĒ
A£®ŹµŃéŹ£ÓąµÄŅ©Ę·²»ÄÜ·Å»ŲŌŹŌ¼ĮĘæ
B£®¾Ę¾«µĘÄŚ¾Ę¾«²»ÄܶąÓŚ¾Ę¾«µĘČŻ»żµÄ2/3
C£®ŹµŃé½įŹųŗó½«ŹŌ¹ÜĒåĻ“øɾ»
D£®½ŗĶ·µĪ¹Ü²»Äܽ»²ęŹ¹ÓĆ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ŗÓ±±ŹÆ¼Ņ×ƵŚŅ»ÖŠŃ§ø߶žÉĻĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
¶ŌÓŚ±½ŅŅĻ©µÄĻĀĮŠŠšŹöÖŠ£¬ÕżČ·µÄŹĒ
¢ŁÄÜŹ¹ĖįŠŌKMnO4ČÜŅŗĶŹÉ«
¢ŚæÉ·¢Éś¼Ó³É·“Ó¦
¢ŪæÉČÜÓŚĖ®
¢ÜæÉČÜÓŚ±½ÖŠ
¢ŻÄÜÓėÅØĻõĖįŌŚÅØH2SO4×÷ÓĆĻĀ·¢ÉśČ”“ś·“Ó¦
¢ŽĖłÓŠµÄŌ×ÓæÉÄܹ²Ę½Ćę”£
A£®¢Ł¢Ś¢Ū¢Ü¢Ż B£®¢Ł¢Ś¢Ż¢Ž
C£®¢Ł¢Ś¢Ü¢Ż¢Ž D£®Č«²æ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģŗŚĮś½Ź”øßČżµŚČż“ĪŌĀæ¼Ąķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
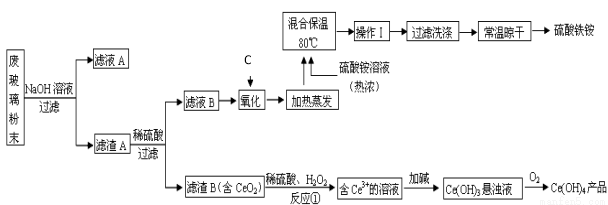
Ę½°åµēŹÓĻŌŹ¾ĘĮÉś²ś¹ż³ĢÖŠ²śÉś“óĮæµÄ·Ļ²£Į§·ŪÄ©£Øŗ¬SiO2”¢Fe2O3”¢CeO2”¢FeOµČĪļÖŹ£©”£Ä³æĪĢāŅŌ“Ė·ŪÄ©ĪŖŌĮĻ£¬Éč¼ĘČēĻĀ¹¤ŅÕĮ÷³Ģ¶Ō׏Ō“½ųŠŠ»ŲŹÕ£¬µĆµ½Ce(OH)4ŗĶĮņĖįĢśļ§¾§Ģå£ŗ
¢”£®ĖįŠŌĢõ¼žĻĀ£¬īęŌŚĖ®ČÜŅŗÖŠÓŠ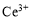 ”¢
”¢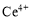 Į½ÖÖÖ÷ŅŖ“ęŌŚŠĪŹ½£¬
Į½ÖÖÖ÷ŅŖ“ęŌŚŠĪŹ½£¬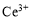 Ņ×Ė®½ā£¬
Ņ×Ė®½ā£¬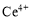 ÓŠ½ĻĒæŃõ»ÆŠŌ”£
ÓŠ½ĻĒæŃõ»ÆŠŌ”£
¢¢£®CeO2²»ČÜÓŚĻ”ĮņĖį
¢££®ĮņĖįĢśļ§¾§Ģå¹ć·ŗÓĆÓŚĖ®µÄ¾»»Æ“¦Ąķ”£
£Ø1£©ŌŚŃõ»Æ»·½Ś£¬ĻĀĮŠĪļÖŹÖŠ×īŹŹŗĻÓĆ×÷Ńõ»Æ¼ĮCµÄŹĒ ”£
A£®NaClO B£®H2O2 C£®KMnO4 D£®ÅØĮņĖį
£Ø2£©²Ł×÷¢ńµÄĆū³ĘŹĒ £¬¼ģŃéĮņĖįĢśļ§ČÜŅŗÖŠŗ¬ÓŠNH4+µÄ·½·ØŹĒ£ŗ ”£
£Ø3£©·“Ó¦¢ŁÖ®Ē°ĻČŅŖĻ“µÓĀĖŌüB£¬ĘäÄæµÄŹĒĪŖĮĖ³żČ„ £ØĢīĄė×Ó·ūŗÅ£©£»·“Ó¦¢ŁµÄĄė×Ó·½³ĢŹ½ĪŖ ”£
£Ø4£©ÓƵĪ¶Ø·Ø²ā¶ØÖʵƵÄCe(OH)4²śĘ·“æ¶Č£ŗ

µĪ¶ØŹ±ĖłÓƶØĮæŅĒĘ÷µÄ×īŠ”æĢ¶ČĪŖ £»ĖłÓĆFeSO4ČÜŅŗŌŚæÕĘųÖŠĀ¶ÖĆŅ»¶ĪŹ±¼äŗóŌŁ½ų½ųŠŠµĪ¶Ø£¬Ōņ²āµĆøĆCe(OH)4²śĘ·µÄÖŹĮæ·ÖŹż ”££ØĢī”°Ę«“ó”±”¢”°Ę«Š””±»ņ”°ĪŽÓ°Ļģ”±£©
£Ø5£©³ĘČ”14.00gĮņĖįĢśļ§ŃłĘ·£¬½«ĘäČÜÓŚĖ®ÅäÖĘ³É100mLČÜ Ņŗ£¬·Ö³ÉĮ½µČ·Ż£¬ĻņĘäÖŠŅ»·Ż¼ÓČė×ćĮæNaOHČÜŅŗ£¬¹żĀĖĻ“µÓ³Įµķ²¢ŗęøÉ×ĘÉÕÖĮŗćÖŲµĆµ½1.60g¹ĢĢ壻ĻņĮķŅ»·ŻČÜŅŗÖŠ¼ÓČė0.5mol/L Ba(NO3)2ČÜŅŗ100mL£¬Ē”ŗĆĶźČ«·“Ó¦”£ŌņøĆĮņĖįĢśļ§µÄ»ÆѧŹ½ĪŖ ”£
Ņŗ£¬·Ö³ÉĮ½µČ·Ż£¬ĻņĘäÖŠŅ»·Ż¼ÓČė×ćĮæNaOHČÜŅŗ£¬¹żĀĖĻ“µÓ³Įµķ²¢ŗęøÉ×ĘÉÕÖĮŗćÖŲµĆµ½1.60g¹ĢĢ壻ĻņĮķŅ»·ŻČÜŅŗÖŠ¼ÓČė0.5mol/L Ba(NO3)2ČÜŅŗ100mL£¬Ē”ŗĆĶźČ«·“Ó¦”£ŌņøĆĮņĖįĢśļ§µÄ»ÆѧŹ½ĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com