
”¾ĢāÄæ”æÉčNAĪŖ°¢·üŁ¤µĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø””””£©
A.78gNa2O2¹ĢĢåÖŠŗ¬ÓŠµÄŅõĄė×ÓŹżĪŖNA
B.±ź×¼×“æöĻĀ£¬2.24LÄŹĘųĖłŗ¬Ō×ÓŹżĪŖ0.2NA
C.1molCl2Óė×ćĮæFe·“Ó¦£¬×ŖŅʵĵē×ÓŹżĪŖ3NA
D.±ź×¼×“æöĻĀ£¬2.24LŅŃĶéŗ¬ÓŠĢ¼Ō×ӵďżÄæĪŖ0.6NA
”¾“š°ø”æA
”¾½āĪö”æA”¢ŅĄ¾Żn= ![]() ¼ĘĖćĪļÖŹµÄĮæ=
¼ĘĖćĪļÖŹµÄĮæ= ![]() =1mol£¬½įŗĻ¹żŃõ»ÆÄĘŹĒÄĘĄė×ÓŗĶ¹żŃõøłĄė×Ó¹¹³É£¬ŗ¬ÓŠµÄŅõĄė×ÓŹżĪŖNA£¬¹ŹA·ūŗĻĢāŅā£»
=1mol£¬½įŗĻ¹żŃõ»ÆÄĘŹĒÄĘĄė×ÓŗĶ¹żŃõøłĄė×Ó¹¹³É£¬ŗ¬ÓŠµÄŅõĄė×ÓŹżĪŖNA£¬¹ŹA·ūŗĻĢāŅā£»
B”¢ŅĄ¾Żn= ![]() ¼ĘĖćĪļÖŹµÄĮæ=
¼ĘĖćĪļÖŹµÄĮæ= ![]() =0.1mol£¬½įŗĻÄŹĘųŹĒµ„Ō×Ó·Ö×Ó£¬Ėłŗ¬Ō×ÓŹżĪŖ0.1NA£¬¹ŹB²»·ūŗĻĢāŅā£»
=0.1mol£¬½įŗĻÄŹĘųŹĒµ„Ō×Ó·Ö×Ó£¬Ėłŗ¬Ō×ÓŹżĪŖ0.1NA£¬¹ŹB²»·ūŗĻĢāŅā£»
C”¢ĀČĘųŗĶĢś·“Ӧɜ³ÉĀČ»ÆĢś£¬µē×Ó×ŖŅĘŅĄ¾Ż·“Ó¦µÄĀČĘų¼ĘĖć£¬×ŖŅʵĵē×ÓŹżĪŖ2NA£¬¹ŹC²»·ūŗĻĢāŅā£»
D”¢±ź×¼×“æö¼ŗĶé²»ŹĒĘųĢ壬2.24LŅŃĶé²»ŹĒ0.1mol£¬¹ŹD²»·ūŗĻĢāŅā£»
ĖłŅŌ“š°øŹĒ£ŗA£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŹżĮæµÄĪļÖŹÖŠŗ¬Ō×ÓøöŹż×ī¶ąµÄŹĒ£ŗ
A”¢0.4mol ŃõĘų B”¢4”ꏱ£¬5.4mLH2O
C”¢±źæöĻĀ5.6L ¶žŃõ»ÆĢ¼ D”¢10 g ÄŹ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijÖÖ”°¹āĆōŠŌøß·Ö×Ó”±²ÄĮĻŌŚÓ«¹āĘĮ¼°“ó¹ęÄ£¼Æ³ÉµēĀ·ÖŠÓ¦ÓĆ¹ć·ŗ£®Ęä½į¹¹æɱķŹ¾ĪŖ£ŗ¶ŌøĆ”°¹āĆōŠŌøß·Ö×Ó”±ŠšŹöÕżČ·µÄŹĒ£Ø £©”¾©COO©»łĶÅÓėĒāĘų²»·“Ó¦”æ 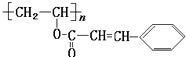
A.»ÆѧŹ½ĪŖ£ØC11H11O2£©n
B.ĖüÄÜ·¢Éś»¹Ō·“Ó¦
C.ĖüæÉŅŌŗĶFeCl3ČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦
D.1moløĆ·Ö×Ó×ī¶ąÄÜŗĶ4molH2·¢Éś¼Ó³É·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”ææĘѧ¼ŅĢį³ö¹čŹĒ”°21ŹĄ¼ĶµÄÄÜŌ“”±£¬ÕāÖ÷ŅŖŹĒÓÉÓŚ×÷ĪŖ°ėµ¼Ģå²ÄĮĻµÄ¹čŌŚĢ«ŃōÄÜ·¢µē¹ż³ĢÖŠ¾ßÓŠÖŲŅŖµÄ×÷ÓĆ”£ĻĀĮŠ¹ŲÓŚ¹čµÄĖµ·ØÖŠÕżČ·µÄŹĒ£Ø £©
A.¹čŌŚ»Æѧ·“Ó¦ÖŠŅ׵Ƶ½µē×ÓB.×ŌČ»½ēÖŠ“ęŌŚ“óĮæµ„ÖŹ¹č
C.øß“æ¶ČµÄ¹č±»ÓĆÓŚÖĘ×÷¼ĘĖ滜Š¾Ę¬D.¹āµ¼ĻĖĪ¬µÄÖ÷ŅŖ³É·ÖŹĒSi
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠø÷×éĪļÖŹµÄ¾§ĢåÖŠ£¬»Æѧ¼üĄąŠĶĻąĶ¬”¢¾§ĢåĄąŠĶŅ²ĻąĶ¬µÄŹĒ£Ø £©
A.SO2ŗĶSiO2B.NaClŗĶHClC.CCl4ŗĶKClD.CO2ŗĶH2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹŹōÓŚ“æ¾»ĪļµÄŹĒ£Ø £©
A.ŹÆÓĶ
B.ÉśŹÆ»Ņ
C.ĀĮČČ¼Į
D.ĘÆ·Ū¾«
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø1£©Š“³öĢśÓėĖ®ÕōĘųŌŚøßĪĀĻĀ·“Ó¦·½³ĢŹ½___________________________”£
£Ø2£©³£ĪĀĻĀ£¬ĶŌŚ³±ŹŖµÄæÕĘųĄļ»į±»ŠāŹ“£¬ÓŠ¹Ų»Æѧ·½³ĢŹ½ĪŖ___________________________________”£
£Ø3£©ŌŚŗōĪüĆę¾ßÖŠ£¬Na2O2 Ęš·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ____________________________________”£µ±ÓŠ7.8æĖNa2O2·“Ó¦Ź±£¬·Å³öŃõĘųµÄÖŹĮæĪŖ____________”£
£Ø4£©½«6.4gµÄĶʬĶ¶Čėµ½100mlµÄFeCl3ČÜŅŗÖŠĒ”ŗĆĶźČ«·“Ó¦£¬·¢ÉśµÄ·“Ó¦Ąė×Ó·½³ĢŹ½ĪŖ______________________________________£¬ FeCl3ČÜŅŗµÄĪļÖŹµÄĮæÅضČ______________”£
£Ø5£©ĻņFeSO4ČÜŅŗÖŠµĪ¼ÓNaOHČÜŅŗŹ±£¬Éś³ÉµÄ°×É«Šõד³ĮµķŃøĖŁ±ä³É»ŅĀĢÉ«£¬×īŗó±ä³ÉŗģŗÖÉ«”£Š“³ö“Ė±ä»Æ¹ż³ĢµÄ»Æѧ·½³ĢŹ½£ŗ_________________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æSO2±»³ĘĪŖ”°æÕÖŠĖĄÉń”±£¬Ęä¶Ō»·¾³µÄĪ£ŗ¦³£±ķĻÖĪŖ__________________”£ĪŖĮĖ¼õÉŁĪ£ŗ¦£¬ČĖĆĒ½ųŠŠĮĖŠķ¶ąÓŠŅęµÄĢ½Ė÷ŗĶŃŠ¾æ£¬²¢ĒŅŌŚŹµ¼ŹÓ¦ÓĆÉĻČ”µĆĮĖŅ»¶ØµÄ³É¹ū”£
£Ø1£©¹¤ŅµÉĻ³£ÓĆÉśŹÆ»ŅĄ““¦ĄķĆŗĢæÖŠµÄSO2£¬ÕāŹĒĄūÓĆĮĖSO2ŹōÓŚ__________Ńõ»ÆĪļµÄŠŌÖŹ”£
£Ø2£©½üÄźĄ“£¬ÓŠČĖĢį³öĮĖŅ»ÖÖĄūÓƵē½ā±„ŗĶĀČ»ÆÄĘČÜŅŗ(2NaCl£«2H2O===2NaOH£«Cl2£«H2)Ń»·ÖĪĄķŗ¬¶žŃõ»ÆĮņµÄ·ĻĘų²¢»ŲŹÕ¶žŃõ»ÆĮņµÄ·½·Ø”£øĆ·½·ØµÄĮ÷³ĢČēĻĀ£ŗ
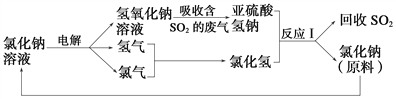
¢Ł“ĖÖÖ·½·ØÖŠ£¬æÉŅŌŃ»·ĄūÓƵÄĪļÖŹŹĒ______________________________”£
¢ŚŠ“³ö·“Ó¦¢ńµÄĄė×Ó·½³ĢŹ½£ŗ______________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æäå»ÆøĘŌŚŅ½Ņ©ÉĻÓĆ×÷ÖŠŹąÉń¾ŅÖÖĘŅ©£¬ŹµŃéŹŅÓĆ”°ÄņĖŲ·Ø”±Öʱøäå»ÆøʵÄÖ÷ŅŖĮ÷³ĢČēĻĀ£ŗ
äå»ÆøĘµÄ²æ·ÖČܽā¶ČŹżÖµČēĻĀ£ŗ
ĪĀ¶Č | 0”ę | 10”ę | 20”ę | 40”ę | 60”ę | 80”ę | 100”ę |
Čܽā¶Č£Øg£© | 125 | 132 | 143 | 213 | 278 | 295 | 312 |
£Ø1£©6Ca£ØOH£©2+6Br2 ![]() 5CaBr2+6H2O+Ca£ØBrO3£©2 £¬ ĆæÉś³É1mol Ca£ØBrO3£©2×ŖŅʵē×ÓµÄĪļÖŹµÄĮæĪŖ£»50”«70”ꏱ£¬ÄņĖŲ[CO£ØNH2£©2]½«Éś³ÉµÄCa£ØBrO3£©2»¹ŌĪŖCaBr2 £¬ ÄņĖŲ±»Ńõ»ÆĪŖN2 £¬ øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ £®
5CaBr2+6H2O+Ca£ØBrO3£©2 £¬ ĆæÉś³É1mol Ca£ØBrO3£©2×ŖŅʵē×ÓµÄĪļÖŹµÄĮæĪŖ£»50”«70”ꏱ£¬ÄņĖŲ[CO£ØNH2£©2]½«Éś³ÉµÄCa£ØBrO3£©2»¹ŌĪŖCaBr2 £¬ ÄņĖŲ±»Ńõ»ÆĪŖN2 £¬ øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ £®
£Ø2£©¹żĀĖĖłŠčµÄ²£Į§ŅĒĘ÷ÓŠ²£Į§°ō”¢”¢ £®
£Ø3£©¼ÓČėĒāäåĖįµ÷pHµÄ×÷ÓĆŹĒ £®
£Ø4£©²Ł×÷I°üĄØ”¢”¢¹żĀĖ”¢±łĖ®Ļ“µÓ”¢øÉŌļ£®
£Ø5£©”°¶žŃõ»ÆĮņ·Ø”±ÖʱøµÄĒāäåĖį“ÖĘ·ÖŠ³£ŗ¬ÓŠÉŁĮæµÄäåŗĶĮņĖį£»ĒėŃ”ÓĆĖłĢį¹©µÄŹŌ¼Į£¬ŹŌŠ“³ö¼ģŃéĒāäåĖį“ÖĘ·ÖŠŹĒ·ńŗ¬ÓŠSO42©µÄŹµŃé·½°ø£ŗ £®
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com