
| A、1:1 | B、10:1 |
| C、100:1 | D、1:10 |


科目:高中化学 来源: 题型:
| A、C2H4和C2H6 |
| B、C2H2和C3H8 |
| C、C2H6和C3H8 |
| D、C2H6和CH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、小于0.9mol |
| B、等于0.9mol |
| C、在0.9mol与1.8mol之间 |
| D、等于1.8mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
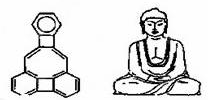
| A、该有机物所有原子一定在同一平面 |
| B、该有机物属于苯的同系物 |
| C、该有机物分子中含有21个碳原子 |
| D、该有机物一氯代物只有4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液中含有1molNaCl |
| B、1L溶液里含有NaCl58.5克 |
| C、58.5gNaCl溶于941.5g水中 |
| D、1molNaCl溶于1L水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
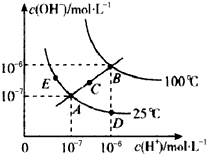
| A、从图中可以看出,水的电离是吸热过程 |
| B、若从A点到D点,可采用:温度不变在水中加入适量的NH4Cl固体 |
| C、在处于C点状态的溶液中:Na+、Al3+、CO32-、Cl-能够大量共存 |
| D、在处于E点状态的CH3COONa溶液中:c(Na+)>c(CH3COO-)>c(OH+)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在AgNO3溶液中依次滴加同浓度的NaCl、Na2S溶液,可证明KSP(AgCl)>KSP(Ag2S) |
| B、△S>0的反应在一定条件下不一定可以自发进行 |
| C、以Al作阳极,Fe作阴极,可以实现铁上镀铝 |
| D、工业合成SO3不采用高压是因为增大压强对SO2的转化率影响不大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com