
【题目】下列物质没有固定熔沸点的是
A.液氯B.干冰C.胆矾D.纯盐酸
科目:高中化学 来源: 题型:
【题目】两种气态烃的混和物共0.1mol,完全燃烧后得3.36L(标况下)CO2和3.6g水,下列说法正确的是( )
A. 一定有乙烯B. 一定有甲烷
C. 可能有乙烷D. 一定有乙烷,但不一定有甲烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于共价键的说法正确的是( )
A.丙炔分子中含有5个σ键和2个π键
B.乙醇分子中O-H键的极性强于C-H键的极性
C.乙烷分子中只含有极性键不含有非极性键
D.分子晶体中共价键键能越大,该分子晶体的熔点和沸点一定也越高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外实验小组设计的下列实验不合理的是( )
A. 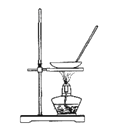 蒸干NH4Cl饱和溶液制备NH4Cl晶体
蒸干NH4Cl饱和溶液制备NH4Cl晶体
B. 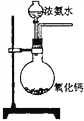 实验室制备少量氨气
实验室制备少量氨气
C. 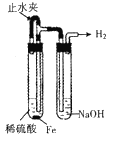 制备并观察氢氧化亚铁
制备并观察氢氧化亚铁
D. 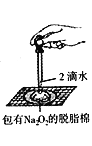 证明过氧化钠与水反应放热
证明过氧化钠与水反应放热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】滴定法是化学常用来定量测定物质浓度的一种重要的实验方法。在食品工业、药品制造、化妆品行业等等都被广泛应用。中华人民共和国国家标准(GB2760-2011)规定葡萄酒中SO2最大使用量为0.25 g·L-1。某兴趣小组用如图装置(夹持装置略)收集某葡萄酒中SO2,并对其含量进行测定。
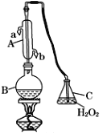
(1)仪器A的名称是________,水通入A的进口为________。B中加入300.00 mL葡萄酒和适量盐酸,加热B使SO2全部逸出并与C中H2O2完全反应。
(2)除去C中过量的H2O2,然后用0.090 0 mol·L-1NaOH标准溶液进行滴定,若滴定终点时溶液的pH=8.8,则选择的指示剂为________。滴定终点现象为_______________。
(3)滴定至终点时,消耗NaOH溶液25.00 mL,该葡萄酒中SO2含量为:________g·L-1。
(4)该测定结果往往比实际值偏高,最可能的原因是_________________,在不改变装置的情况下,如何改进:______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,可逆反应A(g)+3B(g) ![]() 2C(g)达到平衡的标志是
2C(g)达到平衡的标志是
A. C生成的速率与C分解的速率相等
B. 单位时间内生成n molA,同时消耗3nmol B
C. A、B、C的浓度相等
D. A、B、C的分子数之比为1∶3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列反应中,HNO3既表现出氧化性,又表现出酸性的是
A. 3Cu+8HNO3(稀) =3Cu(NO3)2+2NO↑+4H2O↑
B. CuO+2HNO3=Cu(NO3)2+H2O
C. 4HNO3(浓) ![]() 4NO2↑+O2↑+2H2O
4NO2↑+O2↑+2H2O
D. H2S+2HNO3(浓) ![]() S↓+2NO2+2H2O
S↓+2NO2+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某课外活动小组同学用如图装置进行实验,试回答下列问题:
①若开始时开关K与a连接,则铁发生电化学腐蚀中的________腐蚀。
②若开始时开关K与b连接,则总反应的离子方程式为____________________________。
(2)芒硝化学式为Na2SO4·10H2O,无色晶体,易溶于水,是一种分布很广泛的硫酸盐矿物。该小组同学设想,如果模拟工业上离子交换膜法制烧碱的方法,用如图所示装置电解硫酸钠溶液来制取氢气、氧气、硫酸和氢氧化钠,无论从节省能源还是从提高原料的利用率而言都更加符合绿色化学理念。
①该电解槽的阳极反应式为______________________________________。
此时通过阴离子交换膜的离子数________(填“大于”、“小于”或“等于”)通过阳离子交换膜的离子数
②制得的氢氧化钠溶液从出口(填写“A”、“B”、“C”或“D”)________导出。

③通电开始后,阴极附近溶液pH会增大,请简述原因:____________________________。
④若将制得的氢气、氧气和氢氧化钠溶液组合为氢氧燃料电池,则电池负极的电极反应式为______________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢能源是一种重要的清洁能源。现有两种可产生H2的化合物甲和乙。将6.00g甲加热至完全分解,只得到一种短周期元素的金属单质和6.72LH2(已折算成标准状况),甲与水反应也能产生H2,同时还产生一种白色沉淀物,该白色沉淀可溶于NaOH溶液。化合物乙在催化剂存在下可分解得到H2和另一种单质气体丙,丙在标准状态下的密度为1.25g/L。请回答下列问题:
(1)甲的化学式是__________;乙的电子式是__________。
(2)甲与水反应的化学方程式是__________。
(3)气体丙与金属镁反应的产物是__________(用化学式表示)。
(4)乙在加热条件下与CuO反应可生成Cu和气体丙,写出该反应的化学方程式__________。有人提出产物Cu中可能还含有Cu2O,请设计实验方案验证之__________(已知Cu2O+2H+=Cu+Cu2++H2O)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com