
现用18.4 mol·L-1的浓硫酸来配制500mL 0.2 mol·L-1的稀硫酸,可供选择的仪器有:①玻璃棒 ②烧杯 ③胶头滴管 ④量筒 ⑤托盘天平
(1)上述仪器在配制过程中不需要用到的是__________________。(填序号)除上述仪器外,尚缺最重要的仪器是 。
(2)计算所需浓硫酸的体积为___________m L(保留1位小数)。
(3)实验中用到玻璃棒,其作用分别是:___________、__________。
(4)配制时,一般可分为以下几个步骤:
①量取 ②计算 ③稀释 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却。其正确的操作顺序
为:②→①→③→____ →____→____→____→④(填序号)
(5)在配制过程中,下列操作可引起所配溶液浓度偏低的有____________(填序号)
①定容时,仰视刻度线。
②未冷却至室温就转移到容量瓶中。
③容量瓶中含有少量蒸馏水。
④未洗涤稀释浓硫酸时用过的烧杯和玻璃棒。
⑤定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线。
(共11分)(1)⑤(1分) 500mL容量瓶 (1分)(2)5.4mL(2分)
(3)搅拌 引流 (1+1分) (4)⑧→⑤→⑥→⑦(2分) (顺序有错不得分)(5)①④⑤(3分)
解析试题分析:(1)浓硫酸配置稀硫酸,因此不需要托盘天平,答案选⑤;根据所给的仪器可知,还缺少500mL容量瓶。
(2)稀释过程中,硫酸的物质的量是不变的,所以需要浓硫酸的体积是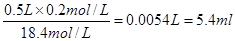
(3)稀释需要玻璃棒的搅拌,转移到容量瓶中需要玻璃棒的引流。
(4)正确的操作顺序应该是②→①→③→⑧→⑤→⑥→⑦→④。
(5)根据n=c·V可知,定容时,仰视刻度线,则溶液的体积增加,浓度偏低;未冷却至室温就转移到容量瓶中,则容量瓶中冷却后溶液体积减少,浓度偏高;容量瓶中含有少量蒸馏水,浓度不变;未洗涤稀释浓硫酸时用过的烧杯和玻璃棒,则溶质减少,浓度偏低;定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线,则溶液的体积增加,浓度偏低,答案选①④⑤。
考点:考查一定物质的量浓度溶液的配置、计算、仪器的选择以及误差分析
点评:该题是中等难度的试题,试题基础性强,侧重考查学生的实验能力,有助于培养学生的规范操作、实验动手能力,提高学生分析问题、解决问题的能力。该题的难点是误差分析,学生需要明确,根据cB=nB/V可得,一定物质的量浓度溶液配制的误差都是由溶质的物质的量nB和溶液的体积V引起的。误差分析时,关键要看配制过程中引起n和V怎样的变化。在配制一定物质的量浓度溶液时,若nB比理论值小,或V比理论值大时,都会使所配溶液浓度偏小;若nB比理论值大,或V比理论值小时,都会使所配溶液浓度偏大。


 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源: 题型:
(5分)现用18.4 mol·L-1的浓H2SO4来配制250 mL、0.300 mol·L-1的稀H2SO4。可供选择的仪器有: ①药匙 ②量筒 ③托盘天平 ④玻璃棒 ⑤烧瓶?
⑥胶头滴管 ⑦容量瓶 ⑧烧杯。 请回答下列问题:
(1)上述仪器中,在配制稀H2SO4时用不到的有 (填代号)。
(2)经计算,需浓H2SO4的体积为 。
现有① 5 mL ②10 mL ③20 mL 三种规格量筒,你选用的量筒是 (填代号)。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年福建省罗源县第一中学高一上学期期中联考化学试卷 题型:填空题
(5分)现用18.4 mol·L-1的浓H2SO4来配制250 mL、0.300 mol·L-1的稀H2SO4。可供选择的仪器有: ①药匙 ②量筒 ③托盘天平 ④玻璃棒 ⑤烧瓶?
⑥胶头滴管 ⑦容量瓶 ⑧烧杯。 请回答下列问题:
(1)上述仪器中,在配制稀H2SO4时用不到的有 (填代号)。
(2)经计算,需浓H2SO4的体积为 。
现有①5 mL ②10 mL ③20 mL 三种规格量筒,你选用的量筒是 (填代号)。
查看答案和解析>>
科目:高中化学 来源:2015届福建省、二中高一上学期期末联考化学试卷(解析版) 题型:实验题
现用18.4 mol·L-1的浓硫酸来配制500mL 0.2 mol·L-1的稀硫酸,可供选择的仪器有:①玻璃棒 ②烧杯 ③胶头滴管 ④量筒 ⑤托盘天平
(1)上述仪器在配制过程中不需要用到的是__________________。(填序号)除上述仪器外,尚缺最重要的仪器是 。
(2)计算所需浓硫酸的体积为___________m L(保留1位小数)。
(3)实验中用到玻璃棒,其作用分别是:___________、__________。
(4)配制时,一般可分为以下几个步骤:
①量取 ②计算 ③稀释 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却。其正确的操作顺序
为:②→①→③→____ →____→____→____→④(填序号)
(5)在配制过程中,下列操作可引起所配溶液浓度偏低的有____________(填序号)
①定容时,仰视刻度线。
②未冷却至室温就转移到容量瓶中。
③容量瓶中含有少量蒸馏水。
④未洗涤稀释浓硫酸时用过的烧杯和玻璃棒。
⑤定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线。
查看答案和解析>>
科目:高中化学 来源:2014届福建省高一上学期期中联考化学试卷 题型:填空题
(5分)现用18.4 mol·L-1的浓H2SO4来配制250 mL、0.300 mol·L-1的稀H2SO4。可供选择的仪器有: ①药匙 ②量筒 ③托盘天平 ④玻璃棒 ⑤烧瓶?
⑥胶头滴管 ⑦容量瓶 ⑧烧杯。 请回答下列问题:
(1)上述仪器中,在配制稀H2SO4时用不到的有 (填代号)。
(2)经计算,需浓H2SO4的体积为 。
现有① 5 mL ②10 mL ③20 mL 三种规格量筒,你选用的量筒是 (填代号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com