
【题目】实验室用电石和水反应制备的乙炔气体中含有少量的H2S气体,为了净化和检验乙炔气体,某学生设计如图所示装置,试回答下列问题

A B C
(1)写出A中发生反应的化学方程式__________________________
(2)饱和食盐水的作用是__________________
(3)B的作用是___________________________
(4)C中现象是__________________________,C中发生的反应类型是_________________
科目:高中化学 来源: 题型:
【题目】雯雯在自学碳酸钠性质时,查到了以下资料:
① CO2+ Na2CO3+ H2O === 2NaHCO3,CO2通入饱和碳酸钠溶液会产生白色沉淀,CO2不溶于饱和碳酸氢钠溶液。
② 碳酸钠、碳酸氢钠在不同温度下的溶解度
0℃ | 10℃ | 20℃ | 30℃ | |
Na2CO3 | 7.1 | 12.2 | 21.8 | 39.7 |
NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 |
【进行实验1】验证CO2通入饱和碳酸钠溶液会产生白色沉淀
① 配制碳酸钠溶液:取100 g 20℃的水,加入35 g碳酸钠固体,搅拌后,静置,取上层清液。
② 利用装置一进行实验,连续5分钟向新制得的碳酸钠溶液中通入CO2。
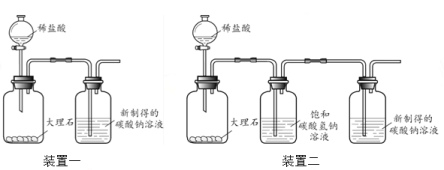
【发现问题】实验中,始终没有看到沉淀现象,原因是什么呢?雯雯进行了以下实验探究。
【进行实验2】
实验操作 | 实验现象 |
① 取100 g 20℃的水,加入35 g碳酸钠固体,搅拌后,静置,取上层清液 ② 利用装置二进行实验,连续5分钟向新制得的碳酸钠溶液中通入CO2 | 没有出现白色沉淀 |
(1)在0℃~30℃,Na2CO3和NaHCO3的溶解度受温度变化影响较大的是 。
(2)大理石与稀盐酸反应的化学方程式为 。
(3)装置二中饱和碳酸氢钠溶液的作用是 。
【进行实验3】
实验操作 | 实验现象 |
① 取100 g热开水,加入35 g碳酸钠固体,完全溶解,再降温至20℃,取上层清液 ② 利用装置一和装置二分别进行实验,连续3分钟向新制得的碳酸钠溶液中通入CO2 | 装置一和装置二中的碳酸钠溶液中均出现白色沉淀 |
(4)雯雯在最初的实验中没有看到沉淀现象的原因是 。
(5)CO2通入饱和碳酸钠溶液会产生白色沉淀的原因是 。
(6)请你依据题中信息,写出一种能够区分碳酸钠和碳酸氢钠固体的实验方案 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,中国的科学家将C60分子组装在一单层分子膜表面,在﹣268℃时冻结分子的热振荡,并利用扫描隧道显微镜首次“拍摄”到能清楚分辨碳原子间单、双键的分子图象.下列化合物分子中一定既含单键又含双键的是( )
A.CO2 B.COCl2 C.C2H4O D.H2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
①![]() Li+中含有的中子数与电子数之比为 2:1
Li+中含有的中子数与电子数之比为 2:1
②在 C2H6分子中极性共价键与非极性共价键数之比为 3:1
③常温下,11.2L的甲烷气体中含有的氢、碳原子数之比为 4:1
④5.6g铁与足量的氯气反应失去的电子与参与反应的铁的物质的量之比为2:1
A. ①② B. ②③ C. ①③ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,用0.10 mol·L-1的盐酸分别滴定体积相同且浓度均为0.10 mol·L-1的三种一元碱XOH、YOH 及ZOH,滴定曲线如图所示。下列说法正确的是
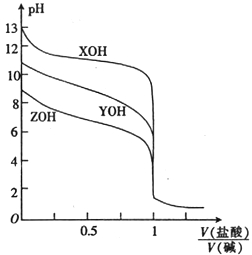
A. YOH 是强碱
B. V(盐酸)/V(碱)=0.5 时,c(Z+)>c(Y+ )>c(X+)
C. X++H2O![]() XOH+H+ 的平衡常数K=10-4
XOH+H+ 的平衡常数K=10-4
D. 滴定XOH 时可用酚酞作指示剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H、Al、O、N、S、Fe是常见的六种元素。
(1)S位于元素周期表______周期第______族,Fe的基态原子核外价电子排布式为______;O的基态原子核外有______种运动状态不同的电子。
(2)用“>”“<”或“=”填空
第一电离能 | 氧化性 | 沸点 | 非金属性 |
N______S | Fe3+______ Al3+ | NH3______H2O | 16O______18O |
(3)已知:下列两个热化学方程式:
4Fe(s)+302(g)=2Fe2O3(s)△H=﹣a kJ/mol
4Al(s)+3O2(g)=2Al2O3(s)△H=﹣b kJ/mol
则Al(s)的单质和Fe2O3(s)反应的热化学方程式是______。
(4)FeSO4溶液可与硝酸发生反应,写出此反应的离子方程式,并标出电子转移的方向和数目____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化钠样品中含有少量的杂质Na2SO4,按下列流程进行净化,流程中的( )中是合适的试剂,在[ ]中是实验操作名称。写出有关反应的化学方程式:

(1)操作①、②、③、⑤中所需加入试剂分别为_______、______、______、_____。
(2)操作①、④、⑥的操作名称分别为_________、_______、_______。
(3)写出有关的离子反应方程式:
第②步:_____________________________。
第⑤步:_____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com