
用100mL 1.00mol·L-1盐酸与100mL 1.10mol·L-1NaOH溶液在如下图所示的装置中进行中和热测定实验。以下是四次实验所得数据。回答下列问题:

实验 数据 | 盐酸起始温度t1/℃ | 氢氧化钠起始温度t2/℃ | 两溶液混合后 温度t3/℃ |
1 | 21.0 | 21.1 | 26.9 |
2 | 21.5 | 21.7 | 28.2 |
3 | 21.9 | 22.1 | 28.7 |
4 | 22.3 | 22.5 | 29.2 |
(1)上表中的温度差平均值为 ℃
(2)近似认为上述两种溶液的密度都是1 g·cm-3,中和后生成溶液的比热容c=4.18J·(g·℃)-1。则计算得到中和热ΔH= (取小数点后一位)。
(3)上述实验数值结果与57.3 kJ·mol-1有偏差,产生偏差的原因可能是(填字母) 。
a.实验装置保温、隔热效果差
b.用环形铜质搅拌棒代替环形玻璃搅拌棒
c.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
d.用温度计测定盐酸溶液起始温度后直接测定NaOH溶液的温度
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源:2017届新疆生产建设兵团二中高三上第二次月考化学卷(解析版) 题型:选择题
下列说法正确的是
A.石油裂解可以得到氯乙烯
B.油脂水解可得到氨基酸和甘油
C.所有烷烃和蛋白质中都存在碳碳单键
D.淀粉和纤维素水解的最终产物都是葡萄糖
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江省高三10月月考化学卷(解析版) 题型:选择题
金属铈(58Ce)常用于制作稀土磁性材料,可应用于制造玻璃、打火石、陶瓷和合金等。已知:Ce4++Fe2+=Ce3+ +Fe3+。下列说法正确的是
A.可用电解熔融CeO2制取金属铈,铈在阳极生成
B.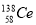 、
、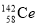 是同素异形体
是同素异形体
C.铈能溶于HI溶液,发生反应的离子方程式为:Ce+4H+=Ce4++2H2
D.铈的原子核外有58个电子
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省四地六校高一上第一次月考化学试卷(解析版) 题型:选择题
下列物质中,不能由两种单质直接化合得到的是( )
A.HCl B.Na2O2 C.MgO D.FeCl2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省四地六校高一上第一次月考化学试卷(解析版) 题型:选择题
关于金属钠的说法不正确的是( )
A.钠是银白色固体,质软 B.钠在自然界中既有游离态,又有化合态
C.少量的钠保存在煤油中 D.钠钾合金可以做原子反应堆的导热剂
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省四地六校高二上第一次月考化学试卷(解析版) 题型:选择题
某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见下图,电池总反应可表示为:2H2+O2=2H2O,下列有关说法正确的是( )
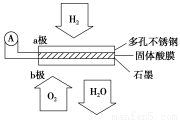
A.电子通过外电路从b极流向a极
B.H+由a极通过固体酸电解质传递到b极
C.b极上的电极反应式为:O2+2H2O+4e-=4OH-
D.每转移0.1 mol电子,消耗1.12 L的H2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省四地六校高二上第一次月考化学试卷(解析版) 题型:选择题
根据以下三个热化学方程式:
2H2S(g)+3O2(g)==2SO2(g)+2H2O(l) ΔH=-Q1 kJ/mol
2H2S(g)+O2(g)==2S(s)+2H2O(l) ΔH=-Q2 kJ/mol;
2H2S(g)+O2(g)==2S(s)+2H2O(g) ΔH=-Q3 kJ/mol。
判断Q1、Q2、Q3三者关系正确的是:( )
A.Q3>Q2>Q1 B.Q1>Q3>Q2 C.Q1>Q2>Q3 D.Q2>Q1>Q3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高二上第一次月考化学卷(解析版) 题型:选择题
用石墨作电极,电解1mol/L下列物质的溶液,溶液的PH值保持不变的是( )
A.HCl B.NaOH C.Na2SO4 D.NaCl
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高二上10月月考化学试卷(解析版) 题型:选择题
用纤维素为主要原料制备乙酸乙酯的路线如下:
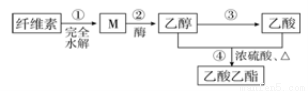
下列说法正确的是( )
A.若用淀粉替代纤维素,一定条件下也能按照此路线制备乙酸乙酯
B.M虽然分子结构中无醛基,但仍然可以发生银镜反应
C.步骤②,1molM完全反应可以生成3mol乙醇
D.③和④都发生了氧化还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com