
| A. | 8 | B. | 6 | C. | 5 | D. | 4 |
分析 同温同压下,M蒸气的密度是CO2的2倍,则该有机物的相对分子质量为88,88g该有机物的物质的量为:$\frac{8.8g}{88g/mol}$=0.1mol,浓硫酸吸收的是水,碱石灰吸收的是二氧化碳,水的物质的量=$\frac{10.8g}{18g/mol}$=0.6mol,二氧化碳的物质的量=$\frac{22g}{44g/mol}$=0.5mol,所以有机物、二氧化碳和水的物质的量之比=0.1mol:0.5mol:0.6mol=1:5:6,所以该有机物分子中含有5个碳原子、12个氢原子,该有机物的相对分子质量是88,88-5×12-12=16,所以该分子中还含有1个氧原子,其分子式为C5H12O,能够与钠反应生成氢气,说明属于醇,先书写戊基-C5H11异构体,戊基异构数目等于戊醇的异构体数目.
解答 解:同温同压下,M蒸气的密度是CO2的2倍,则该有机物的相对分子质量为88,88g该有机物的物质的量为:$\frac{8.8g}{88g/mol}$=0.1mol,浓硫酸吸收的是水,碱石灰吸收的是二氧化碳,水的物质的量=$\frac{10.8g}{18g/mol}$=0.6mol,二氧化碳的物质的量=$\frac{22g}{44g/mol}$=0.5mol,所以有机物、二氧化碳和水的物质的量之比=0.1mol:0.5mol:0.6mol=1:5:6,所以该有机物分子中含有5个碳原子、12个氢原子,该有机物的相对分子质量是88,88-5×12-12=16,所以该分子中还含有1个氧原子,其分子式为C5H12O,能够与钠反应生成氢气,说明为戊醇,戊基-C5H11可能的结构有:-CH2CH2CH2CH2CH3、-CH(CH3)CH2CH2CH3、-CH(CH2CH3)2、-CHCH(CH3)CH2CH3、-C(CH3)2CH2CH3、-CH(CH3)CH(CH3)2、-CH2CH2CH(CH3)2、-CH2C(CH3)3,则戊醇的可能结构有8种,
故选A.
点评 本题考查有机物的推断、同分异构体的书写等,难度中等,利用烃基异构判断,戊基异构数目等于戊醇的异构体数目.


科目:高中化学 来源: 题型:选择题
| A. | ①=②=③=④ | B. | ①=③>②=④ | C. | ④=②>③=① | D. | ①>③>②>④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠与水反应:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 氧化钠与盐酸:O2-+2H+═H2O | |
| C. | 碳酸氢钠溶液与稀硫酸:CO32-+2H+═H2O+CO2↑ | |
| D. | 烧碱溶液与碳酸氢钠溶液:HCO3-+OH-═H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加Fe的物质的量 | |
| B. | 将容器的体积缩小一半 | |
| C. | 保持体积不变,充入水蒸气 | |
| D. | 压强不变,充入Ne使容器的体积增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室制取硝基苯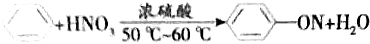 | |
| B. | 实验室制取溴苯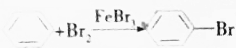 | |
| C. | 溴乙烷的消去反应 CH3CH2Br+NaOH$→_{△}^{H_{2}O}$CH2═CH2↑+NaBr+H2O | |
| D. | 制取TNT |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 目的 | 试剂或试验方法 | 说明 |
| A | 从苯中提溴 | 加CCl4 | 溴易溶于CCl4 |
| B | 检验含Fe3+溶液中是否含Fe2+ | 加高锰酸钾溶液 | 溶液紫色褪去,说明含Fe2+ |
| C | 配置1mol/LFeCl3溶液100mL | 将一定质量FeCl3溶液转移至容量瓶中加水定容 | 容量瓶规格须为100mL |
| D | 制取漂白粉 | 将氯气通入澄清石灰水中 | 氯气与氢氧化钙反应生成次氯酸钙 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
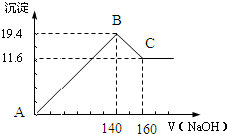
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用托盘天平称量时,将NaOH固体放在右盘内的纸上,称得质量为10.2g | |
| B. | 用25mL碱式滴定管量取高锰酸钾溶液,体积为16.60mL | |
| C. | 用干燥的广泛pH试纸测稀盐酸的pH=3.2 | |
| D. | 用10mL量筒量取NaCl溶液,体积为9.2mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com