
【题目】水煤气(CO 和H2)是合成甲醇的重要原料,它可用水蒸气通过炽热的炭层制得:C(s)+H2O(g)![]() CO(g)+H2(g) △H=+131.3kJ/mol
CO(g)+H2(g) △H=+131.3kJ/mol
⑴该反应的平衡常数的表达式为:_________________;升高温度,K值将 ;容器中气体的平均相对分子质量将 。(填“增大”、“减小”或“不变”)。
⑵上述反应达到平衡后,将体系中的C(s)部分移走,平衡将 (填序号)。
A.向左移 B.向右移 C.不移动
⑶下列事实能说明该反应在一定条件下已达到平衡状态的有 (填序号)。
A.单位体积内每消耗1molCO的同时生成1molH2
B.混合气体总物质的量保持不变
C.生成H2O(g)的速率与消耗CO的速率相等
D.H2O(g)、CO、H2的浓度相等
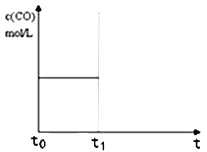
⑷上述反应在t0时刻达到平衡(如图),若在t1时刻改变某一条件,请在图中继续画出t1时刻后c(CO)随时间的变化曲线:
①缩小容器体积(用实线表示)。
②降低温度(用虚线表示)。
⑸某温度下,将4.0mol H2O(g)和足量的炭充入2L的密闭容器中,发生如下反应,C(s)+H2O(g)![]() CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为 。
CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为 。
【答案】(1) ![]() ; 增大;减小;(2)c;(3)AB;
; 增大;减小;(2)c;(3)AB;
(4)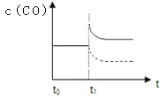 ;(5)50%。
;(5)50%。
【解析】
试题分析:(1)根据化学平衡常数的定义,平衡常数的表达式为:![]() ;正反应是吸热反应,升高温度,平衡向正反应方向移动,化学平衡常数只受温度的影响,故升高温度,平衡常数增大;假设全部进行到底,生成CO和H2的物质的量之比为1:1,此时气体平均摩尔质量为(28+2)/2g·mol-1=15g·mol-1,气体平均摩尔质量减少;(2)C是固体,浓度视为常数,减少碳的量,平衡不移动,故选项c正确;(3)A、用不同物质的反应速率表示,要求反应方向是一正一逆,且化学反应速率之比等于化学计量数之比,消耗CO,生成H2,反应是向正反应和逆反应方向进行,速率之比等于物质的量之比,故正确;B、碳是固体,反应前后气体系数之和不相等,因此气体总物质的量保持不变,说明反应达到平衡,故正确;C、根据选项A的分析,两者都是向逆反应方向进行,故错误;D、不知道开始时,通入量,因此无法判断,故错误;(4)①缩小容器的体积,压强增大,化学反应速率加快,平衡向逆反应方向移动,CO的浓度减小,瞬间时CO的浓度增大,达到平衡比原平衡时大,②降低温度,化学反应速率减缓,平衡向逆反应方向进行,t1瞬间CO的浓度不变,因此图像是:
;正反应是吸热反应,升高温度,平衡向正反应方向移动,化学平衡常数只受温度的影响,故升高温度,平衡常数增大;假设全部进行到底,生成CO和H2的物质的量之比为1:1,此时气体平均摩尔质量为(28+2)/2g·mol-1=15g·mol-1,气体平均摩尔质量减少;(2)C是固体,浓度视为常数,减少碳的量,平衡不移动,故选项c正确;(3)A、用不同物质的反应速率表示,要求反应方向是一正一逆,且化学反应速率之比等于化学计量数之比,消耗CO,生成H2,反应是向正反应和逆反应方向进行,速率之比等于物质的量之比,故正确;B、碳是固体,反应前后气体系数之和不相等,因此气体总物质的量保持不变,说明反应达到平衡,故正确;C、根据选项A的分析,两者都是向逆反应方向进行,故错误;D、不知道开始时,通入量,因此无法判断,故错误;(4)①缩小容器的体积,压强增大,化学反应速率加快,平衡向逆反应方向移动,CO的浓度减小,瞬间时CO的浓度增大,达到平衡比原平衡时大,②降低温度,化学反应速率减缓,平衡向逆反应方向进行,t1瞬间CO的浓度不变,因此图像是: ;
;
(5)C(s)+H2O(g)![]() CO(g)+H2(g)
CO(g)+H2(g)
起始: 4 0 0
变化: x x x
平衡: 4-x x x
根据化学平衡常数的定义,K=[c(CO)×c(H2)]/c(H2O)=x/2×x/2/(2-x)/2=1,
解得x=2,因此转化率为2/4×100%=50%。


科目:高中化学 来源: 题型:
【题目】已知K2Cr2O7溶液中存在如下平衡:Cr2O72-(橙色)+ H2O![]() 2H++ 2CrO42-(黄色)①向2 mL 0.1 mol·L-1 K2Cr2O7溶液中滴入3滴6 mol·L-1 NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色。②向2 mL 0.1 mol·L-1 酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应:Cr2O72- + 14H++ 6Fe2+=2Cr3+(绿色) + 6Fe3+ + 7H2O。
2H++ 2CrO42-(黄色)①向2 mL 0.1 mol·L-1 K2Cr2O7溶液中滴入3滴6 mol·L-1 NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色。②向2 mL 0.1 mol·L-1 酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应:Cr2O72- + 14H++ 6Fe2+=2Cr3+(绿色) + 6Fe3+ + 7H2O。
下列分析正确的是
A.实验①和②均能证明K2Cr2O7溶液中存在上述平衡
B.实验②能说明氧化性:Cr2O72-> Fe3+
C.CrO42-和Fe2+在酸性溶液中可以大量共存
D.稀释K2Cr2O7溶液时,溶液中各离子浓度均减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室中手不慎被玻璃划破,可用FeCl3溶液应急止血,其主要原因可能是( )。
A.FeCl3溶液有杀菌消毒作用
B.FeCl3溶液能使血液胶体发生聚沉
C.FeCl3溶液能产生Fe(OH)3沉淀堵住伤口
D.FeCl3能使血液发生化学反应
查看答案和解析>>
科目:高中化学 来源: 题型:
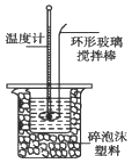
【题目】(12分)中和热的测定是高中重要的定量实验。取0.55 mol/L的NaOH溶液50 mL与0.50 mol/L的盐酸50 mL置于图所示的装置中进行中和热的测定实验,回答下列问题
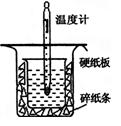
(1)从上图实验装置看,其中尚缺少的一种玻璃用品是_________ _,除此之外,装置中的一个明显错误是 。
(2)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热数值会_________,(填“偏大”、“偏小”或“不变”)。
(3)实验中改用60 mL 0.50 mol·L-1盐酸跟50 mL 0.55 mol·L-1 NaOH溶液进行反应,与上述实验相比,所求中和热 (填“相等”或“不相等”),简述理由: 。
(4)某实验小组用盐酸和氢氧化钠溶液做了三次实验,每次取溶液各50 mL,并记录下原始数据:
实验序号 | 起始温度t1/℃ | 终止温度(t2)/℃ | 温差(t2-t1)/℃ | ||
盐酸 | NaOH溶液 | 平均值 | |||
1 | 25.1 | 24.9 | 25.0 | 28.3 | 3.3 |
2 | 25.1 | 25.1 | 25.1 | 28.6 | 3.5 |
3 | 25.1 | 25.1 | 25.1 | 27.1 | 2.0 |
已知盐酸、NaOH溶液密度近似为1.00 g/cm3,中和后混合液的比热容c=4.18×10-3 kJ/(g·℃),根据计算结果,写出该中和反应的热化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求回答下列问题:
(1)在 ①液氯 ②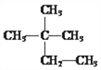 ③白磷 ④氯气
③白磷 ④氯气
⑤![]() ⑥
⑥![]() ⑦
⑦![]() ⑧红磷
⑧红磷
这八种物质中,互为同分异构体的是____,互为同素异形体的是_____。(填序号)
(2)在下列固体中:①CaCl2 ②KOH ③He ④H2SO4 ⑤NH4Cl ⑥金刚石
①其中不含化学键的晶体是_________,
②既含有离子键又含有共价键的物质是______,
③固体熔化时只需破坏共价键的晶体是____(填序号)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液进行中和热的测定。
Ⅰ.配制0.50 mol/L NaOH溶液
若实验中大约要使用245 mL NaOH溶液,至少需要称量NaOH固体 g
Ⅱ.测定稀硫酸和稀氢氧化钠中和热的实验装置如下图所示。
(1)写出该反应的热化学方程式(中和热为57.3 kJ/mol): 。
(2)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
①请填写下表中的空白:
温度 实验 次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②近似认为0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃)。则中和热△H= (取小数点后一位)。
③上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是: (填字母)。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在体积为2L的密闭容器中通入气体M和N并发生反应,物质的量随时间的变化关系如图。下列说法正确的是( )
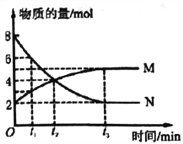
A. M、N之间转化的反应方程式为M =2N
B. t2时刻,反应达到平衡,正、逆反应速率达到相等
C. t3时刻,M的反应速率为![]() mol·L-1·min-l
mol·L-1·min-l
D. t1时刻,在容器内气体M和N的物质的量浓度之比为1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种无色溶液,它们分别是葡萄糖溶液、蔗糖溶液、淀粉溶液、甲酸乙酯中的一种。经实验可知:
(1)B、C均能发生银镜反应。
(2)A遇碘水变蓝色。
(3)A、C、D均能发生水解反应,水解液均能发生银镜反应。试判断它们各是什么物质,并写出有关化学反应方程式:
①A是__________,B是__________,C是____________,D是________。
②有关化学反应方程式:
a.蔗糖水解:__________________________,
b.葡萄糖发生银镜反应:____________________,
c.甲酸乙酯水解:__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com