
| A. | C2H6O和C2H4 | B. | C6H12O2和C5H12O | C. | C2H6O和C3H6O2 | D. | CH4和C2H4O2 |
分析 X、Y无论以何种比例混合,只要总物质的量不变,完全燃烧生成水的量不变,说明X、Y两物质的化学式中,氢原子数相同;二者耗氧量相同,则X、Y两化学式相差一个或若干个“CO2”基团,符合CxHy(CO2)n,可利用分子式的拆写法判断,以此解答该题.
解答 解:A.C2H6O和C2H4含有的H数目不同,物质的量比值不同,生成的水的物质的量不同,故A错误;
B.C6H12O2可写为CO2•C5H12,与C5H12O耗氧量不同,故B错误;
C.C3H6O2可写为CO2•C2H6,与C2H6O耗氧量不同,故C错误;
D.CH4、C2H4O2含有的H数目相同,在分子组成上相差1个“CO2”基团,只要其物质的量之和不变,完全燃烧时耗氧气量和生成水的物质的量也不变,故D正确;
故选D.
点评 本题考查有机物分子式的确定、混合物的计算,题目难度中等,注意有机物分子式的确定方法,试题有利于培养学生的分析、理解能力及灵活应用所学知识的能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 熔点、沸点:Li>Na>K>Rb>Cs | B. | 密度:Li<Na<K<Rb<Cs | ||
| C. | 原子半径:Li>Na>K>Rb>Cs | D. | 还原性:Li>Na>K>Rb>Cs |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烧煤时加入适量石灰石,可减少废气中SO2的量 | |
| B. | 二氧化碳是“城市空气质量日报”报道内容之一 | |
| C. | pH在 5.6~7之间的降水通常称为酸雨 | |
| D. | 某雨水样品放置一段时间后pH减小是因为水中溶解的CO2增多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅与任何酸都不反应 | |
| B. | 硅太阳能电池、计算机芯片、光导纤维都用到硅单质 | |
| C. | 硅的性质很稳定,能以单质形式存在于地壳中 | |
| D. | 水泥路桥、门窗玻璃、砖瓦、陶瓷餐具所用材料为硅酸盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

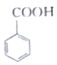 (苯甲酸)+C2H5OH$?_{△}^{浓硫酸}$
(苯甲酸)+C2H5OH$?_{△}^{浓硫酸}$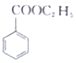 (苯甲酸乙酯)+H2O
(苯甲酸乙酯)+H2O| 物质 | 苯甲酸 | 乙醇 | 苯甲酸乙酯 |
| 熔点/℃ | 122.1 | -117.3 | -34.6 |
| 沸点/℃ | 249 | 78.3 | 213 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com