
 ,氢氧化钠的化学键类型为离子键、极性共价键,
,氢氧化钠的化学键类型为离子键、极性共价键, ;离子键、极性共价键;
;离子键、极性共价键;| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |


 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源: 题型:
| A、甲基橙呈红色的溶液中:MnO4-、Al3+、C2H5OH、SO42- |
| B、常温下的溶液:KW/c(H+)=0.1mol/L的溶液:K+、Na+、SiO32-、NO3- |
| C、稀硫酸中:K+、Mg2+、AlO2-、S2O32- |
| D、加入苯酚显紫色的溶液:K+、NH4+、Cl-、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、雾属于胶体,能产生丁达尔现象 |
| B、目前的雾霾污染,无需治理借助于天气状况改善即可 |
| C、PM2.5颗粒含有重金属、多种烃等有毒物质 |
| D、汽车尾气是目前城市大气污染气体和细小颗粒物产生的一个重要来源 |
查看答案和解析>>
科目:高中化学 来源: 题型:

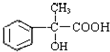 有多种同分异构体,写出所有符合下列条件的同分异构体的结构简式:
有多种同分异构体,写出所有符合下列条件的同分异构体的结构简式: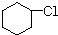 为原料合成
为原料合成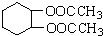
 )
)查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、超氧化钾(KO2)可作为飞船、潜艇等密闭系统的氧气再生剂,若有1molKO2被消耗,可产生O2 22.4L |
| B、高锰酸钾溶液是实验室常用的试剂,欲配置1.00L 0.10mol/L的KMnO4溶液,可将15.8g KMnO4溶于1L水中 |
| C、KNO3可用于制造黑火药,已知黑火药反应为S+2KNO3+3C=K2S+N2↑+3CO2↑,若有1mol KNO3被消耗,则该反应转移电子5×6.02×1023 |
| D、氰化钾(KCN、剧毒)可用于电镀,使镀层更细致,65g KCN晶体中,离子总数为2×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com