
如图所示的电化学装置,下列叙述正确的是
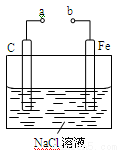
A.a和b用导线连接,电子由碳经过导线流向铁
B.a和b用导线连接,铁电极的电极反应为:Fe-3e-=Fe3+
C.a、b分别连接直流电源正、负极,可以防止铁被腐蚀
D.a、b分别连接直流电源负、正极,电压足够大时,Na+向铁电极移动
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源:2014-2015学年宁夏银川市高三上学期第四次月考理综化学试卷(解析版) 题型:填空题
(14分)A、B、D、E、F为短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。B在D中充分燃烧能生成其最高价化合物BD2。E+与D2-具有相同的电子数。A在F中燃烧,产物溶于水得到一种强酸。
(1)A在周期表位置________写出一种工业制备单质F的离子方程式:___________________。
(2)B、D、E组成的一种盐中,E的质量分数为43%,其俗名为_______其水溶液与F单质反应的化学方程式为__________________________________.
(3)由这些元素组成的物质,其组成和结构信息如下表:
物质 | 组成和结构信息 |
a | 含有A的二元离子化合物 |
b | 含有非极性共价键的二元离子化合物,且原子数之比为1∶1 |
c | 化学组成为BDF2 |
d | 只存在一种类型作用力且可导电的单质晶体 |
a的化学式为________;b的化学式为______________;
c的电子式为________, d是________晶体
(4)由A和B元素组成的二元化合物是 沼气的主要成分,其与氧气在酸性电解质溶液中组成燃料电池消耗标况下11.2L氧气时转移电子数为__________mol。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省高三上学期12月联考化学试卷(解析版) 题型:选择题
已知某有机物X的结构简式如图所示,下列有关叙述不正确的是

A.X的化学式为C10H10O6
B.X在一定条件下能与FeCl3溶液发生显色反应
C.1 mol X分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别为3 mol、4 mol、1 mol
D.X在一定条件下能发生消去反应和酯化反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高三上学期第二次联考理综化学试卷(解析版) 题型:选择题
“绿色化学实验”已走进课堂,下列做法符合“绿色化学”的是

①实验室收集氨气采用图1所示装置
②实验室中做氯气与钠反应实验时采用图2所示装置
③实验室中用玻璃棒分别蘸取浓盐酸和浓氨水做氨气与酸生成铵盐的实验
④实验室中采用图3所示装置进行铜与稀硝酸的反应
A.②③④ B.①②③ C.①②④ D.①③④
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省广州市高三1月模拟考试理综化学试卷(解析版) 题型:填空题
(16分)软锰矿的主要成分为MnO2,还含有Fe2O3、MgO、Al2O3、CaO等杂质,工业上用软锰矿制取MnSO4·H2O的流程如下:

已知:Fe3+、Al3+、Mn2+和Mg2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2、10.4、12.4;温度高于27℃时,MnSO4的溶解度随温度的升高而逐渐降低。
(1)“浸出”过程中MnO2转化为Mn2+的离子方程式为________。
(2)“浸出”过程中Fe2O3转化为Fe3+和Fe2+,相关反应的离子方程式为________。
(3)“滤渣1”的主要成分是__________,“调pH至5~6”所加的试剂是_________(填“石灰水”或“稀硫酸”)。
(4)根据下表数据,选择“第2步除杂”所加的物质A(由一种阳离子和一种阴离子组成),物质A的化学式为________。
Ksp 阳离子 | CO32- | F- | OH- |
Ca2+ | 5.0×10-9 | 1.5×10-10 | 4.7×10-6 |
Mg2+ | 3.8×10-6 | 7.4×10-11 | 5.6×10-12 |
Mn2+ | 2.2×10-11 | 5.3×10-3 | 2.1×10-13 |
Zn2+ | 1.2×10-10 | 3.0×10-2 | 6.9×10-17 |
(5)采用“趁热过滤”操作的原因是________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省广州市高三1月模拟考试理综化学试卷(解析版) 题型:选择题
化学与生活息息相关,下列说法正确的是
A.SO2、CO2和NO2都是可形成酸雨的气体
B.棉、麻和油脂都是高分子化合物
C.氧化铝陶瓷和光导纤维都是无机非金属材料
D.纤维素在人体内可水解成葡萄糖,供人体组织的营养需要
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省天水市高三一轮复习基础知识检测化学试卷(解析版) 题型:选择题
在一个不传热的固定容积的密闭容器中可逆反应mA(g)+nB(g) pC(g)+qQ(g) 当m、n、p、q为任意整数时,达到平衡的标志是
pC(g)+qQ(g) 当m、n、p、q为任意整数时,达到平衡的标志是
①体系的压强不再改变 ②体系的温度不再改变 ③各组分的浓度不再改变
④各组分的质量分数不再改变 ⑤反应速率v(A):v(B):v(C):v(D) =m:n:p:q
⑥单位时间内m mol A断键反应,同时pmol C也断键反应
A.③④⑤⑥ B.②③④⑥ C.①③④⑤ D.①③④⑥
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省襄阳市四校高一上学期期中联考化学试卷(解析版) 题型:填空题
(10分)(1)在KCl和CaCl2的混合物中,K+和Ca2+的物质的量之比为2:1,则KCl和CaCl2的物质的量之比为 ,若要取出含1mol Cl-的该混合物,应称取该混合物的质量为 g。
(2)同温、同压下某瓶充满O2时重106克,充满CO2时重112克,充满某气体时重98克。则某气体的相对分子质量为 。
(3)铜和浓硫酸发生反应的化学方程式为:Cu +2H2SO4(浓) CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
在该反应中,若消耗了32 g Cu,则转移了_ __mol 电子 ,生成 _ _L SO2(标准状况)气体。
查看答案和解析>>
科目:高中化学 来源:2014-2015吉林省松原市高一上学期期中化学试卷(解析版) 题型:选择题
下列各组溶液,只用试管和胶头滴管,不用任何试剂不可以鉴别的是
A. CaCl2和Na2CO3 B. 稀H2SO4和Na2CO3
C. KOH和Al2(SO4)3 D. HCl NaAlO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com