
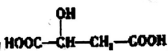
 ,下列说法错误的是( )
,下列说法错误的是( )| A. | lmol苹果酸可与2 molNaOH发生中和反应 | |
| B. | 一定条件下,苹果酸与乙酸或乙醇均能发生酯化反应 | |
| C. |  与苹果酸互为同分异构体 与苹果酸互为同分异构体 | |
| D. | lmol苹果酸与足量金属Na反应生成1.5molH2 |
科目:高中化学 来源: 题型:解答题
| 物质浓度(mol/L)时间(min) | NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 10 | 0.58 | 0.21 | 0.21 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.17 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 宇宙原子总数的88.6%是氢 | B. | 地球上的元素绝大多数是金属 | ||
| C. | 普鲁特“氢是元素之母”的预言 | D. | 宇宙中存在少量稀有气体分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 三种元素的氢化物中只有极性键没有非极性键 | |
| B. | Y元素最高价氧化物对应水化物的化学式可表示为H3YO4 | |
| C. | 三种元素的气态最简单氢化物中Z的氢化物最稳定 | |
| D. | 原子半径由大到小的顺序为Z>Y>X |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对应的最简单氢化物的热稳定性:Z>Y | |
| B. | X、Z、W三种元素形成的化合物既含离子键,又含共价键 | |
| C. | 元素X与Y形成的化合物中,每个原子都达到了8电子稳定结构 | |
| D. | X与Z可形成既含极性共价键又含非极性共价键的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | K+ Ba2+ Fe2+ Al3+ Fe3+ Mg2+ |
| 阴离子 | OH- HCO3- CO32- Cl- NO3- SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9 min | B. | 27 min | C. | 13.5 min | D. | 3 min |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸铝溶液和过量的NaOH溶液反应:Al3++4OH-=AlO2-+2H2O | |
| B. | Mg(OH)2与盐酸的反应:H++OH-═H2O | |
| C. | 硫化亚铁(FeS)与盐酸反应:S2-+2H+═H2S↑ | |
| D. | 钠和冷水反应:Na+2H2O═Na++H2↑+2OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com