
( 6分) 将6 mol X和3 mol Y混合气体置于体积可变的恒压容器中,在一定温度下发生如下反应:2X(g)+Y(g) 2Z(g)。反应达到平衡状态A时,测得气体总物质的量为6.6 mol。,回答下列问题:
2Z(g)。反应达到平衡状态A时,测得气体总物质的量为6.6 mol。,回答下列问题:
(1)达平衡状态A时,Y的转化率为____________,在达到平衡状态A的容器中通入少量Y,体系中X的体积分数____ __(填“增大”或“减小”或“不变”)。
(2)若要使反应开始时向逆反应方向进行,且达到平衡后各气体的物质的量与平衡状态A相同,若Z的起始物质的量用nz表示,则nz的取值范围是_ ___。
科目:高中化学 来源: 题型:阅读理解
| A | |||||||||||||||||
| B | C | D | E | F | |||||||||||||
| G | H | I | J | ||||||||||||||
| K | M | L |





查看答案和解析>>
科目:高中化学 来源: 题型:
反应形成的固体混合物(Fe2O3、FeO)中,元素铁和氧的质量比用m(Fe)∶m(O)表示。
(1)上述固体混合物中,m(Fe)∶m(O)不可能是________(填序号,多选扣分)。
a.21∶9 b.21∶7.5 c.21∶6
(2)若m(Fe)∶m(O)=21∶8,计算Fe2O3被CO还原的质量分数。
(3)设Fe2O3被CO还原的质量分数为A%,则A%和混合物中m(Fe)∶m(O)的关系式为〔用含m(Fe)、m(O)的代数式表示〕。
A%=________________。
(4)如果Fe2O3和CO的反应分两步进行:
3Fe2O3+CO====2Fe3O4+CO2
Fe3O4+CO====3FeO+CO2
试分析反应形成的固体混合物可能的组成及相应的m(Fe)∶m(O)〔令m(Fe)∶m(O)=21∶a,写出a的取值范围〕。将结果填入下表。
混合物组成(用化学式表示) | a的取值范围 |
|
|
查看答案和解析>>
科目:高中化学 来源:2013届湖北省武汉市四校高三10月联考化学试卷(带解析) 题型:实验题
(10分)硫酸工业尾气中二氧化硫的含量超过0.05%(体积分数)时需经处理后才能排放。某校化学兴趣小组欲测定某硫酸工厂排放尾气中二氧化硫的含量,分别采用以下方案:
[甲方案]:如右图所示,图中气体流量计B用于准确测量通过的尾气体积。将尾气通入一定体积已知浓度的碘水中测定SO2的含量。当洗气瓶C中溶液蓝色消失时,立即关闭活塞A。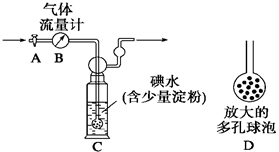
(1)洗气瓶C中导管末端连接一个多孔球泡D,可以提高实验的准确度,其理由是___________________________________。
(2)洗气瓶C中溶液蓝色消失后,没有及时关闭活塞A,测得的SO2含量____________(填“偏高”、“偏低”或“无影响”)。
[乙方案]:实验步骤如下面流程图所示: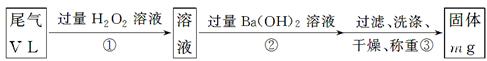
(3)步骤①中过量H2O2的作用是
(4)写出步骤②中反应的化学方程式__________________________________________
(5)步骤②中Ba(OH)2是否足量的判断方法是__________________________________
______________________________________________________________________。
(6)通过的尾气体积为V L(已换算成标准状况)时,该尾气中二氧化硫的含量(体积分数)为_____________________________(用含有V、m的代数式表示)。
查看答案和解析>>
科目:高中化学 来源:2013届浙江省嘉兴一中高三10月月考化学试卷(带解析) 题型:实验题
(共14分)为研究铁质材料与热浓硫酸的反应,某学习小组用碳素钢(即铁和碳的合金)进行了以下探究活动:
[探究一]
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是____________。
(2)称取碳素钢6.0g放入15.0mL浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。
①甲同学认为X中除Fe3+之外还可能含有Fe2+。若要确认其中的Fe2+,应选用 (选填序号)。
A.KSCN溶液和氯水 B.铁粉和KSCN溶液 C.浓氨水 D.酸性KMnO4溶液
②乙同学取560mL(标准状况)气体Y通入足量溴水中,发生SO2+Br2+2H2O===2HBr+H2SO4反应,然后加入足量BaCl2溶液,经适当操作后得干燥固体4.66g。由此推知气体Y中SO2的体积分数为 。
[探究二]
根据上述实验中SO2体积分数的分析,丙同学认为气体Y中还可能含有Q1和Q2两种气体,其中Q1气体,在标准状况下,密度为0.0893g·L-1。为此设计了下列探究实验装置(图中夹持仪器省略,假设有关气体完全反应)。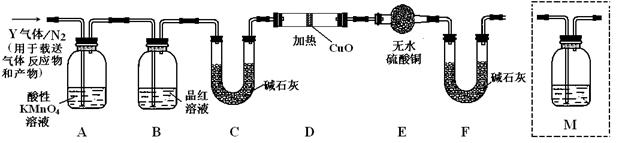
(3)装置B中试剂的作用是
(4)分析Y气体中的Q2气体是如何生成的 (用化学方程式表示)。
(5)为确认Q2的存在,需在装置中添加洗气瓶M于 (选填序号)。
A.A之前 B.A-B间 C.B-C间 D.C-D间
(6)如果气体Y中含有Q1,预计实验现象应是
查看答案和解析>>
科目:高中化学 来源:2012-2013学年浙江省高三10月月考化学试卷(解析版) 题型:实验题
(共14分)为研究铁质材料与热浓硫酸的反应,某学习小组用碳素钢(即铁和碳的合金)进行了以下探究活动:
[探究一]
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是____________。
(2)称取碳素钢6.0g放入15.0mL浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。
① 甲同学认为X中除Fe3+之外还可能含有Fe2+。若要确认其中的Fe2+,应选用 (选填序号)。
A.KSCN溶液和氯水 B.铁粉和KSCN溶液 C.浓氨水 D.酸性KMnO4溶液
② 乙同学取560mL(标准状况)气体Y通入足量溴水中,发生SO2+Br2+2H2O===2HBr +H2SO4反应,然后加入足量BaCl2溶液,经适当操作后得干燥固体4.66g。由此推知气体Y中SO2的体积分数为 。
[探究二]
根据上述实验中SO2体积分数的分析,丙同学认为气体Y中还可能含有Q1和Q2两种气体,其中Q1气体,在标准状况下,密度为0.0893g·L-1。为此设计了下列探究实验装置(图中夹持仪器省略,假设有关气体完全反应)。

(3)装置B中试剂的作用是
(4)分析Y气体中的Q2气体是如何生成的 (用化学方程式表示)。
(5)为确认Q2的存在,需在装置中添加洗气瓶M于 (选填序号)。
A.A之前 B.A-B间 C.B-C间 D.C-D间
(6)如果气体Y中含有Q1,预计实验现象应是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com