
| 编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 实验 |  | 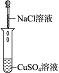 | 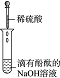 | 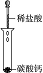 |
分析 (1)氯化钡和硫酸铜反应生成硫酸钡沉淀;
(2)检验氯离子与铜离子是否反应;
(3)发生中和反应,溶液由红色变为无色;
(4)盐酸和碳酸钙反应生成氯化钙、水和二氧化碳.
解答 解:(1)氯化钡和硫酸铜反应生成硫酸钡白色沉淀,反应的离子方程式为Ba++SO42+=BaSO4↓,故答案为:有白色沉淀产生;Ba++SO42+=BaSO4↓;
(2)实验Ⅰ中还存在氯离子和铜离子,实验Ⅱ可验证Cl-与Cu2+不发生反应,故答案为:验证Cl-与Cu2+不发生反应;
(3)发生中和反应,溶液由红色变为无色,说明H+、OH-发生反应,故答案为:H+、OH-;
(4)盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,反应的离子方程式为CaCO3+2H+═Ca2++CO2↑+H2O,故答案为:CaCO3+2H+═Ca2++CO2↑+H2O.
点评 本题考查离子反应以及离子方程式,为高频考点,侧重于学生的分析能力的考查,注意把握常见物质的性质以及实验的原理,难度不大.


科目:高中化学 来源:2016-2017学年甘肃省高二上第一次学段考试化学卷(解析版) 题型:选择题
海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。
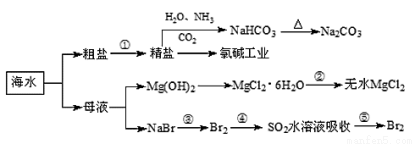
下列有关说法正确的是( )
A.在第③、④、⑤步骤中,溴元素均被氧化
B.制取NaHCO3的反应是利用其在此反应所涉及物质中溶解度最小
C.用澄清的石灰水可鉴别NaHCO3和Na2CO3
D.工业上通过电解饱和MgCl2溶液制取金属镁
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

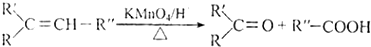
 .
.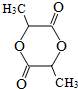 .
.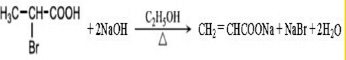 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡是放热反应都是自发的,凡是吸热反应都是非自发的 | |
| B. | 自发反应一定是放热反应,非自发反应一定是吸热反应 | |
| C. | 自发反应在恰当条件下才能实现 | |
| D. | 自发反应在任何条件下都能实现 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡是含有碳元素的化合物都是有机化合物 | |
| B. | 所有的有机化合物均难溶解于水 | |
| C. | 有机物组成元素较少,而有机物的种类繁多 | |
| D. | 完全燃烧只生成CO2和H2O的有机物是烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
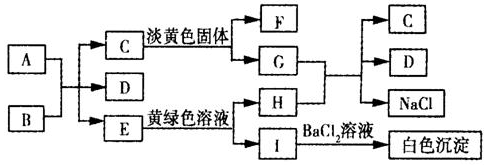
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
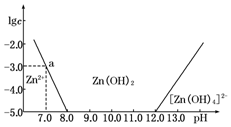
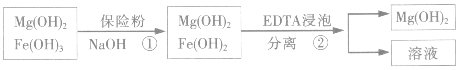
| 精制阻燃剂的条件 | 阻燃剂铁含量 | |||
| 序号 | 提纯体系温度/℃ | 加入EDTA质量/g | 加入保险粉质量/g | W(Fe)/(10-4g) |
| 1 | 40 | 0.05 | 0.05 | 7.63 |
| 2 | 40 | 0.05 | 0.10 | 6.83 |
| 3 | 60 | 0.05 | 0.10 | 6.83 |
| 4 | 60 | 0.10 | 0.10 | 6.51 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
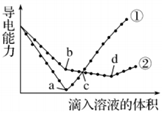
| A. | b点,水电离产生的c(H+)<10-7mol/L | B. | ①代表滴加H2SO4溶液的变化曲线 | ||
| C. | a、d两点对应的溶液均显中性 | D. | c点,两溶液中含有相同量的 OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 次氯酸钙的化学式:CaClO2 | |
| B. | 作为相对原子质量标准的碳原子可表示为:126C | |
| C. | 钠原子的结构示意图: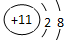 | |
| D. | 硫酸的电离方程式:H2SO4═H++SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com