
在一密闭容器中进行如下反应:2SO2(g)+O2(g) 2SO3(g),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是( )
2SO3(g),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是( )
A.SO2为0.4mol/L、O2为0.2mol/L B.SO2为0.25mol/L
C.SO2、SO3均为0.15mol/L D.SO3为0.4mol/L
B
【解析】
试题分析:SO2、O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,用极端假设法,若反应物全部转化为生成物,则SO3的浓度最大是0.4mol/L;若生成物全部转化为反应物,则SO2、O2的浓度分别为0.4mol/L、0.2mol/L,因为该反应是可逆反应,所以反应不会进行到底,所以介于二者之间的是有可能的。A、违背可逆反应的限度,错误;B、SO2为0.25mol/L介于0-0.4mol/L之间,正确;C、二氧化硫、三氧化硫的浓度不可能都减小,错误;D、三氧化硫的浓度不可能是0.4mol/L,错误,答案选B。
考点:考查可逆反应的限度的判断


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015学年浙江省东阳外国语学校高二上学期期中化学试卷(解析版) 题型:选择题
用水稀释0.1 mol·L-1的CH3COOH溶液,其中随水的量增加而增大的是([ ]表示浓度)

A.①②③ B.②③⑤ C.④⑤ D.④⑤⑥
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南鄢陵县第一高中高二上第一次考试化学(B)试卷(解析版) 题型:选择题
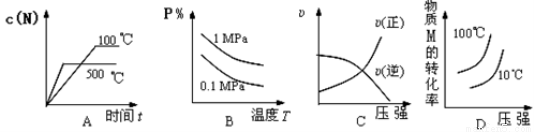
对于可逆反应:2M(g)+N(g) 2P(g) ΔH<0,下列各图中正确的是( )
2P(g) ΔH<0,下列各图中正确的是( )
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南鄢陵县第一高中高二上第一次考试化学(A)试卷(解析版) 题型:填空题
(9分)在体积为1 L的密闭容器中,进行如下化学反应:
CO2(g)+H2(g) CO(g)+H2O(g),化学平衡常数K与温度T的关系如下表:
CO(g)+H2O(g),化学平衡常数K与温度T的关系如下表:
T/℃ | 700 | 800 | 850 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的平衡常数表达式K=__________,升高温度,化学平衡向__________
(填“正反应”或“逆反应”)方向移动。
(2)能判断该反应达到化学平衡状态的依据是________。
A c(CO2)=c(CO) B K不变 C 容器中的压强不变
D.v正(H2)=v正(CO2) E.c(H2)保持不变
(3)若某温度下,平衡浓度符合下列关系:c(CO2)·c(H2)=c(CO)·c(H2O),此时的温
度为_____;在此温度下,若向该容器中投入1 mol CO2、1.2 mol H2、0.75 mol
CO、1.5 mol H2O,则此时反应朝______方向进行(填“正反应”、“逆反应”)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南鄢陵县第一高中高二上第一次考试化学(A)试卷(解析版) 题型:选择题
X、Y、Z三种气体,把a mol X与b mol Y充入一密闭容器中,发生反应:
X+2Y 2Z。达到平衡时,若它们的物质的量满足:n(X)+n(Y)=n(Z),则Y的转
2Z。达到平衡时,若它们的物质的量满足:n(X)+n(Y)=n(Z),则Y的转
化率为
A.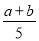 ×100% B.
×100% B.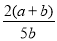 ×100%
×100%
C.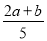 ×100% D.
×100% D.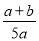 ×100%
×100%
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南鄢陵县第一高中高二上第一次考试化学(A)试卷(解析版) 题型:选择题
下列说法正确的是
A.需要加热才能发生的反应一定是吸热反应
B.核能、太阳能、生物质能、风能、氢能均属于新能源
C.自发反应的熵一定增大,非自发反应的熵一定减小
D.常温下,反应C(s)+CO2(g) 2CO(g)不能自发进行,则该反应的ΔH>0
2CO(g)不能自发进行,则该反应的ΔH>0
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南鄢陵县第一高中高一上第一次考试化学(B)试卷(解析版) 题型:选择题
设NA代表阿伏加德罗常数的值,下列说法不正确的是( )
A.醋酸的摩尔质量(单位:g/mol)与NA个醋酸分子的质量在数值上相等
B.NA个氧分子和NA个氢分子的质量比等于16:1
C.28克氮气所含的原子数目为NA
D.在标准状况下,0.5NA个氯气分子所占体积约为11.2L
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南鄢陵县第一高中高一上第一次考试化学(A)试卷(解析版) 题型:填空题
(10分)用2.4mol/L的H2SO4溶液配制100mL浓度为0.2 mol/L的稀H2SO4,回答下列问题:
(1)需要量取2.4 mol/L的H2SO4溶液的体积是 mL。
(2)配制过程有下列几步操作:
A 用量筒量取所需H2SO4溶液的体积,注入盛有适量水的烧杯中,用玻璃棒搅拌,使其混合均匀;
B 将蒸馏水加入容量瓶至液面接近刻度线1cm~2cm处;
C 向烧杯中加入约20mL蒸馏水;
D.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液也转移到容量瓶中;
E.用 ① 加水至刻度线;
F.待烧杯中溶液冷却后,沿玻璃棒转移到 ② ;
G.盖好瓶塞,反复颠倒摇匀。
以上各步骤操作的先后顺序是 ③ (填字母)
(3)取上述所配溶液10mL与足量BaCl2溶液反应,生成白色沉淀0.48 g。则该溶液浓度
0.2 mol/L(填“大于”“等于”或“小于”)造成此误差的操作可能是
A 定容时俯视容量瓶 B 用量筒取2.4mol/L H2SO4溶液时俯视读数
C 使用容量瓶前未干燥 D.使用的烧杯和玻璃棒未洗涤彻底
E.定容时将蒸馏水洒在容量瓶外面
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省高一上第二次考试化学试卷(解析版) 题型:选择题
离子方程式H+ + OH -= H2O所表示的反应是( )。
A.所有酸和碱之间的中和反应
B.强酸溶液与强碱溶液生成可溶性盐和水的反应
C.所有可溶性酸和可溶性碱之间的中和反应
D.所有强酸和强碱之间的中和反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com