
����Ŀ��ij�о�С�鰴����·�ߺϳ�ҩ��θ����:

��֪: ![]()
��ش�:
��1��������A�Ľṹ��ʽ_______��
��2������˵������ȷ����_______��
A��������B�ܷ����ӳɷ�Ӧ B��������D����FeCl3��Һ������ɫ��Ӧ
C��������E���м��� D��θ�����ķ���ʽ��C13H22ClN3O2
��3����ƻ�����C��������Ӧת��ΪD �ĺϳ�·��(������ͼ��ʾ���Լ���ѡ) _______��
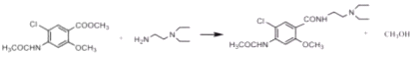
��4��д��D+EF�Ļ�ѧ����ʽ_______��
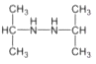
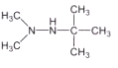
��5��д��������E���ܵ�ͬ���칹��Ľṹ��ʽ_______����ͬʱ����:��1H-NMR�ױ�����������3����ԭ�ӣ�IR����ʾ��NһH�����ڣ��ڷ�����û��ͬһ��̼��������( )���Ľṹ��
)���Ľṹ��
���𰸡� ![]() BD
BD ![]()
 ��
��![]() ��
��
����������������ͼ���������������ķ�ʽ������E�в����ڱ����ṹ����D�к��б����ṹ�����A�к��б���������θ�����Ľṹ��E�ķ���ʽ��EΪ![]() �����D�Ļ�ѧʽ��DΪ
�����D�Ļ�ѧʽ��DΪ![]() �����Fˮ���dz�������θ���������м״����ɡ�A��״�����B��B�����ᷴӦ����C��C����2����Ӧ����D����������ԭ�ӣ����AΪ
�����Fˮ���dz�������θ���������м״����ɡ�A��״�����B��B�����ᷴӦ����C��C����2����Ӧ����D����������ԭ�ӣ����AΪ![]() ��BΪ
��BΪ![]() ��CΪ
��CΪ![]() ��
��
(1)��������������������A�Ľṹ��ʽΪ![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
(2)A��������BΪ![]() �����б������������������ӳɷ�Ӧ����ȷ��B��������DΪ
�����б������������������ӳɷ�Ӧ����ȷ��B��������DΪ![]() �������ڷ��ǻ�����������FeCl3��Һ������ɫ��Ӧ������
�������ڷ��ǻ�����������FeCl3��Һ������ɫ��Ӧ������
C��������EΪ![]() �����а��������м��ԣ���ȷ��D��θ�����ķ���ʽ��C13H21ClN3O2������ѡBD��
�����а��������м��ԣ���ȷ��D��θ�����ķ���ʽ��C13H21ClN3O2������ѡBD��
(3)���ǻ����л�ԭ�ԣ����ױ���������˻�����C��������Ӧת��ΪDʱ��Ҫ�������ǻ���������Ϣ��C������![]() ��Ӧ����
��Ӧ����![]() �����������Ȼ���������ʱ���������������ϵ�ȡ����Ӧ���ɣ��ϳ�·��Ϊ
�����������Ȼ���������ʱ���������������ϵ�ȡ����Ӧ���ɣ��ϳ�·��Ϊ![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
(4)D+EF�Ļ�ѧ����ʽΪ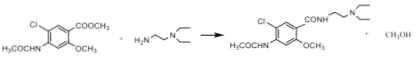 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
(5)EΪ![]() ����1H-NMR�ױ�����������3����ԭ�ӣ�IR����ʾ��NһH�����ڣ��ڷ�����û��ͬһ��̼��������(
����1H-NMR�ױ�����������3����ԭ�ӣ�IR����ʾ��NһH�����ڣ��ڷ�����û��ͬһ��̼��������(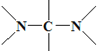 )���Ľṹ����������������E��ͬ���칹����
)���Ľṹ����������������E��ͬ���칹����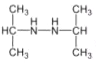 ��
��![]() ��
��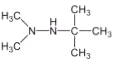 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��![]() ��
�� ��
��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�ܷ���ϵ�з������з�Ӧ��N2��g����3H2��g��![]() 2NH3��g������H<0����ͼ��ijһʱ�����N2�ķ�Ӧ�����뷴Ӧ���̵����߹�ϵͼ��
2NH3��g������H<0����ͼ��ijһʱ�����N2�ķ�Ӧ�����뷴Ӧ���̵����߹�ϵͼ��

�ش��������⣺
��1������ƽ��״̬��ʱ�����______��________��________��
��2��t1��t3��t4ʱ����ϵ�зֱ���ʲô���������˱仯��________��________��________��
��3�����и�ʱ���ʱ�����İٷֺ�����ߵ���________�����������
A��t0��t1 B��t2��t3
C��t3��t4 D��t5��t6
��4����t0��t1 �� t2��t3 N2��ƽ����Ӧ���ʷֱ�Ϊ________��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25 ��ʱ������H2A��HA-��A2-����ˮ��Һ��ϵ�У�H2A��HA-��A2- �����и�����ռ�����ʵ�����������������ҺpH�仯�Ĺ�ϵ��ͼ��ʾ������˵����ȷ����
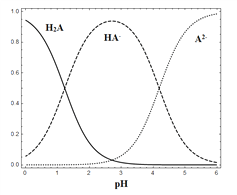
A. �ں�H2A��HA-��A2- ����Һ�У���������NaOH���壬����HA-��һ������
B. �������ʵ�����NaHA��Na2A���������ˮ�����õ���Һ������HA-��=����A2-��
C. NaHA��Һ�У�HA-��ˮ������С��HA-�ĵ�������
D. �ں�H2A��HA-��A2-����Һ�У���c(H2A)+2c(A2-)+c(OH-)=c(H+)��������H2A��������HA-��һ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У�ֻҪ������һ���������Ժ��ֱ�����ϣ���ȫȼ�գ����ɵĶ�����̼��ˮ������Ҳ���Ƕ�ֵ��(����)
A. ��������� B. �������ϩ
C. �������ϩ D. ��ϩ�ͱ�ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ҫ�����ȶ��ĸ߷е�Һ̬�л���͵ͷе�����ʵĻ��������ᴿһ��ʹ���� ��
A. ���� B. �ؽᾧ C. ���� D. ��ȡ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����¶Ȳ���������£��ں��ݵ������н������з�Ӧ��N2O4��g���T2NO2��g������N2O4��Ũ����0.1molL��1����0.07molL��1��Ҫ15s����ôN2O4��Ũ����0.07molL��1����0.05molL��1����ķ�Ӧʱ�䣨 ��
A.����5s
B.����10s
C.��10s
D.����10s
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£���NO2��SO2�������1:2���ں����ܱ������з�����Ӧ: NO2(g)+SO2(g)![]() SO3(g)+NO(g����H=-41.8kJ/mol��������˵����Ӧ�ﵽƽ��״̬����
SO3(g)+NO(g����H=-41.8kJ/mol��������˵����Ӧ�ﵽƽ��״̬����
A. ��ϵѹǿ���ֲ��� B. ���������ɫ���ֲ���
C. SO3��NO������ȱ��ֲ��� D. ÿ����1 mol SO3��ͬʱ����1 mol NO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ�����
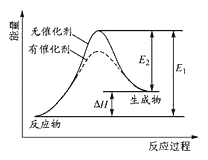
��1��ij��Ӧ�ķ�Ӧ�����������仯��ͼ��ʾ���ش���������:
E�淴Ӧ�Ļ��___E��Ӧ�Ļ��(��������������С����)
��2��50mL 0.50mol/L������50mL 0.55mo/L NaOH��ҹ����ͼ��ʾ��װ���н����кͷ�Ӧ�����ⶨ��Ӧ���������ų��������ɼ����к��ȣ��ش���������:
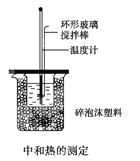
���ձ�����������ĭ����������________
��ʵ���и���60mL 0.50mol/L������50mL 0.55mol/L NaOH��Һ���з�Ӧ��������ʵ����ȣ����ų�������_________(��������������������)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������10 mL 0.1 mol��L��1NaOH��Һ�м���0.1 mol��L��1��һԪ��HA����ҺpH�ı仯������ͼ��ʾ������˵����ȷ����(����)
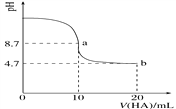
A. a����ʾ��Һ��c(Na��)>c(A��)>c(H��)>c(HA)
B. a��b������ʾ��Һ��ˮ�ĵ���̶���ͬ
C. pH��7ʱ��c(Na��)��c(A��)��c(HA)
D. b����ʾ��Һ��c(A��)>c(HA)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com