
| 容器 | 甲 | 乙 | 丙 | |
| 反应物投入量 | 1 molCO、2 mol H2 | 1mol CH3OH | 2mol CH3OH | |
| 衡 时 数据 | CH3OH的浓度(mol•L-1) | c1 | c2 | c3 |
| 反应的能量变化 | a kJ | bkJ | ckJ | |
| 体系压强(Pa) | p1 | p2 | p3 | |
| 反应物转化率 | a1 | a2 | a3 | |
| A. | 2 c1>c3 | B. | |a|+|b|=90.8 | C. | 2 p2<p3 | D. | a1+a3<1 |
分析 A.甲、丙相比较,把甲等效为开始加入1molCH3OH,丙中甲醇的物质的量为甲的2倍,压强增大,对于反应CH3OH(g)?CO(g)+2H2(g),平衡向生成甲醇的方向移动;
B.由题目可知生成1molCH3OH的能量变化为90.8kJ,甲、乙平衡状态相同,平衡时相同物质的物质的量相等,设平衡时甲醇为nmol,计算反应热数值;
C.比较乙、丙可知,丙中甲醇的物质的量为乙的2倍,压强增大,对于反应CH3OH(g)?CO(g)+2H2(g),平衡向生成甲醇的方向移动;
D.甲、乙处于相同的平衡状态,则α1+α2=1,结合α2>α3分析.
解答 解:A.甲、丙相比较,把甲等效为开始加入1molCH3OH,丙中甲醇的物质的量为甲的2倍,增大了压强,平衡CH3OH(g)?CO(g)+2H2(g)向生成甲醇的方向移动,则2c1<c3,故A错误;
B.由题目可知生成1molCH3OH的能量变化为90.8kJ,甲、乙平衡状态相同,设平衡时甲醇为nmol,对于甲容器:a=90.8n,对于乙容器:b=90.8(1-n),故a+b=90.8,故B正确;
C.比较乙、丙可知,丙中甲醇的物质的量为乙的2倍,压强增大,对于反应CH3OH(g)?CO(g)+2H2(g),平衡向生成甲醇的方向移动,则2p2>p3,故C错误;
D.甲、乙处于相同的平衡状态,则α1+α2=1,由C可知α2>α3,则a1+a3<1,故D正确,
故选BD.
点评 本题考查了化学平衡的计算,题目难度中等,涉及等效平衡、转化率、化学平衡及其影响等知识,明确等效平衡的含义为解答关键,注意掌握化学平衡及其影响,试题培养了学生的分析、理解能力及逻辑推理能力.


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 压强/MPa 体积分数/% 温度/℃ | 1.0 | 20 | 3.0 |
| 810 | 54.0 | a | b |
| 915 | c | 75.0 | d |
| 1000 | e | f | 83.0 |
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 取反应后溶液,滴入几滴KSCN溶液,无血红色出现 | |
| B. | 该合金中铁与铜的物质的量之比是1:2 | |
| C. | 反应后溶液(忽略溶液体积变化)中c(H+)=2.5 mol•L-1 | |
| D. | 向反应后的溶液中加入2.0 mol•L-1NaOH溶液至金属离子恰好全部沉淀时,需加入NaOH溶液的体积是120 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
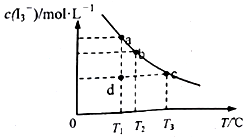 I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)═I3-(aq),某I2、KI混合溶液中,c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)下列说法不正确的是( )
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)═I3-(aq),某I2、KI混合溶液中,c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)下列说法不正确的是( )| A. | 温度为T1时,向该平衡体系中加入KI固体,平衡正向移动 | |
| B. | 反应I2(aq)+I-(aq)═I3-(aq)△H<0 | |
| C. | 若T1时,反应进行到状态d时,一定有v正>v逆 | |
| D. | 状态a与状态b相比,状态b时I2的转化率更高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向淀粉水解后的溶液中滴加碘水,即可检验淀粉是否水解 | |
| B. | NaAlO2 溶液中滴加 Na2 CO3 溶液,有沉淀和气体生成 | |
| C. | 将 SO2 分别通入硝酸钡溶液和溶有氨气的氯化钡溶液中产生的沉淀成分不同 | |
| D. | 用铂丝蘸取少量试液进行焰色反应,火焰呈黄色的一定是钠盐溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
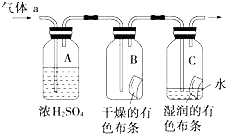 甲同学设计如图所示装置研究氯气能否与水发生反应.气体a是含有少量空气和水蒸气的氯气.请回答下列问题:
甲同学设计如图所示装置研究氯气能否与水发生反应.气体a是含有少量空气和水蒸气的氯气.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com