

| ||
| ||
| ||
| ||
| ||
| ||
| ||
| ||



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 ��2013?̩����ģ��SO2��NO��NO2��CO������Ⱦ�������к����壬������л��������ǽ��ܼ��ŵ���Ҫ���⣮
��2013?̩����ģ��SO2��NO��NO2��CO������Ⱦ�������к����壬������л��������ǽ��ܼ��ŵ���Ҫ���⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ��ɽ��ʡ̩���и��������ָ�ϰ����������ۻ�ѧ�Ծ��������棩 ���ͣ������
SO2 ��NO��NO2��CO������Ⱦ�������к����壬������л��������ǽ��ܼ��ŵ���Ҫ���⡣
��1����������������ֱ���������ʱ�������������__________���ѧʽ����
��2����֪��2SO2(g)+ O2(g)=2SO3(g)����H=��196.6kJ/mol
O2(g)+2NO(g)=2NO2(g)����H=��113.0kJ/mol
�ٷ�Ӧ��NO2(g) +SO2(g)= SO3(g) +NO(g)�ġ�H=_ kJ/mol��
��һ�������£���NO2��SO2�������1��1���ں��º��ݵ��ܱ������з�����Ӧ�� NO2(g) +SO2(g)  SO3(g) +NO(g)��
SO3(g) +NO(g)��
���в���˵����Ӧ�ﵽƽ��״̬����_____������ĸ����
a����ϵѹǿ���ֲ���
b������������ɫ���ֲ���
c��NO�����ʵ������ֲ���
d��ÿ����1molSO3��ͬʱ����1molNO2
��3��CO�����ںϳɼ״����䷴Ӧ�Ļ�ѧ����ʽΪCO(g)+2H2(g)
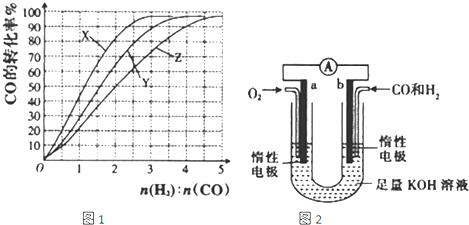
 CH3OH(g)����һ�ݻ��ɱ���ܱ������г���10molCO��20mol H2���ڴ��������·�����Ӧ���ɼ״���CO��ƽ��ת���ʣ��������¶ȣ�T����ѹǿ��p���Ĺ�ϵ��ͼ��ʾ��
CH3OH(g)����һ�ݻ��ɱ���ܱ������г���10molCO��20mol H2���ڴ��������·�����Ӧ���ɼ״���CO��ƽ��ת���ʣ��������¶ȣ�T����ѹǿ��p���Ĺ�ϵ��ͼ��ʾ��

�������ϳɼ״��ķ�ӦΪ______������ȡ������ȡ�����Ӧ��
��A��B��C�����ƽ�ⳣ��KA��KB��KC�Ĵ�С��ϵΪ___________��
�����ﵽƽ��״̬Aʱ�����������Ϊ10L������ƽ��״̬Bʱ���������Ϊ_____L��
��4��ij�о�С���������ͼ��ʾ�ļ״�ȼ�ϵ��װ�á�

�ٸõ�ع���ʱ��OH-��______���a����b�������ƶ���
�ڵ�ع���һ��ʱ������Һ��pH��С����õ���ܷ�Ӧ�����ӷ���ʽΪ__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010-2011ѧ�����ʡ����5��ģ�⣨���ۣ���ѧ���� ���ͣ�ѡ����
ij�о�С���������ͼ��ʾ��ѭ��ϵͳ���������ܽ����ԴΣ����ij�����ʣ���������ĵ�����̫���ܹ����ṩ���й�������ȷ���� �� ��
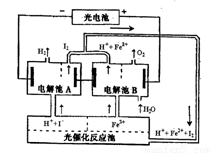
A����Ƹ�ѭ��ϵͳ��Ŀ������ȡI2
B������A�����ӷ�Ӧ����ʽ��
H2+I2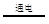 2H++2I-
2H++2I-
C�������Ӧ�������ӷ�Ӧ����ʽΪ��
2Fe2++I2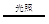 2Fe3++2I-
2Fe3++2I-
D����ϵͳ�е�Fe3+��H2O��I-����ѭ��ʹ�õ�����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com