
| A. | CH3COOH | B. | NaCl | C. | HCl | D. | Na2CO3 |
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
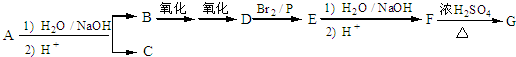
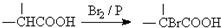
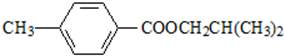 .
. ,该反应属于取代反应(或酯化反应) (填反应类型).
,该反应属于取代反应(或酯化反应) (填反应类型).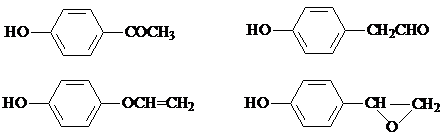 .
.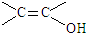 )结构.
)结构.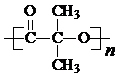 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
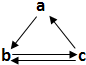 下表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是( )
下表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是( )| 选项 | a | b | c |
| A | S | SO3 | H2SO4 |
| B | Fe | FeCl2 | FeCl3 |
| C | HNO3 | NO | NO2 |
| D | CH2=CH2 | C2H5Br | C2H5OH |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 容器 | 起始各物质的物质的量/mol | 达到平衡时体系 能量的变化 | |||
| SO2 | O2 | SO3 | Ar | ||
| 甲 | 2 | 1 | 0 | 0 | 放出热量:Q1 |
| 乙 | 1.8 | 0.9 | 0.2 | 0 | 放出热量:Q2 |
| 丙 | 1.8 | 0.9 | 0.2 | 0.1 | 放出热量:Q3 |
| A. | Q1=Q2=Q3 | |
| B. | 达到平衡时,丙容器中SO2的体积分数最大 | |
| C. | 甲、乙、丙3个容器中反应的平衡常数不相等 | |
| D. | 若在上述条件下反应生成2molSO3(s)的放热大于197kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
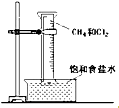 按要求书写:
按要求书写: ;-CH3
;-CH3

 系统命名法的名称3,3-二甲基-5-乙基庚烷
系统命名法的名称3,3-二甲基-5-乙基庚烷查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 海水密度(g/ml) | CaSO4 | NaCl | MgCl2 | MgSO4 | NaBr |
| 1.13 | 0.56 | ||||
| 1.20 | 0.91 | ||||
| 1.21 | 0.05 | 3.26 | 0.004 | 0.008 | |
| 1.22 | 0.015 | 9.65 | 0.01 | 0.04 | |
| 1.26 | 0.01 | 2.64 | 0.022 | 0.02 | 0.04 |
| 1.31 | 1.40 | 0.54 | 0.03 | 0.06 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 羟甲基(-CH2OH)和甲氧基(CH3O-) | B. | S2-和Cl- | ||
| C. | Mg2+和F- | D. | 羟基(-OH)和氢氧根(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com