
【题目】为提纯下列物质![]() 括号内为杂质
括号内为杂质![]() ,所用的除杂试剂和分离方法都正确的是( )
,所用的除杂试剂和分离方法都正确的是( )
序号 | 不纯物 | 除杂试剂 | 分离方法 |
A | 甲烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
B | 溴乙烷(Br2) | NaOH溶液 | 蒸馏 |
C | 溴苯(液溴) | 乙醇 | 分液 |
D | 乙醇(水) | 新制生石灰 | 蒸馏 |
A.AB.BC.CD.D
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增大,W与Y最外层电子数之和为X的最外层电子数的2倍,Z最外层电子数等于最内层电了数,X、Y、Z的简单离子的电子层结构相同,W的单质是空气中体积分数最大的气体。下列说法正确的是
A. Y的最高价氧化物对成水化物的酸性比W的强
B. W的气态氢化物比X的稳定
C. 离子半径的大小顺序:r(w)>r(X)>r(Y)>(Z)
D. XY2与ZY2中的化学键类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钙[Ca(NO2)2]是水泥混凝土外加剂的主要原料,某学习小组设计实验制备亚硝酸钙,实验装置如图所示(夹持装置略去)。
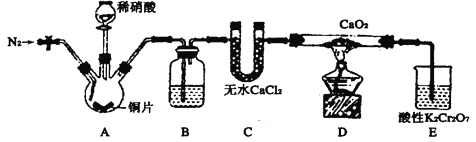
已知:2NO+CaO2=Ca(NO2)2;2NO2+CaO2=Ca(NO3)2。
请回答下列问题:
(1)向三颈烧瓶中加入稀硝酸之前,应向装置中通入一段时间的N2,原因为(用方程式表示)_________。
(2)装置B所加试剂是__________,作用是除去__________(填化学式)。
(3)装置E中,酸性K2Cr2O7溶液可将剩余的NO氧化成![]() ,溶液由橙色变为绿色(Cr3+),发生反应的离子方程式是__________。
,溶液由橙色变为绿色(Cr3+),发生反应的离子方程式是__________。
(4)已知:Ca(NO2)2溶液遇酸会产生NO气体。设计实验证明装置D中有亚硝酸钙生成:_________。
(5)工业上可用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得应用广泛的Ca(NO2)2,反应原理为Ca(OH)2+NO+NO2=Ca(NO2)2+H2O。
①若n(NO) :n(NO2)>1 :1,则会导致_______________;
②若n(NO) :n(NO2)<1 :1,则会导致________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、D、E、X均为中学化学常见物质,相互转化关系如图所示(部分物质略去)。
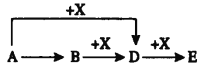
Ⅰ.若A为气体单质,气体B能使湿润红色石蕊试纸变蓝,E为红棕色气体。
(1)实验室制取B的化学方程式为___________。
(2)D和CO均是汽车尾气的主要成分,通过汽车尾气催化转化装置生成无污染气体,降低污染物排放,写出该反应的化学方程式: __________。
Ⅱ.若A是淡黄色固体,B中阴、阳离子均为10电子粒子,常温下X是无色气体。
(3)A与X反应的化学方程式:____________。
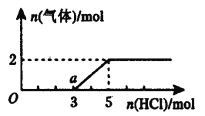
(4)将一定量的气体X通入B的溶液中,在所得溶液中逐滴加入稀盐酸至过量,产生的气体与HCl物质的量的关系如图所示(忽略气体的溶解和HCl的挥发)。a点溶液中所含溶质的化学式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关装置图的叙述中正确的是( )
A.装置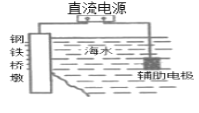 中桥墩应与电源的负极相连能被保护,该方法叫做外加电流的阴极保护法
中桥墩应与电源的负极相连能被保护,该方法叫做外加电流的阴极保护法
B.装置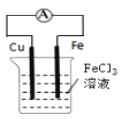 的总反应式:Cu+2Fe3+=Cu2++2Fe2+
的总反应式:Cu+2Fe3+=Cu2++2Fe2+
C.装置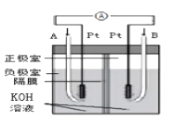 为氢氧燃料电池的工作原理,A中通入的气体是氧气
为氢氧燃料电池的工作原理,A中通入的气体是氧气
D.装置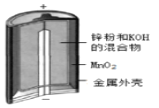 为碱性锌锰干电池,其负极的电极反应式为:Zn-2e-=Zn2+
为碱性锌锰干电池,其负极的电极反应式为:Zn-2e-=Zn2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验,能达到实验目的是( )
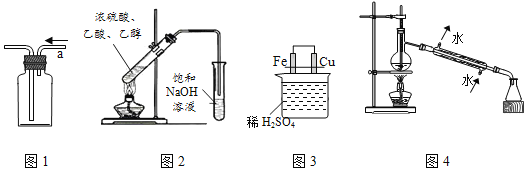
A. 用图1从a口进气可收集乙烯 B. 用图2制取并收集乙酸乙酯
C. 用图3比较Fe、Cu的金属活动性 D. 用图4进行石油的蒸馏实验
查看答案和解析>>
科目:高中化学 来源: 题型:
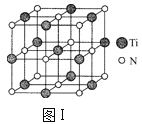
【题目】(1)以四氯化钛、碳化钙、叠氮酸盐作原料,可以生成碳氮化钛化合物。其结构是用碳原子取代氮化钛晶胞(结构如图Ⅰ)顶点的氮原子,这种碳氮化钛化合物的化学式为___。
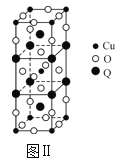
(2)图Ⅱ是由Q、Cu、O三种元素组成的一种高温超导体的晶胞结构,其中Cu为+2价,O为-2价,则Q的化合价为___价。
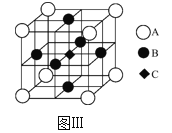
(3)一种新型阳极材料LaCrO3的晶胞如图Ⅲ所示,已知距离每个Cr原子最近的原子有6个,则图Ⅲ中___(填字母)原子代表的是Cr原子。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com