
(13分)我国是世界上发现和使用铜及铜器最早的国家之一,直到现在铜及其化合物在工农业生产中仍然有着广泛的应用。
(1)工业上可以用黄铜矿(主要成分CuFeS2)为原料冶炼铜。主要反应如下:
① 2CuFeS2+4O2=Cu2S+3SO2+2FeO ② 2Cu2S + 3O2=2SO2+2Cu2O③ Cu2S+ 2Cu2O=6Cu+ SO2
在③中被氧化与被还原元素原子的物质的量之比为 ;若由3mol CuFeS2生成3molCu,理论上消耗O2 的物质的量为 。
(2)常温下Cu2O能溶于稀硫酸,得到蓝色溶液和红色固体,可以利用该性质检验工业上冶炼铜得到的粗铜中是否含有Cu2O,写出此反应的离子方程式 。
(3)刻蚀印刷电路的废液中含有大量的CuCl2、FeCl2、FeCl3,任意排放将导致环境污染和资源的浪费, 为了使FeCl3循环利用和回收CuCl2,现设计如下生产过程:
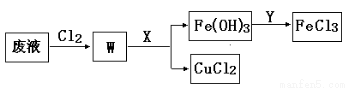
①试剂Y的名称 ;物质X最好是 (填化学式)。
②若常温下1L废液中含CuCl2、FeCl2、FeCl3的物质的量浓度均为0.5 mol· , 则加入Cl2气和物质X使溶液的pH在 范围时(设溶液体积保持不变),铁元素完全转化为Fe(OH)3,而CuCl2 不产生沉淀。( KSP [Fe(OH)3]=1.0×10—38 、 KSP [Cu(OH)2]=2.0×10—20 、 lg5=0.7)
, 则加入Cl2气和物质X使溶液的pH在 范围时(设溶液体积保持不变),铁元素完全转化为Fe(OH)3,而CuCl2 不产生沉淀。( KSP [Fe(OH)3]=1.0×10—38 、 KSP [Cu(OH)2]=2.0×10—20 、 lg5=0.7)
(13分)
(1)1﹕6 (2分), 7.5mol(3分,没单位扣1分)。
(2)Cu2O+2H+=Cu+Cu2+ +H2O (2分,没配平扣1分,化学式错0分)
(3)①盐酸或氯化氢(1分);CuO (2分)。② 3.0—4.3(3分)
【解析】
试题分析:(1) Cu2S+ 2Cu2O=6Cu+ SO2中,被氧化的元素即化合价升高的元素是S元素,被还原的元素即化合价降低的元素是Cu元素,由方程式可知,③中被氧化与被还原元素原子的物质的量之比为1:6;
由①得6CuFeS2~12O2~3Cu2S; 由②得 2Cu2S ~ 3O2~2Cu2O, 由③Cu2S~ 2Cu2O~6Cu,所以最终得关系式6CuFeS2~15O2~6Cu,若由3mol CuFeS2生成3molCu,理论上消耗O2 的物质的量为7.5mol;
(2)常温下Cu2O能溶于稀硫酸,得到蓝色溶液和红色固体,根据氧化还原反应理论,蓝色溶液为硫酸铜溶液,红色固体为单质铜,离子方程式为Cu2O+2H+=Cu+Cu2+ +H2O;
(3)①由氢氧化铁生成氯化铁,需要试剂Y是稀盐酸或氯化氢;加入X的目的是调节溶液pH,使铁离子沉淀,所以为了不引入新的杂质,X最好选择CuO;
② 加入氯气后铜离子的浓度仍是0.5mol/L,铁离子的浓度为1.0mol/L,根据所给沉淀的溶度积计算氢氧化铁完全沉淀时的c(OH-)3=1.0×10—38 /1.0×10—5mol· , 则c(OH-)=1.0×10—11mol·
, 则c(OH-)=1.0×10—11mol· , pH=3;当铜离子开始沉淀时,c(OH-)2=2.0×10—20 /0.5=4.0×10—20mol·
, pH=3;当铜离子开始沉淀时,c(OH-)2=2.0×10—20 /0.5=4.0×10—20mol· ,c(OH-)=2.0×10—10mol·
,c(OH-)=2.0×10—10mol· ,pH=4.3,所以铁元素完全转化为Fe(OH)3,而CuCl2 不产生沉淀时溶液对pH的范围是3.0—4.3。
,pH=4.3,所以铁元素完全转化为Fe(OH)3,而CuCl2 不产生沉淀时溶液对pH的范围是3.0—4.3。
考点:考查氧化还原反应的计算,试剂的选择,溶液pH的计算


科目:高中化学 来源:2013-2014河南省周口市高一下学期5月联考化学试卷(解析版) 题型:选择题
下列对“化学反应速率”的理解正确的是
A.化学反应速率表示的是化学反应进行的限度
B.化学反应速率可以用单位时间内反应物浓度的减少量来表示
C. 对于任何化学反应来说,反应速率越快,反应现象就越明显
D.化学反应速率可以是正值,也可以是负值
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省南阳市春期高一期终质量评估化学试卷(解析版) 题型:选择题
甲—辛等八种元素在周期表中的相对位置如下表。甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断不正确的是
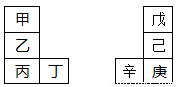
A.乙的单质在空气中燃烧生成只含离子键的化合物
B.原子半径:辛>己>戊
C.丙与庚的原子核外电子数相差13
D.最高价氧化物的水化物的碱性:丙>乙>甲
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省六市毕业班第二次联合调研检测理综化学试卷(解析版) 题型:选择题
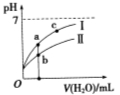
已知下表为250C时某些弱酸的电离平衡常数。下图表示常温时,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化。依据所给信息,下列说法正确的是
CH3COOH | HClO | H2CO3 |
Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.4×10-7 Ka2=4.7×10-11 |
A.相同浓度的CH3COONa和NaClO的混合溶液中,各离子浓度的大小关系是:
C(Na+)>C(ClO—)>C(CH3COO—)>C(OH—)>C(H+)
B.向NaClO溶液中通入少量二氧化碳的离子方程式为:2ClO—+CO2+H2O═2HClO+CO32—
C.a、b、c三点所示溶液中水的电离程度c>a>b
D.图像中,Ⅰ表示CH3COOH,Ⅱ表示HClO,且溶液导电性:c>b>a
查看答案和解析>>
科目:高中化学 来源:2013-2014河南师大附中高三4月份月考理综化学试卷(解析版) 题型:推断题
【化学—选修5:有机化学基础】(15分)
苯的同系物是人类最早认识的芳香族化合物,其中对二甲苯(英文名称p—xylene,缩写为PX)是化学工业的重要原料。
(1)写出PX的结构简式______________。
(2)PX可能发生的反应有_____ __、___ _____。(填反应类型,只填两种。)
(3)有机物M存在如下图所示的转化关系,其中A 是PX的一种同分异构体。
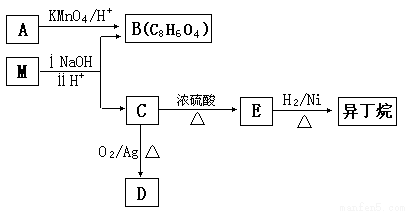
已知:M的分子式为C16H22O4,D能发生银镜反应。
①B的苯环上存在3 种不同化学环境的氢原子,则B 的结构简式是__________。
②D分子中所含的官能团是______________(填化学式)。
③M的结构简式是_______________。
(4)F是B 的一种同分异构体,具有如下特征:
a.是苯的对位二取代物;b.遇FeCl3溶液显示紫色;c.能与碳酸氢钠溶液反应。
写出F与NaHCO3溶液反应的化学方程式_____________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014河南师大附中高三4月份月考理综化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值。下列说法正确的是
A.2.24LCO2中含有的原子数为0.3NA
B.1.8g NH4+离子中含有的质子数为NA
C.C60和石墨的混合物共1.8g,含碳原子数目为0.15NA
D.0.5mol/LNaOH溶液中,含Na+离子数目为0.5NA
查看答案和解析>>
科目:高中化学 来源:2013-2014河北省邯郸市高二7月调研考试化学试卷(解析版) 题型:选择题
下图所示的电解池I和II中,a、b、c和d均为Pt电极。电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b<d。符合上述实验结果的盐溶液是

选项 | X | Y |
A. | MgSO4 | CuSO4 |
B. | AgNO3 | Pb(NO3)2 |
C. | FeSO4 | Al2 (SO4)3 |
D. | CuSO4 | AgNO3 |
查看答案和解析>>
科目:高中化学 来源:2013-2014河北省高二下学期第三次月考化学试卷(解析版) 题型:填空题
(13分)已知酮类化合物可以和氰化氢发生加成反应。
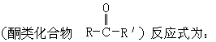

上述反应的生成物在一定条件下可发生水解生成羧酸:
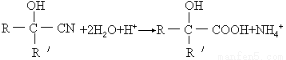
依上述反应规律,按照提示的反应类型,写出用丙酮为原料经5步合成聚甲基丙烯酸甲酯的反应方程式,并注明所缺的反应类型(其它必要的原料可任意选择):
(1)_________,______________________________________________;
(2)水 解,______________________________________________;。
(3)_________,______________________________________________;
(4)消 去,______________________________________________;
(5)_________,______________________________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014河北省高一下学期第三次月考化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.增大压强,活化分子数增加,化学反应速率一定增大
B.升高温度,活化分子百分数增加,化学反应速率一定增大
C.活化分子间所发生的分子间的碰撞为有效碰撞
D.增大反应物浓度,使活化分子百分数增加,化学反应速率增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com