

| 物质 | Fe(OH)3 | Cu(OH)2 | Ca(OH)2 | Mn(OH)2 | CuS | CaS | MnS | MnCO3 |
| pKsp | 37.4 | 19.32 | 5.26 | 12.7 | 35.2 | 5.86 | 12.6 | 10.7 |
分析 (1)依据铝热反应原理可知:高温条件下,Al和Mn3O4发生置换反应生成Mn和氧化铝;
(2)软锰矿还原浸出得到硫酸锰溶液,说明浸取液为稀硫酸,同时溶液中还含有Ca2+、Fe3+、Cu2+等杂质,调节溶液的pH,Fe(OH)3pKap为37.4与其它离子相比最大,调节pH可以将 Fe(OH)3沉淀下来,向滤液中加入硫化铵,CuSpKap为35.2,可以将铜离子形成硫化物沉淀下来,再加入MnF2,形成CaF2沉淀,除去Ca2+,最后对得到的含有锰离子的盐电解,可以得到金属锰;
(3)锰离子和碳酸氢根离子反应生成碳酸锰沉淀、水和二氧化碳气体,根据反应物和生成物书写方程式;K=$\frac{c(C{O}_{3}{\;}^{2}{\;}^{-})}{{c}^{2}(OH{\;}^{-})}$=$\frac{\frac{{K}_{sp}(MnC{O}_{3})}{c(M{n}^{2}{\;}^{+})}}{\frac{{K}_{sp}[Mn(OH)_{{\;}_{2}}]}{c(Mn{{\;}^{2}}^{+})}}$;
解答 解:(1)高温条件下,Al和Mn3O4发生置换反应生成Mn和氧化铝,化学方程式:8Al+3Mn3O4$\frac{\underline{\;高温\;}}{\;}$4Al2O3+9Mn,
故答案为:8Al+3Mn3O4$\frac{\underline{\;高温\;}}{\;}$4Al2O3+9Mn;
(2)①软锰矿还原浸出的反应为:12MnO2+C6H12O6+12H2SO4═12MnSO4+6CO2↑+18H2O,反应中C6H12O6中的碳元素化合价升高,所以C6H12O6做还原剂;
提高温度能够加快反应速率;
故答案为:C6H12O6;升高反应温度;
②软锰矿还原浸出的反应为:12MnO2+C6H12O6+12H2SO4=12MnSO4+6CO2↑+18H2O,溶液呈强酸性,还原浸出液中含有Mn2+、Ca2+、Fe3+、Cu2+,此时未形成沉淀,Kp为电离平衡常数,pKp=-1gKp,pKp越大,沉淀溶解平衡常数越小,滤液1为形成Fe(OH)3沉淀,pKp=-1gKp=37.4,Kp=10-37.4,Kp=c(Fe3+)×c3(OH-)=10-37.4,c(OH-)≈10-10,c(H+)=1×10-4mol/L,pH=4,所以滤液1的pH大于MnSO4浸出液的pH=4才能形成氢氧化铁沉淀,
故答案为:>;
③CaF2难溶于水,滤液2为Mn2+、Ca2+、NH4+、SO42-,加入MnF2的目的除去形成CaF2沉淀,除去Ca2+,故答案为:Ca2+;
(3)锰离子和碳酸氢根离子反应生成碳酸锰沉淀、水和二氧化碳气体,离子方程式为Mn2++2HCO3-=MnCO3↓+H2O+CO2↑;由MnCO3(s)+2OH-(aq)?Mn(OH)2(s)+CO32-(aq)可知,K=$\frac{c(C{O}_{3}{\;}^{2}{\;}^{-})}{{c}^{2}(OH{\;}^{-})}$=$\frac{\frac{{K}_{sp}(MnC{O}_{3})}{c(M{n}^{2}{\;}^{+})}}{\frac{{K}_{sp}[Mn(OH)_{{\;}_{2}}]}{c(Mn{{\;}^{2}}^{+})}}$=$\frac{1{0}^{-10.7}}{10{\;}^{-12.7}}$=100.
故答案为:Mn2++2HCO3-=MnCO3↓+H2O+CO2↑;100.
点评 本题为工艺流程题,涉及物质的提纯与分离、离子方程式的书写、有关kSP、K的计算、氧化还原反应基本概念,熟悉相关理论是解题关键,题目难度中等.


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 全部 | B. | ①②⑤ | C. | ② | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 分别表示N2、H2、NH3和固体催化剂,则在固体催化剂表面合成氨的过程可用下图表示:
分别表示N2、H2、NH3和固体催化剂,则在固体催化剂表面合成氨的过程可用下图表示: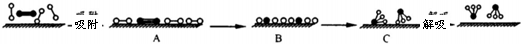
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 青蒿素易溶于水和酒精 | |
| B. | 青蒿素中含多个环状结构,其中有一个六元碳环 | |
| C. | 青蒿素中含过氧键,过氧键属于极性共价键 | |
| D. | 青蒿素和纤维素都属于高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
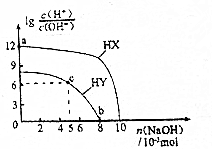
| A. | HX的酸性弱于HY | |
| B. | a点由水电离出的c(H+)=10-12mol•L-1 | |
| C. | c点溶液中:c(Y-)>c(HY) | |
| D. | b点时酸碱恰好完全中和 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 17.92L | B. | 22.4L | C. | 8.96L | D. | 11.2L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com