
【题目】硫单质及其化合物在工农业生产中有着重要的应用,请回答下列问题: 
(1)一种煤炭脱硫技术可以把硫元素以CaSO4的形成固定下来,但产生的CO又会与CaSO4发生化学反应,相关的热化学方程式如下: ①CaSO4(s)+CO(g)CaO(s)+SO2(g)+CO2(g)△=+210.5kJmol﹣1
② ![]() CaSO4(s)+CO(g)
CaSO4(s)+CO(g) ![]() CaS(s)+CO2(g)△=﹣47.3kJmol﹣1
CaS(s)+CO2(g)△=﹣47.3kJmol﹣1
反应:CaO(s)+3CO(g)+SO2(g)CaS(s)+3CO2(g)△H=kJmol﹣1
平衡常数K的表达式为 .
(2)图1为密闭容器中H2S气体分解生产H2和S2(g)的平衡转化率与温度、压强的关系. 图1中压强P1、P2、P3的大小顺序为 , 理由是 , 该反应平衡常数的大小关系为K(T1)K(T2)(“>”“=”或“<”),理由是
(3)在一定条件下,二氧化硫和氧气发生反应:2SO2(g)+O2(g)2SO3△H<0 ①600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图2,反应处于平衡状态的时间段所示
②据图2判断,反应进行至20min时,曲线发生变化的原因是(用文字表达):10min到15min的曲线变化的原因可能是(填写编号)
A.加了催化剂
B.缩小容器体积
C.降低温度
D.增加SO2的物质的量
(4)烟气中SO2可用某浓度NaOH溶液吸收得到Na2SO3和NaHSO3混合溶液,且所得溶液呈中性,该溶液中c(Na+)=(用含硫微粒浓度的代数式表示)
【答案】
(1)﹣399.7;![]()
(2)P1<P2<P3;反应前后气体体积增大,增大压强,平衡逆向进行;<;反应是吸热反应,升温,平衡正向进行,平衡常数增大
(3)15﹣20min和25﹣30min;增大氧气的浓度;AB
(4)2c(SO32﹣)+c(HSO3﹣)
【解析】解:(1)(1)①CaSO4(s)+CO(g)CaO(s)+SO2(g)+CO2(g)△=+210.5kJmol﹣1② ![]() CaSO4(s)+CO(g)
CaSO4(s)+CO(g) ![]() CaS(s)+CO2(g)△=﹣47.3kJmol﹣1
CaS(s)+CO2(g)△=﹣47.3kJmol﹣1
结合盖斯定律可知,②×4﹣①得到CaO(s)+3CO(g)+SO2(g)CaS(s)+3CO2(g),
则△H=(﹣47.3kJmol﹣1)×4﹣(+210.5kJmol﹣1)=﹣399.7kJ/mol;
K= ![]() ,
,
所以答案是:﹣399.7; ![]() ;(2)图1中压强P1、P2、P3的大小顺序为P1<P2<P3;理由是反应前后气体体积增大,增大压强,平衡逆向进行;由图可知,温度越高,转化率越大,则该反应为吸热反应,升高温度,K增大,即K(T1)<K(T2),
;(2)图1中压强P1、P2、P3的大小顺序为P1<P2<P3;理由是反应前后气体体积增大,增大压强,平衡逆向进行;由图可知,温度越高,转化率越大,则该反应为吸热反应,升高温度,K增大,即K(T1)<K(T2),
所以答案是:P1<P2<P3;反应前后气体体积增大,增大压强,平衡逆向进行;<;反应是吸热反应,升温,平衡正向进行,平衡常数增大;(3)①平衡时物质的量不变,则反应处于平衡状态的15﹣20min和25﹣30min时间段所示,所以答案是:15﹣20min和25﹣30min;
②反应进行至20min时,氧气的浓度瞬间增大,则曲线发生变化的原因是增大氧气的浓度;10min到15min的曲线斜率增大,反应速率加快,反应物浓度减小,加催化剂、缩小体积均符合,C中降低温度,反应速率减小,D中二氧化硫浓度增大,故选AB,
所以答案是:增大氧气的浓度;AB;(4)得到Na2SO3和NaHSO3混合溶液,且所得溶液呈中性,存在c(H+)=c(OH﹣),c(Na+)+c(H+)=c(OH﹣)+2c(SO32﹣)+c(HSO3﹣),则c(Na+)=2c(SO32﹣)+c(HSO3﹣),所以答案是:2c(SO32﹣)+c(HSO3﹣).
【考点精析】认真审题,首先需要了解化学平衡状态本质及特征(化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效)),还要掌握化学平衡的计算(反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%)的相关知识才是答题的关键.


科目:高中化学 来源: 题型:
【题目】关于O2与O3气体,下列比值一定为2:3的是( )
A.若两种气体所占体积相同,两种气体的质量之比
B.若温度和压强相同,两种气体的密度之比
C.若两种气体原子数相同,两种气体的质子数之比
D.若两种气体的质量相同,两种气体的分子数之比
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A+B3C+5D反应中,表示该反应速率最快的是( )
A.v(A)═0.5 mol/(Ls)
B.v(B)═0.3mol/(Ls)
C.v(C)═0.8 mol/(Ls)
D.v(D)═1mol/(Ls)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,A处通入Cl2 , 关闭B阀时,C处的红布看不到明显现象;当打开B阀后,C处红布条逐渐褪色.则D瓶中装的是( ) 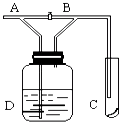
A.浓盐酸
B.NaOH溶液
C.H2O
D.饱和NaCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为原子序数依次增大的五种元素,A的一种同位素可用于考古中测定生物的死亡年代; B与A同周期,其s能级电子数比p能级电子数多;C原子的最外层电子数是次外层的3倍;D与B同主族;E的原子序数为29.回答下列问题:
(1)五种元素中第一电离能最大的是(填元素符号),其中D原子价电子排布图为 .
(2)元素B的简单气态氢化物的沸点填“高于”或“低于”)元素A的简单气态氢化物的沸点,其主要原因是; A的简单气态氢化物中心原子的杂化轨道类型为 .
(3)BC3﹣的立体构型为 , 与其互为等电子体的分子是(写化学式).
(4)EC在加热条件下容易转化为E2C,从原子结构的角度解释原因;E原子的外围电子排布式为 , E晶体的堆积方式为(填序号) ①简单立方堆积 ②体心立方堆积
③六方最密堆积 ④面心立方最密堆积
(5)硼与D可形成一种耐磨材料F,其结构与金刚石相似(如图),可由硼的三溴化物和D的三溴化物于高温下在氢气的氛围中合成.写出合成F的化学方程式: . F的晶胞边长为a pm,则该晶体密度的表达式为gcm﹣3 . (用含a、NA的式子表示,不必化简). 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)是一种新型无机非金属材料.为了分析某AlN样品(样品中的杂质不与氢氧化钠溶液反应)中A1N的含量,某实验小组设计了如下两种实验方案.
已知:AlN+NaOH+H2O=NaAlO2+NH3↑
【方案l】取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去).
(1)如图C装置中球形干燥管的作用是 .
(2)完成以下实验步骤:组装好实验装置后,首先 ,
再加入实验药品.接下来关闭K1 , 打开K2 , 打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体.打开K1 , 通入氮气一段时间,测定C装置反应前后的质量变化.通入氮气的目的是 .
(3)装置B中试剂可以为(选正确序号填空).
①浓硫酸 ②碱石灰 ③P2O5④还原铁粉
若去掉装置B,则导致测定结果 (填“偏高”、“偏低”或“无影响”).由于上述装置还存在缺陷,导致测定结果偏高,请提出改进意见 .
(4)【方案2】按以下步骤测定样品中A1N的纯度:
步骤②生成沉淀的离子方程式为 .
步骤③的操作是 . A1N的纯度是 (用m1、m2表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋是一个丰富的资宝库,通过海水的综合利用可获得许多物质供人类使用.
(1)海水中盐的开发利用:
①海水制盐目前以盐田法为t,建盐田必须选在远离江河入海口,多风少雨,潮汐落差大且又平坦空旷的海滩.所建盐田分为贮水池、蒸发池和池.
②目前工业上采用比较先进的离子交换膜电解槽法进行氯碱工业生产,在电解槽中阳离子交换膜只允许阳离子通过,阻止阴离子和气体通过,请说明氯碱生产中阳离子交换膜的作用:(写一点即可).
(2)电渗析法是近年发展起的一种较好的海水淡化技术,其原理如图所示.其中具有选择性的阴离子交换膜和阳离子交换膜相间排列.请回答下面的问题:
①海水不能直接通人到阴极室中,理由是 .
②A口排出的是(填“淡水”或“浓水”)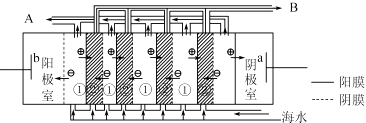
(3)用苦卤(含Na+、K+、Mg2+、Cl﹣、Br﹣等离子)可提取溴,其生产流程如下 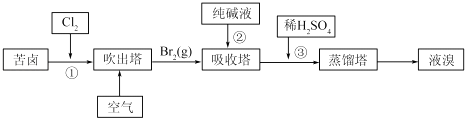
①若吸收塔中的溶液含BrO3﹣ , 则吸收塔中反应的离子方程式为:
②通过①氯化已获得含Br2的溶液.为何还需经过吹出、吸收、酸化重新获得含Br2的溶液? .
③向蒸馏塔中通入水蒸气加热.控制温度在90℃左右进行蒸馏的原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化锌(ZnS)是一种重要的化工原料,难溶于水,可由炼锌的废渣锌灰制取t其工艺流程如图1所示. 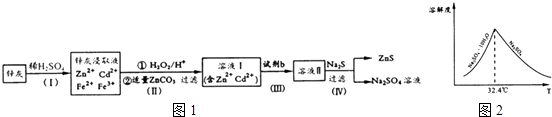
(1)为提高锌灰的浸取率,可采用的方法是(填序号).
①研磨 ②多次浸取 ③升高温度 ④加压 ⑤搅拌
(2)步骤Ⅱ所得滤渣中的物质是(写化学式).
(3)步骤Ⅲ中可得Cd单质,为避免引入新的杂质,试剂b应为
(4)步骤Ⅳ还可以回收Na2SO4来制取Na2S.
①检验ZnS固体是否洗涤干净的方法是 ,
②Na2S可由等物质的量的Na2S04和CH4在高温、催化剂条件下制取.化学反应方程式为
③已知Na2SO4 . 10H2O及Na2SO4的溶解度随温度变化曲线如图2.从滤液中得到Na2SO4.10H2O的操作方法是
(5)若步骤Ⅱ加入的ZnCO3为b mol,步骤Ⅲ所得Cd为d mol,最后得到VL,物质的量浓度为c mol/L的Na2SO4溶液.则理论上所用锌灰中含有锌元素的质量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组利用含硫酸铜的工业废液制备硫酸铵,流程如下: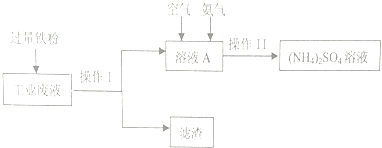
(1)操作Ⅰ的名称为 , 滤渣的成分为 .
(2)工业废液中加入过量铁粉所发生反应的离子方程式为 .
(3)操作Ⅱ得到的(NH4)2SO4溶液进行蒸发浓缩,需要的仪器除了酒精灯、铁架台、蒸发皿外,还需要 .
(4)如图溶液A中发生反应的离子方程式为4Fe2++O2+8NH3+10H2O=8NH4++4Fe(OH)3↓该反应是否为氧化还原反应(填“是”或“否”).
(5)检验(NH4)2SO4溶液中含有SO ![]() 的方法为 .
的方法为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com