
已知某种气态化石燃料含有碳和氢两种元素。为了
测定这种燃料中碳和氢两种元素的质量分数,可将气态燃料放入足量的氧气中燃烧,并使产生的气体全部通入如图所示的装置,得到如表所列的实验数据(U形管中干燥剂只吸收水蒸气且假设产生的气体完全被吸收)。
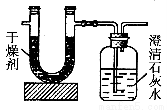
| 实验前 | 实验后 |
(干燥剂+U形管)的质量 | 101.1g | 102.9g |
(石灰水+广口瓶)的质量 | 312.0g | 314.2g |
根据实验数据求:
(1)实验完毕后,生成物中水的质量为________g。假设广口瓶里生成一种正盐,其质量为________g。
(2)生成的水中氢元素的质量为________g。
(3)生成的CO2中碳元素的质量为________g。
(4)气态化石燃料中碳元素与氢元素的质量比为________。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014年高一化学人教版必修二 3-4-1糖类练习卷(解析版) 题型:选择题
英国《独立报》公布“英国科学家研究结果表明:高纤维素食物可降低患乳腺癌风险”。高纤维素食物富含维生素、锌和其他微量营养素,可以平衡体内胰岛素水平并调节雌激素。下列关于高纤维素的叙述不正确的是( )
A.高纤维素中的“高”指食物中所含纤维素的质量分数大
B.纤维素与淀粉通式都是(C6H10O5)n,它们互为同分异构体
C.纤维素与淀粉都属于糖类且都是高分子化合物
D.纤维素与淀粉都能水解,水解的最终产物相同,且产物都能发生银镜反应
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 3-2-2苯练习卷(解析版) 题型:实验题
苯和溴取代反应的实验装置如图所示,其中A为由具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑粉。填写下列空白:
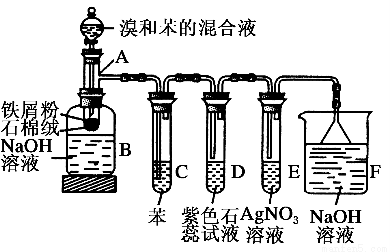
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒内就发生反应。写出A中所发生反应的化学方程式(有机物写结构简式):____________________________。
(2)B中NaOH溶液的作用是____________________。
(3)试管C中苯的作用是_______________________。
反应开始后,观察D和E两试管,看到的现象为____________________________,此现象可以验证苯和液溴的反应为____________(填反应类型)。
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 3-2-1乙烯练习卷(解析版) 题型:选择题
一种气态烷烃和一种气态烯烃组成的混合物共10 g,混合气体的密度是相同状况下氢气密度的12.5倍,该混合气体通过Br2水时,Br2水的质量增加8.4 g,则组成该混合气体的可能是( )
A.甲烷、乙烯 B.丙烷、乙烯 C.乙烷、丙烯 D.甲烷、丙烯
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 3-2-1乙烯练习卷(解析版) 题型:选择题
下列有关化学用语能确定为丙烯的是( )
A.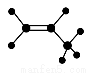
B.C3H6
C.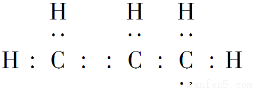
D.CH2= CH—CH3
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 3-1-2烷烃练习卷(解析版) 题型:选择题
燃烧0.1mol两种气态烃的混合物,生成3.58L CO2(标准状况)和3.6g H2O,则混合气体中( )
A.一定有甲烷 B.一定有乙烷
C.一定无甲烷 D.一定有丙烷
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 3-1-2烷烃练习卷(解析版) 题型:选择题
在1.013×105Pa下,测得的某些烷烃的沸点见下表。据表分析,下列选项正确的是( )
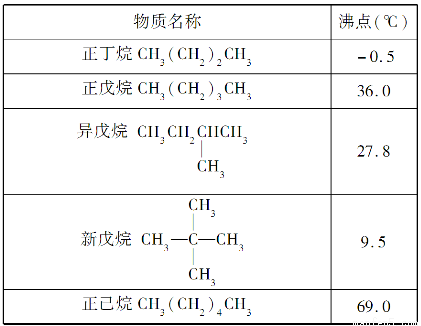
A.在标准状况时,新戊烷是气体
B.在1.013×105Pa、20℃时,C5H12都是液体
C.烷烃随碳原子数的增加,沸点降低
D.C5H12随支链的增加,沸点降低
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 3-1-1甲烷练习卷(解析版) 题型:选择题
1mol甲烷和Cl2发生取代反应,待反应完成后,测得四种取代物的物质的量相等,则消耗Cl2的物质的量为( )
A.0.5mol B.2mol C.2.5mol D.4mol
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 2-2-2发展中的化学电源练习卷(解析版) 题型:选择题
碱性电池具有容量大,放电电流大的特点,因而得到广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:
Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s)
下列说法错误的是( )
A.电池工作时,锌失去电子
B.电池正极的电极反应式为2MnO2(s)+H2O(l)+2e-=
Mn2O3(s)+2OH-(aq)
C.电池工作时,电子由正极通过外电路流向负极
D.外电路中每通过0.2 mol电子,锌的质量理论上减少6.5 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com