
 .
. .
.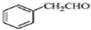 为原料制备
为原料制备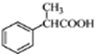 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:分析 (1)由非诺洛芬的结构可知,含有的含氧官能团为醚键、羧基;
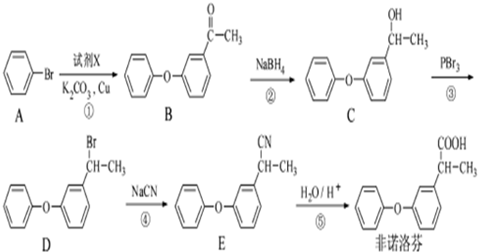
(2)反应①中加入的试剂X的分子式为C8H8O2,对比A、B的结构可知该反应为取代反应,可以判断X的结构简式;
(3)①为取代反应,②中羰基转化为羟基,属于还原反应,③中羟基被-Br取代,④中-Br被-CN取代,⑤中-CN转化为-COOH;
(4)B的一种同分异构体满足下列条件:Ⅰ.能发生银镜反应,其水解产物之一能与FeCl3溶液发生显色反应,含有甲酸与酚形成的酯基,Ⅱ.分子中有6种不同化学环境的氢,且分子中含有两个苯环,可以是2个苯环直接相连,分别含有甲基、-OOCH且与苯环均为对为物质;
(5)苯乙醛和NaBH4发生还原反应生成苯乙醇,苯乙醇发生消去反应生成苯乙烯,苯乙烯发生加成反应生成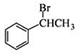 ,
, 和NaCN发生取代反应,然后水解反应生成
和NaCN发生取代反应,然后水解反应生成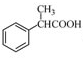 .
.
解答 解:(1)由非诺洛芬的结构可知,含有的含氧官能团为醚键、羧基,故答案为:醚键;羧基;
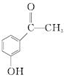
(2)反应①中加入的试剂X的分子式为C8H8O2,对比A、B的结构可知该反应为取代反应,可以判断X的结构简式为: ,
,
故答案为: ;
;
(3)①为取代反应,②中羰基转化为羟基,属于还原反应,③中羟基被-Br取代,属于取代反应,④中-Br被-CN取代,属于取代反应,⑤中-CN转化为-COOH,属于水解反应,
故答案为:①③④;
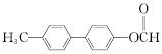
(4)B的一种同分异构体满足下列条件:Ⅰ.能发生银镜反应,其水解产物之一能与FeCl3溶液发生显色反应,含有甲酸与酚形成的酯基,Ⅱ.分子中有6种不同化学环境的氢,且分子中含有两个苯环,可以是2个苯环直接相连,分别含有甲基、-OOCH且与苯环均为对为物质,符合条件的同分异构体为: ,
,
故答案为: ;
;
(5)苯乙醛和NaBH4发生还原反应生成苯乙醇,苯乙醇发生消去反应生成苯乙烯,苯乙烯发生加成反应生成 ,
, 和NaCN发生取代反应,然后水解反应生成
和NaCN发生取代反应,然后水解反应生成 ,合成路线流程图为
,合成路线流程图为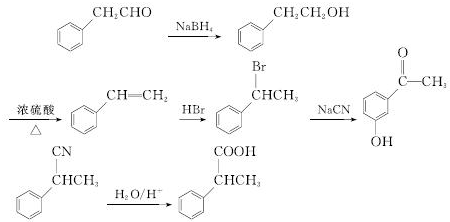 ,
,
故答案为: .
.
点评 本题考查有机物的合成与推断、限制条件同分异构体书写、官能团结构、有机反应类型等,熟练掌握官能团的性质与转化,侧重考查学生分析推理能力、自学能力与迁移运用能力,题目难度中等.


 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:选择题
| A. | 江河入海口三角洲的形成通常与胶体的性质有关 | |
| B. | 明矾净水过程中涉及化学变化 | |
| C. | Fe(OH)3胶体与食盐溶液混合将产生聚沉观象 | |
| D. | 沸水中滴加适量饱和FeCl3溶液,可形成带正电荷的胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
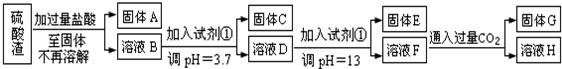
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Ag+、NO3-、Cl- | B. | K+、Ba2+、Cl-、CO32- | ||
| C. | Na+、Fe3+、NO3-、SO42- | D. | Na+、Mg2+、OH-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇分子结构中不存在手性碳 | |
| B. | 在NH4+和[Cu(NH3)4]2+中都存在配位键 | |
| C. | SO2、SO3都是极性分子 | |
| D. | 原子晶体中原子以共价键结合,具有键能大、硬度大的特性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
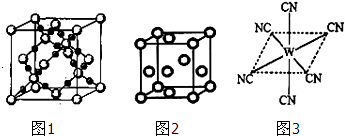
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇分子中的氢原子均可被钠置换 | |
| B. | 乙醇能与钠反应放出氢气,说明乙醉能电离出H+而表现酸性 | |
| C. | 乙醇分子羟基中的氢原子比乙烷分子中的氢原子活泼 | |
| D. | 乙醇分子羟基中的氢原子比水分子中的氢原子活泼 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com