
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
分析 ①依据构成微粒与微粒间的作用可将晶体分为金属晶体、离子晶体、分子晶体、原子晶体;
②由原子直接构成的晶体就是原子晶体,也有可能是分子晶体,如:稀有气体;
③分子晶体的堆积不一定是分子密堆积,如冰晶体中存在氢键,不是分子密堆积;
④NaF和MgF2为离子晶体,SiF4为分子晶体;
⑤在配合物(多聚型)中,为达到18e-,金属与金属间以共价键相连,亦称金属键;
⑥离子键只存在于离子晶体中;
⑦H2O的性质非常稳定,原因在于H-O键的键能较大;
⑧SO2是分子晶体,熔化时破坏的是分子间作用力;SiO2是原子晶体,熔化时破坏的是共价键.
解答 解:①依据构成微粒与微粒间的作用可将晶体分为金属晶体、离子晶体、分子晶体、原子晶体,不是依据粒子的堆积方式分类,故①错误;
②由原子直接构成的晶体就是原子晶体,也有可能是分子晶体,如:稀有气体,故②错误;
③分子晶体的堆积不一定是分子密堆积,如冰晶体中存在氢键,不是分子密堆积,故③错误;
④NaF和MgF2为离子晶体,镁离子带2个单位正电荷,离子晶体中离子所带电荷越多熔点越高,SiF4为分子晶体熔点较低,故晶体的熔点的大小关系为:MgF2>NaF>SiF4,故④正确;
⑤金属键主要在于金属晶体中,在配合物(多聚型)中,为达到18e-,金属与金属间以共价键相连,亦称金属键,故⑤错误;
⑥离子间通过离子键结合形成的晶体为离子晶体,所以离子键只存在于离子晶体中,故⑥正确;
⑦H2O的性质非常稳定,原因在于H-O键的键能较大,与氢键无关,故⑦错误;
⑧SO2是分子晶体,熔化时破坏的是分子间作用力;SiO2是原子晶体,熔化时破坏的是共价键,故⑧正确,
故选A.
点评 本题考查四种晶体类型与结构、性质等,侧重于基础知识的考查,题目难度不大,注意基础知识的掌握与晶体中的特殊性.


科目:高中化学 来源: 题型:选择题
| 混合物 | 试剂 | 分离方法 | |
| A | 苯(苯酚) | 溴水 | 过滤 |
| B | 乙 酸乙酯(乙酸) | NaOH溶液 | 蒸馏 |
| C | 乙醇(乙酸) | 无 | 分液 |
| D | 甲烷(乙烯) | 溴水 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
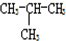
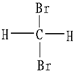 和
和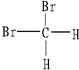
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
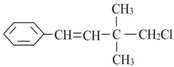 ,关于该有机物,下列叙述不正确的是( )
,关于该有机物,下列叙述不正确的是( )| A. | 所有碳原子不可能在同一平面上 | |
| B. | 属于卤代烃 | |
| C. | 分子式为C12H15Cl | |
| D. | 能发生加成反应、取代反应、加聚反应、消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属元素与非金属元素能形成共价化合物 | |
| B. | 只有在原子中,质子数与核外电子数相等 | |
| C. | 目前使用的元素周期表中,最长的周期含有36种元素 | |
| D. | 氧和臭氧互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇和甲醇 | B. | 邻羟基苯甲醛与对羟基苯甲醛 | ||
| C. | 对羟基苯甲酸与邻羟基苯甲酸 | D. | H2O和H2S |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 乙醇 | 溴乙烷 | 正丁醇 | 1-溴丁烷 | |
| 密度/g•cm-3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
| 沸点/℃ | 78.5 | 38.4 | 117.2 | 101.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
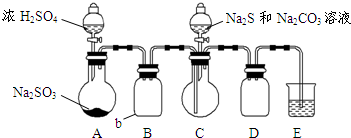 硫代硫酸钠是一种重要的化工产品.某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3•5H2O).
硫代硫酸钠是一种重要的化工产品.某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3•5H2O).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com