
【题目】(1)对于下列反应:2SO2(g)+ O2(g)![]() 2SO3(g) , 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,用O2浓度变化来表示的化学反应速率为____________。如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L·min),那么2min时SO2的浓度为_____________。
2SO3(g) , 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,用O2浓度变化来表示的化学反应速率为____________。如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L·min),那么2min时SO2的浓度为_____________。
(2)下图表示在密闭容器中反应:2SO2+O2 ![]() 2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a-b过程中改变的条件可能是 ;b-c过程中改变的条件可能是 ;若在c处增大压强时,反应速度变化和达平衡情况画在c-d处,并标出V正和V逆。
2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a-b过程中改变的条件可能是 ;b-c过程中改变的条件可能是 ;若在c处增大压强时,反应速度变化和达平衡情况画在c-d处,并标出V正和V逆。

(3)以上反应达平衡后,若此时只将容器的体积扩大为原来的2倍,达新平衡后,容器内温度将____________[填“升高”、“降低”或“不变”(容器不与外界进行热交换)];达新平衡时,容器内混合气体的平均相对分子质量与原平衡相比_____________(填“增大”、“减小”或“相等”)。
【答案】(1)1mol/(L·min);2mol/L
(2)升温;减小SO3浓度;

(3)降低;减小
【解析】
试题分析:2min内SO2的浓度由6 mol/L下降为2 mol/L,![]() mol/(L·min);根据
mol/(L·min);根据![]() ,用O2浓度变化来表示的化学反应速率为1mol/(L·min);v(O2)= 0.5mol/(L·min),2min内O2的浓度的变化为1mol/L,2min内SO2的浓度的变化为2mol/L,如果开始时SO2浓度为4mol/L,2min时SO2的浓度为2mol/L;(2)a-b过程中正逆反应速率均增大,平衡逆向移动,改变的条件可能是升高温度;b-c过程中逆反应速率突然变小,正反应速率逐渐变小,改变的条件可能是减小 SO3 浓度;若在c处增大压强时,正逆反应速率均增大,平衡正向移动,反应速度变化和达平衡时的图像是
,用O2浓度变化来表示的化学反应速率为1mol/(L·min);v(O2)= 0.5mol/(L·min),2min内O2的浓度的变化为1mol/L,2min内SO2的浓度的变化为2mol/L,如果开始时SO2浓度为4mol/L,2min时SO2的浓度为2mol/L;(2)a-b过程中正逆反应速率均增大,平衡逆向移动,改变的条件可能是升高温度;b-c过程中逆反应速率突然变小,正反应速率逐渐变小,改变的条件可能是减小 SO3 浓度;若在c处增大压强时,正逆反应速率均增大,平衡正向移动,反应速度变化和达平衡时的图像是

(3)以上反应达平衡后,若此时只将容器的体积扩大为原来的2倍,平衡逆向移动,反应吸热,达新平衡后,容器内温度将降低;平衡逆向移动,体系物质的量增大,根据![]() ,容器内混合气体的平均相对分子质量与原平衡相比减小。
,容器内混合气体的平均相对分子质量与原平衡相比减小。


 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:
【题目】下列关于化学反应类型的叙述中,正确的是
A.凡是生成盐和水的反应都是中和反应
B.复分解反应一定没有单质参加
C.生成一种单质和一种化合物的反应一定是置换反应
D.分解反应的生成物一定有单质]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,表中所列字母分别代表某一元素。根据表中所列元素回答下列问题:

(1)元素d在周期表中的位置是_____________,h与f原子序数相差______________。
(2)b、c、f的简单离子半径最小的是___________(填离子符号),原子半径最小的是______(填化学式)。
(3)表中第三周期元素的非金属性最强是_________(用元素符号表示), e、f、g三种元素的气态氢化物最不稳定的是__________(用化学式表示)。
(4)g元素与b元素的最高价氧化物对应水化物反应的化学方程式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取一定物质的量浓度的NaOH溶液100mL,然后向其通入一定量的CO2气体,得到溶液A,向A中逐滴缓慢加入0.1mol/L的HCl溶液,产生的CO2气体体积(标准状况)与所加HCl溶液的体积之间关系如图所示,通过计算回答:
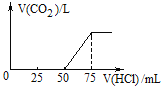
(1)A溶液中的溶质为_________(化学式),其物质的量之比是_______。
(2)通入CO2气体体积__________________(标准状况)。
(3)NaOH溶液的物质的量浓度______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为检验浓硫酸与木炭在加热条件下反应产生SO2和CO2气体,设计了如图11所示实验装置,a、b、c为止水夹,B是用于储气的气囊,D中放有用I2和淀粉的蓝色溶液浸湿的脱脂棉。

请回答下列问题:
(1)实验前欲检查装置A的气密性,可以采取的操作是_______________。
(2)此实验成败的关键在于控制反应产生气体的速率不能过快,由此设计了虚框部分的装置,则正确的操作顺序是______________(用操作编号填写);
①向A装置中加入浓硫酸,加热,使A中产生的气体进入气囊B,当气囊中充入一定量气体时,停止加热;
②待装置A冷却,且气囊B的体积不再变化后,关闭止水夹a,打开止水夹b,慢慢挤压气囊,使气囊B中气体慢慢进入装置C中,待达到实验目的后,关闭止水夹b;
③打开止水夹a和c,关闭止水夹b;
(3)实验时,装置C中的现象为___________________________;
(4)当D中产生____________现象时,可以说明使E中澄清石灰水变浑的是CO2,而不是SO2;
A.进气口一端脱脂棉蓝色变浅,出气口一端脱脂棉蓝色不变
B.脱脂棉上蓝色均变浅
C.脱脂棉上蓝色褪去
D.脱脂棉上蓝色不变
则装置D的作用为_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列防止金属腐蚀的方法属于电化学防护的是
A. 船体表面刷漆 B. 水中的钢闸门连接电源的负极
C. 自行车链条涂油 D. 加入铬、锰、硅等制成不锈钢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作或对实验事实的叙述正确的是
A. 用湿润的pH试纸测定稀盐酸的pH
B. 配制FeSO4溶液时,需加入少量铁粉和稀硫酸
C. 用碱式滴定管量取 20.00 mL 0.1 mol·L-1 KMnO4溶液
D. 用带有玻璃塞的试剂瓶储存Na2CO3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com