
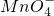 +5e-+8H+═Mn2++4H2O
+5e-+8H+═Mn2++4H2O 2H2O+O2↑; H2O2发生分解,氧元素化合价从-1价变化为0价和-2价,每2mol过氧化氢反应转移电子为2mol,若有0.5mol H2O2发生分解,则转移电子个数为0.5mol,即转移电子个数为3.01×1023;
2H2O+O2↑; H2O2发生分解,氧元素化合价从-1价变化为0价和-2价,每2mol过氧化氢反应转移电子为2mol,若有0.5mol H2O2发生分解,则转移电子个数为0.5mol,即转移电子个数为3.01×1023; 2H2O+O2↑; 3.01×1023
2H2O+O2↑; 3.01×1023

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2011年高考化学总复习30分钟限时训练:专题13 化学实验基础 题型:058
为测试一铁片中铁元素的含量,某课外活动小组提出下面两种方案并进行了实验(以下数据为多次平行实验测定结果的平均值):
方案一:将a g铁片完全溶解于过量稀硫酸中,测得生成氢气的体积为580 mL(标准状况);
方案二:将![]() g铁片完全溶解于过量稀硫酸中,将反应后得到的溶液用0.02000 mol/L的KMnO4溶液滴定,达到终点时消耗了25.00 mL KMnO?溶液.
g铁片完全溶解于过量稀硫酸中,将反应后得到的溶液用0.02000 mol/L的KMnO4溶液滴定,达到终点时消耗了25.00 mL KMnO?溶液.
请回答下列问题:
(1)配平下面的化学方程式:
□KMnO4+□FeSO4+□H2SO4 □Fe2(SO4)3+□MnSO4+□K2SO4+□H2O
□Fe2(SO4)3+□MnSO4+□K2SO4+□H2O
(2)在滴定实验中不能选择________式滴定管,理由是________;
(3)根据方案一和方案二测定的结果计算,铁片中铁的质量分数依次为________和________;(铁的相对原子质量以55计算)
(4)若排除实验仪器和操作的影响因素,试对上述两种方案测定结果的准确性做出判断和分析.
①方案一________(填“准确”“不准确”“不一定准确”),理由是________;
②方案二________(填“准确”“不准确”“不一定准确”),理由是________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com