
NA“ś±ķ°¢·ü¼ÓµĀ ĀŽ³£ŹżµÄÖµ”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
ĀŽ³£ŹżµÄÖµ”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
A£®60g±ū“¼ÖŠ“ęŌŚµÄ¹²¼Ū¼ü×ÜŹżĪŖ10NA
B£®1L 0.1mol”¤L£1µÄNaHCO3£ČÜŅŗÖŠHCO3£ŗĶCO32£Ąė×ÓŹżÖ®ŗĶĪŖ0.1NA
C£®ÄĘŌŚæÕĘųÖŠČ¼ÉÕæÉÉś³É¶ąÖÖŃõ»ÆĪļ”£23gÄĘ³ä·ÖČ¼ÉÕŹ±×ŖŅʵē×ÓŹżĪŖ1NA
D£®235gŗĖ»„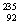 U·¢ÉśĮѱ䷓Ӧ£ŗ
U·¢ÉśĮѱ䷓Ӧ£ŗ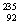 U+
U+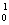 n
n
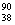 Sr+
Sr+ U+10
U+10 n¾»²śÉśµÄÖŠ×Ó(
n¾»²śÉśµÄÖŠ×Ó( n)ŹżĪŖ10NA
n)ŹżĪŖ10NA
 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻÖÓŠpH=3µÄ“×ĖįŗĶpH=3µÄĮņĖįĮ½ÖÖČÜŅŗ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®¼ÓĖ®Ļ”ŹĶ100±¶ŗóĮ½ČÜŅŗµÄpHČŌĻąĶ¬
B£®Į½ČÜŅŗÖŠ·Ö±š¼ÓČė×ćĮæµÄŠæʬ·Å³öH2µÄĢå»żĻąĶ¬
C£®“×ĖįÖŠµÄc (CH3COO”Ŗ)ŗĶĮņĖįÖŠµÄc(SO42”Ŗ) ĻąĶ¬
D£®Į½ČÜŅŗÖŠĖ®µēĄė³öµÄc(H+)=1”Į10”Ŗ11mol/L
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŹŅĪĀĻĀ£¬½«0.05mol Na2CO3¹ĢĢåČÜÓŚĖ®Åä³É100mLČÜŅŗ£¬ĻņČÜŅŗÖŠ¼ÓČėĻĀĮŠĪļÖŹ”£ÓŠ¹Ų½įĀŪÕżČ·µÄŹĒ
| ¼ÓČėµÄĪļÖŹ | ½įĀŪ | |
| A | 50mL 1mol·L£1H2SO4 | ·“Ó¦½įŹųŗó£¬c(Na+)=c(SO42£) |
| B | 0.05molCaO | ČÜŅŗÖŠ |
| C | 50mL H2O | ÓÉĖ®µēĄė³öµÄc(H+)·c(OH—)²»±ä |
| D | 0.1molNaHSO4¹ĢĢå | ·“Ó¦ĶźČ«ŗó£¬ČÜŅŗpH¼õŠ”£¬c(Na+)²»±ä |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
a£®b£®c£®dĪŖ¶ĢÖÜĘŚŌŖĖŲ£¬aµÄMµē×Ó²ćÓŠ1øöµē×Ó£¬bµÄ×īĶā²ćµē×ÓŹżĪŖÄŚ²ćµē×ÓŹżµÄ2±¶£¬cµÄ×īøß»ÆŗĻ¼ŪĪŖ×īµĶ»ÆŗĻ¼Ū¾ų¶ŌÖµµÄ3±¶£¬cÓėdĶ¬ÖÜĘŚ£¬dµÄŌ×Ó°ė¾¶Š”ÓŚc”£ĻĀĮŠŠšŹö“ķĪóµÄŹĒ
A£®dŌŖĖŲµÄ·Ē½šŹōŠŌ×īĒæ
B£®ĖüĆĒ¾ł“ęŌŚĮ½ÖÖ»ņĮ½ÖÖŅŌÉĻµÄŃõ»ÆĪļ
C£®Ö»ÓŠaÓėĘäĖūŌŖĖŲÉś³ÉµÄ»ÆŗĻĪļ¶¼ŹĒĄė×Ó»ÆŗĻĪļ
D£®b£®c£®dÓėĒāŠĪ³ÉµÄ»ÆŗĻĪļÖŠ»Æѧ¼ü¾łĪŖ¼«ŠŌ¹²¼Ū¼ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
[Ń”ŠŽ3—ĪļÖŹ½į¹¹ÓėŠŌÖŹ]
19—¢ń£Ø6·Ö£©ĻĀĮŠĪļÖŹµÄ½į¹¹»ņŠŌÖŹÓėĒā¼üĪŽ¹ŲµÄŹĒ
A£®ŅŅĆѵķŠµć B£®ŅŅ“¼ŌŚĖ®ÖŠµÄČܽā¶Č
C£®Ēā»ÆĆ¾µÄ¾§øńÄÜ D£®DNAµÄĖ«ĀŻŠż½į¹¹
19—¢ņ£Ø14·Ö£©·°£Ø23V£©ŹĒĪŅ¹śµÄ·į²śŌŖĖŲ£¬¹ć·ŗÓĆÓŚ“߻Ƽ°øÖĢś¹¤Ņµ”£
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©·°ŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆĪŖ £¬Ęä¼Ū²ćµē×ÓÅŲ¼Ķ¼ĪŖ ”£
£Ø2£©·°µÄijÖÖŃõ»ÆĪļµÄ¾§°ū½į¹¹ČēĶ¼1ĖłŹ¾”£¾§°ūÖŠŹµ¼ŹÓµÓŠµÄŅõ£®ŃōĄė×ÓøöŹż·Ö±šĪŖ £® ”£
£Ø3£©V2O5³£ÓĆ×÷SO2 ×Ŗ»ÆĪŖSO3µÄ“߻ƼĮ”£SO2 ·Ö×ÓÖŠSŌ×Ó¼Ū²ćµē×Ó¶ŌŹżŹĒ ¶Ō£¬·Ö×ÓµÄĮ¢Ģå¹¹ŠĶĪŖ £»SO3ĘųĢ¬ĪŖµ„·Ö×Ó£¬øĆ·Ö×ÓÖŠSŌ×ÓµÄŌӻƹģµĄĄąŠĶĪŖ £»SO3µÄČż¾ŪĢ廷ד½į¹¹ČēĶ¼2ĖłŹ¾£¬øĆ½į¹¹ÖŠSŌ×ÓµÄŌӻƹģµĄĄąŠĶĪŖ £»øĆ½į¹¹ÖŠS—O¼ü³¤ÓÉĮ½Ąą£¬Ņ»Ąą¼ü³¤Ō¼140pm£¬ĮķŅ»Ąą¼ü³¤Ō¼ĪŖ160pm£¬½Ļ¶ĢµÄ¼üĪŖ (ĢīĶ¼2ÖŠ×ÖÄø)£¬øĆ·Ö×ÓÖŠŗ¬ÓŠ øö¼ü”£
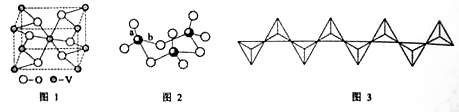
£Ø4£©V2O5 ČܽāŌŚNaOHČÜŅŗÖŠ£¬æɵƵ½·°ĖįÄĘ£ØNa3VO4£©£¬øĆŃĪŅõĄė×ÓµÄĮ¢Ģå¹¹ŠĶĪŖ £»Ņ²æÉŅŌµĆµ½Ę«·°ĖįÄĘ£¬ĘäŅõĄė×Ó³ŹČēĶ¼3ĖłŹ¾µÄĪŽĻŽĮ“ד½į¹¹£¬ŌņĘ«·°ĖįÄʵĻÆѧŹ½ĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
¼×“¼ŹĒÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬ÓÖæɳĘĪŖČ¼ĮĻ”£ĄūÓĆŗĻ³ÉĘų£ØÖ÷ŅŖ³É·ÖĪŖCO”¢CO2ŗĶH2£©ŌŚ“߻ƼĮµÄ×÷ÓĆĻĀŗĻ³É¼×“¼£¬·¢ÉśµÄÖ÷·“Ó¦ČēĻĀ£ŗ
¢ŁCO(g)+2H2(g) CH3OH(g) ”÷H1
CH3OH(g) ”÷H1
¢ŚCO2(g)+3H2(g) CH3OH£Øg£©+H2O(g) ”÷H2
CH3OH£Øg£©+H2O(g) ”÷H2
¢ŪCO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)  ”÷H3
”÷H3
»Ų“šĻĀĮŠĪŹĢā£ŗ
»Æѧ¼ü | H-H | C-O | C | H-O | C-H |
E/£ØkJ.mol-1£© | 436 | 343 | 1076 | 465 | 413 |
£Ø1£©ŅŃÖŖ·“Ó¦¢ŁÖŠµÄĻą¹ŲµÄ»Æѧ¼ü¼üÄÜŹż¾ŻČēĻĀ£ŗ
ÓÉ“Ė¼ĘĖć”÷H1= kJ.mol-1£¬ŅŃÖŖ”÷H2=-58kJ.mol-1£¬Ōņ”÷H3= kJ.mol-1
£Ø2£©·“Ó¦¢ŁµÄ»ÆŃ§Ę½ŗā³£ŹżKµÄ±ķ“ļŹ½ĪŖ £»Ķ¼1ÖŠÄÜÕżČ··“Ó³Ę½ŗā³£ŹżKĖęĪĀ¶Č±ä»Æ¹ŲĻµµÄĒśĻßĪŖ £ØĢīĒśĻß±ź¼Ē×ÖÄø£©£¬ĘäÅŠ¶ĻĄķÓÉŹĒ  ”£
ӣ
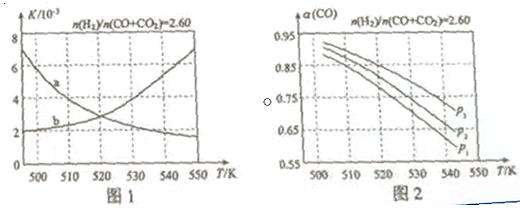
£Ø3£©ŗĻ³ÉĘųµÄ×é³Én(H2)/n(CO+CO2)=2.60Ź±ĢåĻµÖŠµÄCOĘ½ŗā×Ŗ»ÆĀŹ£Øa£©ÓėĪĀ¶ČŗĶŃ¹ĒæµÄ¹ŲĻµČēĶ¼2ĖłŹ¾”£a£ØCO£©ÖµĖęĪĀ¶ČÉżø߶ų £ØĢī”°Ōö“ó”±»ņ”°¼õŠ””±£©£¬ĘäŌŅņŹĒ ”£Ķ¼2ÖŠµÄŃ¹ĒæÓɓ󵽊”ĪŖ_____£¬ĘäÅŠ¶ĻĄķÓÉŹĒ_____”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
±ź×¼×“æöĻĀÓŠ¢Ł0.112 LĖ®””¢Ś0.5NAøöHCl·Ö×Ó
¢Ū25.6 g SO2ĘųĢå””¢Ü0.2 mol°±Ęų””¢Ż2 molŗ¤Ęų””¢Ž6.02”Į1023øö°×Į×·Ö×Ó£¬Ėłŗ¬Ō×ÓøöŹż“ӓ󵽊”µÄĖ³ŠņĪŖ______________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
NA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£Źż£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ(””””)
A£®1 mol FeI2Óė×ćĮæĀČĘų·“Ó¦Ź±×ŖŅʵĵē×ÓŹżĪŖ2NA
B£®2 L 0.5 mol·L£1ĮņĖį¼ŲČÜŅŗÖŠŅõĄė×ÓĖł“ųµēŗÉŹżĪŖNA
C£®1 mol Na2O2¹ĢĢåÖŠŗ¬Ąė×Ó×ÜŹżĪŖ4NA
D£®±ūĻ©ŗĶ»·±ūĶé×é³ÉµÄ42 g»ģŗĻĘųĢåÖŠĒāŌ×ÓµÄøöŹżĪŖ6NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚ100”ꏱ£¬½«0.50 mol N2O4ĘųĢåĶØČėµ½Ģå»żĪŖ5.0 LµÄÕęæÕĆܱÕČŻĘ÷ÖŠĮ¢¼“³öĻÖŗģ×ŲÉ«£¬·“Ó¦½ųŠŠµ½2ĆėŹ±£¬NO2µÄÅضČĪŖ0.02 mol/L£¬60ĆėŹ±ĢåĻµŅŃ“ļĘ½ŗā£¬“ĖŹ±ČŻĘ÷ÄŚŃ¹ĒæĪŖæŖŹ¼µÄ1.6±¶£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A”¢Ē°2ĆėŅŌN2O4µÄÅØ¶Č±ä»Æ±ķŹ¾µÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ0.010 mol/(L”¤s)
B”¢ŌŚ2ĆėŹ±ĢåĻµÄŚŃ¹ĒæĪŖæŖŹ¼Ź±µÄ1.1±¶
C”¢Ę½ŗāŹ±ĢåĻµÄŚŗ¬N2O4 ĪŖ0.25mol
D”¢Ę½ŗāŹ±Čē¹ūŃ¹ĖõČŻĘ÷Ģå»ż£¬ŌņæÉŅŌĢįøßN2O4µÄ×Ŗ»ÆĀŹ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com