
| A、前者呈蓝色,后者先变红后褪色 |
| B、前者呈蓝色,后者呈红色 |
| C、前者褪色,后者呈红色 |
| D、两者都褪色 |
 特高级教师点拨系列答案
特高级教师点拨系列答案科目:高中化学 来源: 题型:
| A、盐类的水解过程破坏了纯水的电离平衡 |
| B、盐类的水解是酸碱中和反应的逆过程 |
| C、盐类水解的结果使溶液不一定呈中性 |
| D、Na2CO3水解的实质是Na+与H2O电离出的OH-结合生成了NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知X、Y、Z、E、F五种常见物质含有同一元素M,在一定条件下它们有如下转化关系,Z是NO,下列推断不合理的是( )
已知X、Y、Z、E、F五种常见物质含有同一元素M,在一定条件下它们有如下转化关系,Z是NO,下列推断不合理的是( )| A、X可能是一种氢化物 |
| B、F中M元素的化合价可能为+5 |
| C、E可能是一种有色气体 |
| D、若X为单质,Y生成Z属于化合反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、高锰酸钾溶液中,H+、Na+、SO42-、葡萄糖分子能够大量共存 |
| B、向含有4molFeBr2的溶液中通入3molCl2,充分反应的离子方程式:4Fe2++2Br-+3Cl2=4Fe3++6Cl-+Br2 |
| C、某温度下,PH=7的CH3COOH与CH3COONa混合溶液,一定存在C(Na+)=C(CH3COO-)>C(H+)=C(OH-) |
| D、25℃,已知Kap[Cu(OH)2]=2.2×10-20,在0.10mol?L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=2.2×10-14mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
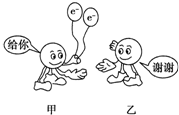 如图为反应3Cu+8HNO3(稀)=3Cu(NO3)3+2NO↑+4H2O中电子转移的关系图,则图中的元素甲、乙分别表示( )
如图为反应3Cu+8HNO3(稀)=3Cu(NO3)3+2NO↑+4H2O中电子转移的关系图,则图中的元素甲、乙分别表示( )| A、Cu,O | B、Cu,H |
| C、H,O | D、Cu,N |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、163 | B、126 |
| C、60 | D、120 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去)下列推断错误的是( )
由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去)下列推断错误的是( )A、若A是单质,B和D的反应是OH-+HCO
| ||||
B、若D为CO,C能和E反应,则A一定为Na2O2,其电子式是Na+[ ]2-Na+ ]2-Na+ | ||||
| C、若D为白色沉淀,与A摩尔质量相等,则X一定是铝盐 | ||||
| D、若X是Na2CO3,C为含极性键的分子,则A一定是氯气,且D和E能发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、7.8gNa2S固体和7.8 gNa2O2固体中含有的阴离子数目均为0.1NA |
| B、0.1mol?L-1的NaHSO4溶液中含有阳离子的物质的量为0.2mol |
| C、常温常压下,氧原子总数为0.2NA的SO2和O2的混合气体,其体积约为2.24L |
| D、标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com