
| A. | 78gNa2O2晶体中所含离子数约为1.806×1024 | |
| B. | 4.48L氨气分子中含0.6NA个N-H键 | |
| C. | PCl3和BCl3分子中所有原子的最外层都达到8电子稳定结构 | |
| D. | N2H4分子中极性键和非极性键的比值为1:4 |
分析 A.根据n=$\frac{m}{M}$计算物质的量,过氧化钠是2个钠离子和1个过氧根离子构成;
B.没有说明是标准状况下,无法计算;
C.分子中原子价电子数加上化合价的绝对值即是该原子的最外层电子数;
D.根据N2H4的结构式分析.
解答 解:A.78g Na2O2固体物质的量=$\frac{78g}{78g/mol}$=1mol,过氧化钠是2个钠离子和1个过氧根离子构成,则离子的物质的量为3mol,所以所含离子数约为1.806×1024,故A正确;
B.没有说明是标准状况下,无法计算氨气的物质的量,所以不能计算分子中的N-H键数,故B错误;
C.PCl3分子中所有原子的最外层都达到8电子稳定结构,BCl3分子中B原子的最外层电子数为6,故C错误;
D.N2H4的结构式为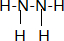 ,分子中含有1个N-N非极性键和4个N-H极性键,则极性键和非极性键的比值为4:1,故D错误;
,分子中含有1个N-N非极性键和4个N-H极性键,则极性键和非极性键的比值为4:1,故D错误;
故选A.
点评 本题考查了物质的量的计算、气体摩尔体积、8电子稳定结构、极性键和非极性键等,题目涉及的知识点较多,侧重于基础知识的应用的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2L的戊烷所含的分子数为0.5NA | |
| B. | 28g乙烯所含共用电子对数目为4NA | |
| C. | 1 mol甲基的电子数目为10NA | |
| D. | 现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲、乙、丙属同系物均可与氯气、溴蒸气发生取代反应 | |
| B. | C5H12表示一种纯净物 | |
| C. | 甲、乙、丙中,丙的沸点最低 | |
| D. | 乙有3种不同沸点的二氯取代物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化碳是形成酸雨的主要物质 | |
| B. | 随意丢弃废电池会对生态环境造成危害 | |
| C. | 任意排放工业废水会导致土壤和水源的污染 | |
| D. | 燃煤时加入适量的石灰可减少二氧化硫的排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
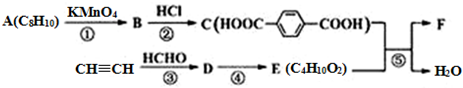
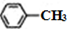 $\stackrel{KMnO_{4}}{→}$
$\stackrel{KMnO_{4}}{→}$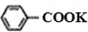
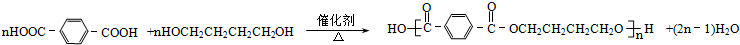 .
.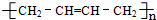
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当参加反应的O2等物质的量时,反应①、②中电子转移数目相等 | |
| B. | 反应①中氧化剂是氧气和水 | |
| C. | 与铜质水龙头连接处的钢质水管不易发生腐蚀 | |
| D. | 钢铁在潮湿的空气中不能发生电化学腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{m}{A+16}$(A-n+8)mol | B. | $\frac{m}{A+16}$(A-n+10)mol | C. | (A-n+2)mol | D. | $\frac{m}{A+16}$(A-n+6)mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第二周期ⅡA族 | B. | 第三周期ⅡA族 | C. | 第三周期ⅢA族 | D. | 第二周期ⅢA族 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com