
【题目】不能说明反应P(g)+Q(g)![]() R(g)+S(s)在恒温、恒容下已达到平衡的是( )
R(g)+S(s)在恒温、恒容下已达到平衡的是( )
A.反应容器内的压强不随时间改变
B.反应容器内P、Q、R、S四者共存
C.P的生成速率和S的生成速率相等
D.反应容器内的气体总物质的量不随时间变化
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】工业上以黄铜矿(主要成分CuFeS2)为原料制备CuSO4·5H2O的主要流程如下:
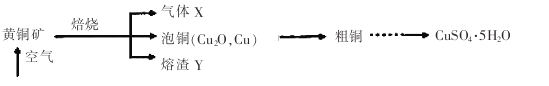
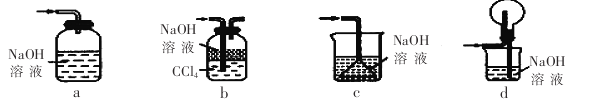
(1)下列装置不能用于吸收气体X的是_____________(填代号)。
(2)熔渣Y的成分为Fe2O3和FeO,选用提供的试剂,设计实验验证熔渣中含有FeO。写出有关实验操作、现象与结论。
提供的试剂:稀盐酸、稀硫酸、KSCN溶液、KMn04溶液、NaOH溶液、氯水。 。
(3)向粗铜中加入硫酸和硝酸的混酸溶液制取硫酸铜时(杂质不参加反应),混酸中HNO3与H2SO4的最佳物质的量之比为
(4)用滴定法测定所得产品中CuSO4.5H2O的含量,称取ag样品配成100 mL溶液,取出20.00 mL,用c mol.L-l滴定剂EDTA( H2Y2-)标准溶液滴定至终点(滴定剂不与杂质反应),消耗滴定剂bmL。滴定反应如下:Cu2++ H2Y2-= CuY2-+ 2H+,则CuSO4·5H2O质量分数为_____________。滴定管用蒸馏水洗涤后,直接注入标准溶液,则会导致测定结果偏 。(填“偏高”、“偏低”和“无影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O、Br2。
(1)已知KBrO3在反应中得到电子,则该反应的氧化产物是________。
(2)0.2 mol KBrO3在反应中得到_____________ mol电子生成 Br2。
(3)根据上述反应可推知________。
a.氧化性:KBrO3>H3AsO4 b.氧化性:H3AsO4>KBrO3
c.还原性:AsH3> Br2 d.还原性:Br2>AsH3
(4)将氧化剂和还原剂的化学式及其配平后的化学计量数填入下列方框中,并标出电子转移的方向和数目(用单线桥法):![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用12mol·L-1浓盐酸配制100mL 4.20mol·L-1稀盐酸的实验步骤如下:
①计算所需取用浓盐酸的体积 ②量取一定体积的浓盐酸 ③溶解 ④转移、洗涤 ⑤振荡 ⑥定容 ⑦摇匀 ⑧烧瓶贴标签。完成下列问题:
(1)所需取用的浓盐酸体积是 mL,量取浓盐酸所用的量筒的规格是 (从下列中选用) A.10mL B.25mL C.50mL D.100mL
(2)第⑥步实验的操作是 。
(3)下列情况对所配制的浓盐酸有何影响?(用“偏大”“偏小”“无影响”填写)
A.所用的浓盐酸长时间放置在密封不好的容器中 ;
B.容量瓶用蒸馏水洗涤后残留少量的水 ;
C.量完溶液,洗涤量筒,并将洗涤液转入容量瓶 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学在生活中应用广泛,下列物质性质与对应用途错误的是
A. 明矾易水解生成胶体,可用作净水剂
B. 晶体硅熔点高硬度大,可用作芯片
C. 氮气化学性质稳定,可用作粮食保护气
D. NaClO具有强氧化性,可作织物漂白剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.凡含碳元素的化合物都是有机化合物
B.烃是指仅含碳和氢两种元素的有机物
C.烃是指燃烧后生成二氧化碳和水的有机物
D.所有的有机物均难溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铁在现代生产和生活中应用广泛。某化学研究性学习小组模拟工业生产流程制备无水氯化铁并对产物做了如下探究实验。

经查阅资料得知:①无水氯化铁在空气中易潮解,加热易升华;②工业上,向500—600℃的铁屑中通入氯气可生产无水氯化铁;③向炽热铁屑中通入氯化氢可以生产无水氯化亚铁和氢气。
请回答下列问题:
(1)装置的连接顺序为_______________(用a、b、c…h表示)。
(2)若缺少装置E对本实验造成的影响是________________________。
(3)工业生产中,会将D中干燥剂换成无水氯化钙,通过D后产生的过量氯气再用氯化亚铁溶液吸收,得到氯化铁溶液作为副产品。氯化亚铁溶液因吸收C12失去作用而失效,下列试剂中能够检验氯化亚铁溶液是否完全失效的是_______________。
a.硫氰酸钾溶液 b.铁氰化钾溶液 c.高锰酸钾溶液 d.烧碱溶液
(4)实验结束并冷却后,将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验:

淡红色溶液中加入过量H2O2后溶液红色加深的原因是___________________(用离子方程式表示)。
已知红色褪去的同时有气体生成,经检验为O2。该小组对红色褪去的原因进行探究。

根据实验现象判断,以下说法正确的是_________________________。(填标号)
a.实验I说明是SCN发生了反应而不是Fe3+发生反应
b.实验I说明是Fe3+发生了反应而不是SCN-发生反应
c.实验I中第3份溶液中生成的白色沉淀为BaSO3
d.实验Ⅱ排除H2O2分解产生的O2氧化SCN-的可能
由实验I和Ⅱ得出结论为_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的定容容器中,当下列哪些物理量不再发生变化时,表明反应A(g)+2B(g)![]() C(g)+D(g)已达到平衡状态的是( )
C(g)+D(g)已达到平衡状态的是( )
①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度 ④混合气体的总物质的量 ⑤混合气体的平均相对分子质量 ⑥v(C)与v(D)的比值 ⑦混合气体的总质量
A.②③④⑤⑥⑦ B.①③④⑤ C.①②③④⑤⑦ D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为响应 “APEC蓝”号召,保护好蓝天白云,减轻“雾霾”,应采用的措施是
A. 尽量使用化石燃料 B. 尽力发展清洁能源
C. 增加工厂烟囱高度 D. 夜间排放工业废气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com