
化学已经渗透到人类生活的各个方面,下列说法不正确的是
A. 食盐可作氯碱工业的原料
B. 碘酒是指单质碘的乙醇溶液
C. 大量使用化肥和农药,以提高农作物产量,符合绿色化学的原则
D. 低碳生活注重节能减排,尽量使用太阳能等代替化石燃料,减少温室气体的排放
科目:高中化学 来源: 题型:
已知1,3丁二烯之间能够发生与1,4加成相似的聚合反应。写出下面的有机物发生聚合反应的化学方程式。
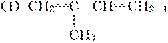
(2)1,3丁二烯和苯乙烯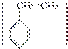 按物质的量之比1∶1发生加聚反应。
按物质的量之比1∶1发生加聚反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
测定有机化合物中碳和氢组成常用燃烧分析法,下图是德国化学家李比希测定烃类有机物组成的装置,氧化铜作催化剂,在750 ℃左右使有机物在氧气流中全部氧化为CO2和H2O,用含有固体氢氧化钠和高氯酸镁[Mg(ClO4)2]的吸收管分别吸收CO2和H2O。
试回答下列问题:
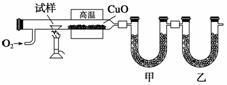
(1)甲装置中盛放的是__________,甲、乙中的吸收剂能否颠倒?说明理由:
________________________________________________________________________。
(2)实验开始时,要先通入氧气一会儿,然后再加热。为什么?
(3)若测得甲装置增重a g,乙装置增重b g,试求出烃中碳、氢原子个数比为________________。
(4)若已知试样是纯净物,某次测定时,测出碳、氢原子个数比为N(C)∶N(H)=11∶23,能否确定其为何种烃?________(填“能”或“不能”);若能,写出其分子式________(若不能,此空不必回答)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验原理或操作正确的是

A.用图1装置验证在该条件下铁钉发生吸氧腐蚀
B.用湿润的蓝色石蕊试纸检验氨气
C.用20mL量筒量取15mL酒精,加水5mL,配制质量分数为75%酒精溶液
D.用图2装置检验实验室制得的乙烯中混有SO2和CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验、现象及相关结论均正确的是( )
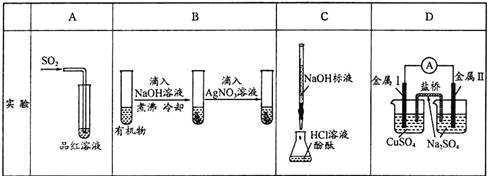
| 现象 | 品红褪色 | 最后试管有浅黄色沉淀 | 最后一滴溶液使酚酞由无色变为粉红色,且30秒不复原 | 盐桥左端从 无色逐渐变为 蓝色 |
| 结论 |
氧化性 | 有机物中含 有溴原子 | 滴定达到终点 | 金属II比I活泼 |
查看答案和解析>>
科目:高中化学 来源: 题型:
铝生产产业链由铝土矿开采、氧化铝制取、铝的冶炼和铝材加工等环节构成。请回答下列问题:
(1)工业上采用电解氧化铝—冰晶石(Na3AlF6)熔融体的方法冶炼得到金属铝:2Al2O3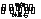 4Al+3O2↑
4Al+3O2↑
加人冰晶石的作用是_____________________。
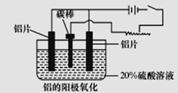
(2)上述工艺所得铝材中往往含有少最Fe和Si等杂质,可用电解方法进一步提纯,该电解池中阳极的电极反应式为_____________,下列可作阴极材料的是____________(填字母序号)。
A.铝材 B.石墨 C.铅板 D.纯铝
(3)阳极氧化能使金属表面生成致密的氧化膜。以稀硫酸为电解液,铝阳极发生的电极反应式为__________。
(4)在铝阳极氧化过程中,需要不断地调整电压,理由是______________________________。
(5)下列说法正确的是(填字母序号)。
A.阳极氧化是应用原电池原理进行金属材料表面处理的技术
B.铝的阳极氧化可增强铝表面的绝缘性能
C.铝的阳极氧化可提高金属铝及其合金的耐腐蚀性,但耐磨性下降
D.铝的阳极氧化膜富有多孔性,有很强的吸附性能,能吸附染料而呈各种颜色
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是
A. 铝溶于NaOH溶液:Al+2OH—=AlO2—+H2↑
B. 铜溶于稀硝酸:3Cu+ 8H+ +2NO3—=3Cu2+ +2NO↑ + 4H2O
C. 碳酸镁中滴加稀盐酸:CO32—+2H+ =CO2↑ + H2O
D. 稀硫酸中滴加氢氧化钡溶液:H++ OH—=H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学取一定量的Al、Fe混合物,与2.0L极稀的HNO3充分反应,假设HNO3的还原产物全部为铵盐。在反应后的溶液中,逐滴加入4mol·L-1的NaOH溶液,所加NaOH溶液的体积与产生的沉淀的物质的量的关系如图所示。分析图像回答问题:
(1)DE段发生反应的离子方程式为:_____________________________________ 。
(2)请写出任意一个Al、Fe与极稀HNO3反应的化学方程式:_______________ 。
(3)B点对应的沉淀的物质的量为_______mol,C点对应的氢氧化钠溶液的体积为______mL。
(4)原硝酸溶液的物质的量浓度为_______mol/L。

查看答案和解析>>
科目:高中化学 来源: 题型:
已知可逆反应温度为T0时,在容积固定的密闭容器中发生X(g)+Y(g) Z(g)(未配平)反应,各物质浓度随时间变化的关系如图a所示。其他条件相同,温度分别为T1、T2时发生反应;Z的浓度随时间变化的关系如图b所示。下列叙述正确的是( )
Z(g)(未配平)反应,各物质浓度随时间变化的关系如图a所示。其他条件相同,温度分别为T1、T2时发生反应;Z的浓度随时间变化的关系如图b所示。下列叙述正确的是( )

A.发生反应时,各物质的反应速率大小关系为v(X)=v(Y)=2v(Z)
B.图a中反应达到平衡时,Y的转化率为37.5%
C.T0时,该反应的平衡常数为33.3 D.该反应正反应的反应热ΔH<0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com