

| ||
| �� |
| ||
| �� |
| ||
| �� |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��21.2 g |
| B��21.6 g |
| C��22.0 g |
| D��22.3 g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
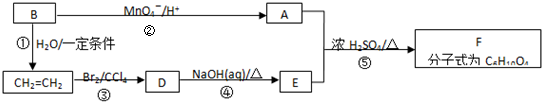
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������ᴿ������˳���ǣ��ܽ⡢���ˡ�������ϴ�� |
| B��ʵ������ȡ������Ϻ�Ӧ��ȡ������ƿ����ȡ�����ܣ����ֹͣ���� |
| C��������Ũ�����������ϣ�Ӧ�����ռ���Һ�кͣ�����ʪ��Ĩ�� |
| D�����Թܼмг��Թ�ʱ�����Թܼд��Թܵײ������ף������Թ����ϲ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
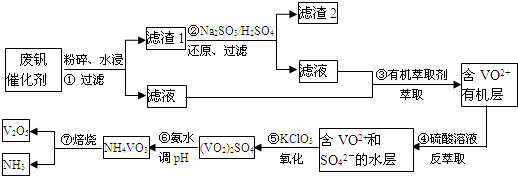
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
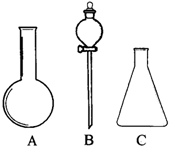 ��1������ͼ��ʾA��B��C������������ѡ�������������Ƶ���ţ�������Ӧ�Ŀո��ڣ����ձ�����ͨ©����Բ����ƿ����ƿ�ݷ�Һ©������ʽ�ζ���
��1������ͼ��ʾA��B��C������������ѡ�������������Ƶ���ţ�������Ӧ�Ŀո��ڣ����ձ�����ͨ©����Բ����ƿ����ƿ�ݷ�Һ©������ʽ�ζ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����Ƶ�Cu��OH��2����Һ |
| B����ˮ |
| C��NaOH��Һ |
| D��ϡ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com