
【题目】下列事实中,能说明氯元素的非金属性比硫元素的非金属性强的是( )
①盐酸的酸性比氢硫酸(H2S水溶液)酸性强 ②HCl的稳定性比H2S强 ③相同条件下,Cl2与铁反应生成FeCl3 ,而S与铁反应生成FeS ④Cl2能与H2S反应生成S ⑤酸性强弱:硫酸<高氯酸
A. ①②③④B. ②③④C. ①②③④⑤D. ②③④⑤
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,回答下列有关问题:
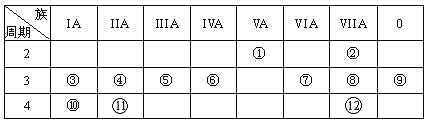
(1)写出下列元素符号:① _________,⑥_________,⑦_______。
(2)画出原子的结构示意图:④__________,⑧____________。
(3)在①~12元素中,金属性最强的元素是______,非金属性最强的元素是____,最不活泼的元素是_____。(均填元素符号)
(4)元素⑦与元素⑧相比,非金属性较强的是______(用元素符号表示),下列表述中能证明这一事实的是________。
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(5)第三周期中原子半径最大的元素是___(填序号),跟它同周期原子半径最小的元素是__(填序号),它们可以形成____(填离子或共价)化合物,用电子式表示其形成过程:____。(6)已知某元素原子最外层电子数是其次外层电子数的2倍,该元素可以与⑧形成一种AB4型的化合物,请用电子式表示其形成过程:_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如下图所示(图中有些反应的生成物和反应的条件没有标出)。
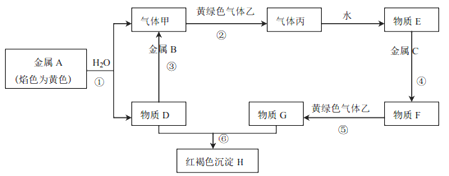
请回答下列问题:
(1)写出 B、乙的化学式:B______、乙________, E的名称:________。
(2)写出下列反应的化学方程式:
反应⑤ _______________;
反应⑥________________。
(3)写出下列反应的离子方程式:
反应①___________;
反应③______________;
(4)若向F的溶液中滴入适量D的溶液,现象是:________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是 ( )
A. F2、Cl2、Br2、I2的氧化性逐渐增强
B. VIA族元素的原子,其半径越大,越容易得到电子
C. 同周期元素中,VIIA族元素的原子半径最大
D. 元素周期表中从IIIB到IIB的10个纵列的元素都是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家预测原子序数为114的元素,具有相当稳定性的同位素,它的位置在第7周期IVA族,称为类铅。关于它的性质,预测错误的是
A.它的最外层电子数为4B.它的金属性比铅强
C.它具有+2、+3、+4价D.它的最高价氧化物的水化物是强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】混合物的分离方法①过滤,②蒸发,③蒸馏,④分液,⑤萃取,请从上面选择下列各混合物的分离方法(填序号)
(1)食盐水与泥沙______
(2)苯和水______
(3)蒸馏水的制取_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A. 人类历史上使用最早的合金是青铜
B. 钢属于铁合金
C. 目前世界上使用量最大的合金是铝合金
D. 目前世界上用途最广的是合金钢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硅单质及其化合物的说法错误的是( )
A.硅是构成岩石和矿物的基本元素
B.粗硅制备单晶硅不涉及氧化还原反应
C.高纯度的硅单质广泛用于制作半导体材料
D.水泥、玻璃、陶瓷都是硅酸盐产品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于A2 + 3B2![]() 2C+D的反应来说,以下化学反应速率的表示中,反应速率最快的是( )
2C+D的反应来说,以下化学反应速率的表示中,反应速率最快的是( )
A.v(B2) =0.8mol(Ls)-1 B.v(A2) =0.4 mol(Ls)-1
C.v(C) =0.6 mol(Ls)-1 D.v(D) =0.1 mol(Ls)-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com