
�������̿������ɵ��ȥ�������ϳɹ�ҵ�Ĵ�������������������ҵ���´ɹ�ҵ����ɫ������ɫ�����������ȡ�
��(1)п—�̼��Ե�ؾ��������ŵ��������ص㣬����õ��㷺Ӧ�á���ص��ܷ�ӦʽΪZn(s)��2MnO2(s)��H2O(l)===Zn(OH)2(s)��Mn2O3(s)��
��ص�������ӦʽΪ________________________________
��ij��ѧ�о���ѧϰС����ӷϾɸɵ���л��ն���������ȡ̼���̡�
�ٽ��ɵ�����С���ѡ�õ���ɫ������Ҫ�ɷ�ΪMnO2��ϴ�ӡ����ˡ���ɡ�
�ڽ��������尴��Һ�����2:9����Ũ���ᡢ���ȣ���Ӧ��ȫ����ˡ�Ũ����
����������Һ�м���Na2CO3��Һ���ӱ߽��裬�ٹ��˼��ɵõ�̼���̡�
��2���ڵڢڲ��У�������������Ũ�����ϵ�Ŀ����________________________________
��3��������Ϊ�����ڢ۲��е�Na2CO3��Һ����NH4HCO3��Һ��Ҳ�ܴﵽ����Ŀ�ģ���ͬʱ���������ɡ���д������NH4HCO3��Һʱ���������ӷ�Ӧ����ʽ��
_______________________________________
�� ʪ�����̼������������Һ��������̵��������̷�Ϊ���Ͻ�ȡ�������������������ӡ���Ʒ���ա������������������£�
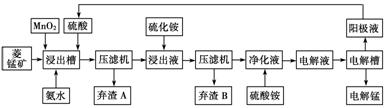
��֪�������̿�����Ҫ�ɷ���̼���̣���Ҫ������Fe2����Co2����Ni2����
���������������pH���±�������ij����Ũ��С�ڵ���10-5mol/L������Ϊ��ȫ������
| ���� | Fe(OH)2 | Ni(OH)2 | Co(OH)2 | Mn(OH)2 |
| ��ʼ����pH | 7.5 | 7.7 | 7.6 | 8.3 |
| ��ȫ����pH | 9.7 | 8.4 | 8.2 | 9.8 |
��������������������pKsp����(pKsp����lgKsp)��
| �������� | Fe(OH)3[��Դ��ȫ,Ʒ����&��*��+��] | Ni(OH)2 | Co(OH)2 | NiS | CoS |
| pKsp | 38.55 | 15.26 | 14.7 | 18.49 | 20.40 |
��4�����̿�������ᷴӦ�Ļ�ѧ����ʽ��________________________________��
��5��ʹ�ð�ˮ��Ŀ���ǵ���pHֵ��________֮��(��pH��Χ����ȷ��С�����1λ����)��
�ڡ�����Һ���м���(NH4)2S����泥���Ŀ����_________________________________
��6��������ʹ�õ��Ƕ��Ե缫�壬��ⷴӦ����ʽΪ_________________________
��֪ʶ�㡿���ܵ���ʵ��ܽ�ƽ�⼰����ת���ı��ʡ��Ʊ�ʵ�鷽�������
���𰸽����� (ÿ��2��)��1��2MnO2+2e-+H2O=2OH-+Mn2O3 ��2����MnO2��ԭ��Mn2+
��3��Mn2++2HCO3-=MnCO3��+CO2��+H2O (4)MnCO3+H2SO4=MnSO4+H2O+CO2��
(5)3.8��8.3 ��������������NiS���� (6)2MnSO4+2H2O  2H2SO4+O2��+2Mn
2H2SO4+O2��+2Mn
��������1��п—�̼��Ե�ص��ܷ�ӦʽΪZn(s)��2MnO2(s)��H2O(l)===Zn(OH)2(s)��Mn2O3(s),
Zn���ϼ����ߣ�ʧ���ӣ���������MnO2�е�Mn���ϼ۽��ͣ��õ��ӣ��������������ܷ�Ӧ��������뷴Ӧ����ص�������ӦʽΪ��2MnO2+2e-+H2O=2OH-+Mn2O3
(2)Ũ������������̷���������ԭ��Ӧ�������������Ȼ��̣��Ա��ڼ���̼���ƺ��������̼���̳�����
��3������NH4HCO3��Һʱ���������壬���ӷ���ʽΪ��Mn2++2HCO3-=MnCO3��+CO2��+H2O
��4�����̿����Ҫ�ɷ���̼���̣������ᷴӦ���������̡�ˮ�Ͷ�����̼����ѧ����ʽ��:
MnCO3+H2SO4=MnSO4+H2O+CO2��
��5����������MnO2���������ԣ��ܽ����̿�������ȡҺ�е�Fe2+����ΪFe3+�� ��ˮ���Խ������ӳ���������������Ksp=c3��OH-��•c��Fe3+������������ȫ����ʱ�������ӵ�Ũ����1��10-5mol/L����ʱc��OH-��= = 10-11.2mol/L������pH=3.8�����Խ������ӳ�����ȫ������������δ�����ķ�Χ��3.8��8.3���˷�Χ��Co2+�Ѿ�������ȫ�������ټ�����什�Ni2+������
= 10-11.2mol/L������pH=3.8�����Խ������ӳ�����ȫ������������δ�����ķ�Χ��3.8��8.3���˷�Χ��Co2+�Ѿ�������ȫ�������ټ�����什�Ni2+������
��6�����ݵ��صĹ���ԭ�������������������Һ���ɶ������̡��������������ⷴӦ����ʽΪ��
2MnSO4+2H2O  2H2SO4+O2��+2Mn
2H2SO4+O2��+2Mn
��˼·�㲦��������һ��ʵ�鷽����ƵĹ���������Ŀ������ѧ����������ۺ�֪ʶ�����������ǵڣ�5���⣬�������̽������������ٵ���PH�ļ����Ѷȴ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��pH��13����ɫ��Һ�У����Դ��������һ�������� (����)
A��NH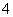 ��NO
��NO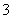 ��K����SO
��K����SO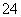
B��CO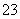 ��NO
��NO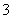 ��HCO
��HCO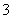 ��Na��
��Na��
C��Na����ClO����AlO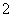 ��NO
��NO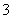
D��Cu2����K����Na����SO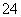
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��CO2����ͨ��CaCl2��Һ�У���Ҫ�а�ɫ�����������ɼ�����Լ���(����)
A�����������Һ B��̼�������Һ
C����ˮ D������������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ͼʾ���Ӧ���������������
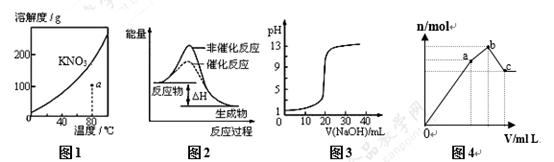
A��ͼ1��ʾKNO3���ܽ�����ߣ�ͼ��a����ʾ����Һ��80��ʱKNO3�IJ�������Һ
B��ͼ2��ʾij���ȷ�Ӧ�ֱ����С�����������·�Ӧ�����е������仯
C��ͼ3��ʾ0.1000mol•L-1NaOH��Һ�ζ�20.00mL0.1000mol•L-1������Һ�õ��ζ�����
D��ͼ4 ��ʾ��NH4Al(SO4)2��Һ����ε���Ba(OH)2��Һ������Ba(OH)2��Һ���V�ı仯�����������ʵ���n�ı仯��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���û�ѧ��Ӧԭ��֪ʶ�ش������й�̼��̼�Ļ���������⣺
(1)����β������Ҫ��Ⱦ����NO�Լ�ȼ��ȼ�ղ���ȫ��������CO���������ִ������е���Ҫ������Ⱦ�Ϊ�˼�������β����ɵĴ�����Ⱦ�����ǿ�ʼ̽������NO��CO��һ��������ת��Ϊ����������E��F�ķ���(��֪�÷�Ӧ��H<0). ��2 L�ܱ������м���һ����NO��CO�����¶ȷֱ���T1��T2ʱ����ø�����ƽ��ʱ���ʵ������±���
T/�� n/mol | NO | CO | E | F |
��ʼ | 0.100 | 0.100 | 0 | 0 |
T1 | 0.020 | 0.020 | 0.080 | 0.040 |
T2 | 0.010 | 0.010 | 0.090 | 0.045 |
�������ϱ����ݣ�д��NO��CO��Ӧ�Ļ�ѧ����ʽ .
��������ӦT1��ʱ��ƽ�ⳣ��ΪK1��T2��ʱ��ƽ�ⳣ��ΪK2�����ݱ������ݼ���K1= �����ݱ��������жϣ��¶�T1��T2�Ĺ�ϵ��(�����)__________��
A��T1>T2B��T1<T2 C��T1=T2 D�����Ƚ�
(2)��Ӧ���ɵ�����E�������������������գ�����0.4molE������200mL 3mol/L NaOH��Һ������ȫ���գ���Һ������Ũ���ɴ�С��˳��Ϊ�� .
(3)��֪CH4��H2��CO��ȼ���ȷֱ�Ϊ890.3kJ/mol��285.8 kJ/mol��283.0 kJ/mol����ҵ��������Ȼ��(��Ҫ�ɷ���CH4)��CO2���и��������Ʊ�CO��H2��д���÷�Ӧ���Ȼ�ѧ����ʽ�� .
(4)CO����������ȼ�ϵ�ص�ȼ�ϣ�ij������ȼ�ϵ�ؾ��иߵķ���Ч�ʣ�����ܵ����ӣ��õ���� Li2CO3 �� Na2CO3 �������λ����������ʣ�COΪ����ȼ����������CO2 �Ļ����Ϊ������ȼ�����Ƶ��� 650 ���¹�����ȼ�ϵ�أ�д���为���������缫��Ӧ����ʽ�������� �������� .
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ͼ��ʾ����̽��������ʴ������ʵ��װ��ͼ�������ʵ�鲢�ش��������⣺
��1������ʼʱ�ס��ҡ���3��װ�õĵ�����Һ��߶���ͬ����һ��ʱ���Һ����ߵ���_____��
��2��ͨ���ס���װ�õĶԱ�˵��������̼�ĺ���Խ________����ߡ��͡�������Խ��ʴ��
��3����װ���з����绯ѧ��ʴʱ�����ĵ缫��ӦʽΪ__________________________ ��
�����û�ѧ��Ӧ��2FeCl3+Cu===2FeCl2+CuCl2 ������ѡ����ʵĵ缫���Ϻ͵������Һ�����һ��ԭ��ء��ɹ�ѡ��ĵ缫���ϣ�������ͭ����ʯī����
�ɹ�ѡ��ĵ������Һ��CuCl2��Һ��FeCl2��Һ��FeCl3��Һ��
����д���пհף�
��1��ѡ��_________���������ϣ�_________���������ϣ�ѡ��____ __���������Һ��
��2��д���йصĵ缫��Ӧʽ��������________________________________��
������_________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������̿������ɵ��ȥ�������ϳɹ�ҵ�Ĵ�������������������ҵ���´ɹ�ҵ����ɫ������ɫ�����������ȡ�
��(1)п—�̼��Ե�ؾ��������ŵ��������ص㣬����õ��㷺Ӧ�á���ص��ܷ�ӦʽΪZn(s)��2MnO2(s)��H2O(l)===Zn(OH)2(s)��Mn2O3(s)��
��ص�������ӦʽΪ________________________________
��ij��ѧ�о���ѧϰС����ӷϾɸɵ���л��ն���������ȡ̼���̡�
�ٽ��ɵ�����С���ѡ�õ���ɫ������Ҫ�ɷ�ΪMnO2��ϴ�ӡ����ˡ���ɡ�
�ڽ��������尴��Һ�����2:9����Ũ���ᡢ���ȣ���Ӧ��ȫ����ˡ�Ũ����
����������Һ�м���Na2CO3��Һ���ӱ߽��裬�ٹ��˼��ɵõ�̼���̡�
��2���ڵڢڲ��У�������������Ũ�����ϵ�Ŀ����________________________________
��3��������Ϊ�����ڢ۲��е�Na2CO3��Һ����NH4HCO3��Һ��Ҳ�ܴﵽ����Ŀ�ģ���ͬʱ���������ɡ���д������NH4HCO3��Һʱ���������ӷ�Ӧ����ʽ��
_______________________________________
�� ʪ�����̼������������Һ��������̵��������̷�Ϊ���Ͻ�ȡ�������������������ӡ���Ʒ���ա������������������£�

��֪�������̿�����Ҫ�ɷ���̼���̣���Ҫ������Fe2����Co2����Ni2����
���������������pH���±�������ij����Ũ��С�ڵ���10-5mol/L������Ϊ��ȫ������
| ���� | Fe(OH)2 | Ni(OH)2 | Co(OH)2 | Mn(OH)2[��Դ��ȫ,Ʒ����&��*��+��] |
| ��ʼ����pH | 7.5 | 7.7 | 7.6 | 8.3 |
| ��ȫ����pH | 9.7 | 8.4 | 8.2 | 9.8 |
��������������������pKsp����(pKsp����lgKsp)��
| �������� | Fe(OH)3 | Ni(OH)2 | Co(OH)2 | NiS | CoS |
| pKsp | 38.55 | 15.26 | 14.7 | 18.49 | 20.40 |
��4�����̿�������ᷴӦ�Ļ�ѧ����ʽ��________________________________��
��5��ʹ�ð�ˮ��Ŀ���ǵ���pHֵ��________֮��(��pH��Χ����ȷ��С�����1λ����)��[��Դ��ȫ,Ʒ����&��*��+��]
�ڡ�����Һ���м���(NH4)2S����泥���Ŀ����_________________________________
��6��������ʹ�õ��Ƕ��Ե缫�壬��ⷴӦ����ʽΪ_________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��FeCl3��Һ��ʴӡˢ��·���ϵ�ͭ�����õ���Һ�м������ۡ��Լ������۳�ַ�Ӧ�����Һ������������
A��������ʣ�࣬����Һ��һ����Fe3�� B�����й�����ڣ�����Һ��һ����Fe2��
C������Һ����Cu2������һ��û�й������� D������Һ����Fe2������һ����Cu����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���д�ʩ����������
A����SO2Ư��ֽ���Ͳ�ñ��
B����������ϴ��¯�е�ˮ��
C���������ý�̿��ԭSiO2��ȡ�ֹ�
D���� Na2S������������ȥ��ˮ�е�Cu2+��Hg2+
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com